Artikli meditsiiniline ekspert
Uued väljaanded
Ravimid
Antipsühhootikumid või antipsühhootikumid
Viimati vaadatud: 23.04.2024

Kõik iLive'i sisu vaadatakse meditsiiniliselt läbi või seda kontrollitakse, et tagada võimalikult suur faktiline täpsus.
Meil on ranged allhanke juhised ja link ainult mainekate meediakanalite, akadeemiliste teadusasutuste ja võimaluse korral meditsiiniliselt vastastikuste eksperthinnangutega. Pange tähele, et sulgudes ([1], [2] jne) olevad numbrid on nende uuringute linkideks.
Kui tunnete, et mõni meie sisu on ebatäpne, aegunud või muul viisil küsitav, valige see ja vajutage Ctrl + Enter.
Antipsühhootikumid (neuroleptikumid) - psühhotroopsete ravimite klass, mida kasutatakse peamiselt skisofreenia raviks. Praegu on tavaks eristada kahte ravimi rühma (või kategooriaid): tüüpilised ja atüüpilised antipsühhootikumid. Alljärgnevalt on toodud andmed ravimi farmakoloogiliste omaduste, ravimi määramise näitude ja kõrvaltoimete kohta.
Näidustused tüüpiliste antipsühhootikumide määramiseks
Praegu on traditsiooniliste neuroleptikumide määramise peamised näited psühhofarmakoterapeudi autoriteetsete teadlaste soovituste kohaselt järgmised.
- Relief agitatsiooni ja käitumishäired, mille põhjuseks on rasked psühhootilisi sümptomeid. Nendel juhtudel, see näitab kasutamist suukaudse või parenteraalse preparaate, millel on antipsühhootiline toime nii globaalse (hlopromazin, levomepromasiin, tioproperasiini, zuklopentiksool) ja selektiivsed - vormis mõju hallutsinatoorse paranoiline häire (haloperidool, trifluoperasiin).
- Antiretroviirus (ennetav) ravi. Selleks manustatakse depoopreparaatideks, eriti nendel patsientidel kehva ravimit vastavuse (haloperidooldekanoaati, pikenenud kujul flupentiksool) või väikese või keskmise annuse ravimit dezingibiruyuschego (antinegativnogo) toimet, neid ressursse, suurtes annustes kasutatakse leevendust ägeda psühhootiliste häirete (flupentiksool, zuklopentiksool). Seda tüüpi ravi on soovitatav nimetamise nn väikeste antipsühhootilise (tioridasiin. Chlorprothixenum, sulpiriidiga), psühhotroopsete tegevus, mis seisneb mõju avaldumist depressiivne masti ja dissomnicheskie häire.
- Ägedate psühhootiliste seisundite juhtimisega ravile antikehadevastase resistentsuse ületamine. Selleks kasutamine on üldiselt parenteraalselt traditsiooniliste antipsühhootikumide kellel globaalse (kloörpromasiin levomepromasiin jt.) Ja selektiivsed (haloperidool) antipsühhootilise toime.
Need ravimid põhjustavad mitmeid kõrvaltoimeid, mille olemus sõltub omaduste farmakoloogilise profiili Iga preparaadi. Antipsühhootikumide rohkem väljendunud antikolinergiline toime põhjustab tõenäolisemalt akommodatsioonihäireid, kõhukinnisust, suukuivust. Uriini säilitamine. Sedatsiooni on tüüpilised antipsühhootikumid enam väljendunud antihistaminiini efekt ja ortostaatiline hüpotensioon - blokeerivate ainetega a1-adrenoretseptorite suhtes. Blokaadi tavapäraste neuroleptikumide kolinergilistel ja dopamiinergiliste edastamise nordrenergicheskoy võib viia mitmete häirete seksuaalse sfääri, nagu amenorröa ja düsmenorröa, Anorgasmia, galaktorröale, turse ja valulikkus rindkere näärmed, vähendatud kangust. Kõrvaltoimeid suguelundite piirkonnas on valdavalt seotud holino- adrenoblokaatorraviga omadused ja neid ravimeid, vaid ka - suurenemisega prolaktiini sekretsiooni tõttu blokaadi dopamiini metabolismi. Kõige tõsisemad kõrvaltoimed tüüpiliste neuroleptikumid - rikkumine motoorse funktsiooni. Need on kõige sagedasem põhjus, miks patsiendid keelduvad ravist. Kolme põhilised kõrvaltoimed seotud teraapia mõju mootori sfääri, on varajane ekstrapüramidaalnähtude sündroom, tardiivdüskineesia ja ROA.
Usutakse, et ekstrapüramidaalsed sündroomid seostuvad D2-retseptorite blokaadiga basaalganglionides. Need hõlmavad düstooniat, neuroleptilist parkinsonismi ja akatiisiat. Äge düstoonilise reaktsiooni (varajane düskineesia) manifestatsioonid on äkki arenevad hüperkineesist, okuliigilised kriisid, näo ja kere lihaste kokkutõmbed, opisthotonus. Need häired on annusest sõltuvad ja esinevad sageli pärast 2-5 päeva kõrgekvaliteediliste neuroleptikumidega, nagu haloperidool ja flufenasiin. Varajase düskineesia lõpetamiseks vähendage neuroleptiline annus ja antikolinergilisi ravimeid (biperideen, trieksefenidüül). Hiline düskineesia hõlmab tavaliselt kaela lihaseid ja vastupidiselt ägedale düstoonilisele reaktsioonile on antikolinergiliste ravimitega ravitav vähem. Neuroleptilise parkinsonismi puhul, mida iseloomustab spontaansete motoorsete võimete, hüpo- ja amüameemia, rahutu värisemise ja jäikuse vähenemine. Need sümptomid on olulised, et eristada skisofreenia väliseid sarnaseid negatiivseid häireid, mida esindab emotsionaalne võõrandumine, mõjusa lööve ja anergia. Nende kõrvaltoimete korrigeerimiseks on näidatud antikolinergiliste ravimite kasutamine, neuroleptilise annuse vähendamine või selle asendamine atüüpiliste antipsühhootikumidega. Akatiisia väljendub sisemine ärevus, suutmatus püsida ühes kohas pikka aega ja vajadus pidevalt käte või jalgade käes. Selle leevendamiseks kasutage antikoliinergilisi aineid ja ka tsentraalseid beetablokaatoreid (propranolooli).
Hiline düskineesia avaldub mis tahes lihasgrupi tahtmatu liikumise, sagedamini keele ja suu lihaste puhul. Kliiniliselt eristada mitmeid selle vormides: düskineesia põselihased, keele, suu (korduvad vähendamine masticatory lihaseid, luua mulje meest grimassitavaks, keele kogemata ulatuvad patsiendi suhu); tardiivne düstoonia ja tardiivne akatiisia; (patsient teostab pea, tüve, ülemisi ja alajäsemeid, koreoatetoidide liikumisi). Sellised häirevormid registreeritakse peamiselt pikaajalise ravi korral traditsiooniliste antipsühhootikumidega ja neid tuvastatakse ligikaudu 15 ... 20% -l patsientidest, kes neid säilitasid. Ilmselt mõnel patsiendil risk haigestuda düskineesia sümptomite suurenenud, sest mõned neist on kliinikus skisofreenia enne "neuroleptiline ajastu." Lisaks kirjeldatakse vananenud düskineesiat eakatel naistel ja afektiivsete häiretega patsientidel. Oletatakse, et Düskineesianähtude seostatakse suurenenud arvu dopamiiniretseptorie juttkehas, kuigi selle patogeneesis on tõenäoliselt kaasatud ka GABA ja teiste neurotransmitterite süsteeme. Selliste kõrvaltoimete tõhusat terviklikku ravi ei ole olemas. Usutakse, et väikeste dooside manustamisega neuroleptikumide vysokopotentnyh millel dofaminblokiruyuschim tegevuse või vitamiin E võib olla mõõdukas kasulik toime nende häirete. Tardiva düskineesia kõige tõhusam meede on tüüpilise neuroleptilise annuse vähendamine või selle asendamine atüüpiliste antipsühhootikumidega.
Tänapäevaste andmete kohaselt esineb pahaloomulist neuroleptilist sündroomi ligikaudu 0,5% -l psühhofarmakoterapia juhtumitest. Tõenäoliselt harv esinemine on nüüd selline eluohtlike patsiendi saab seletada laialdast kasutuselevõttu atüüpiliste antipsühhootikumide, kui on oht MNS ravis neid vahendeid on tühine. Üldiselt arvatakse, et NSA arengu peamine põhjus on dopamiinergilise süsteemi ülemäärane blokeerimine neuroleptikumidega ravimisel, eriti pärast kõrgekvaliteetsete antipsühhootikumide annuse suurendamist. NSA peamised sümptomid on hüpertermia, skeletilihaste toonuse ja kõõluste reflekside suurenemine, kooma üleminekuga seotud teadvuse rikkumine. Vereanalüüs näitab leukotsütoosi, erütrotsüütide sadestumise määra suurenemist, maksa transaminaaside aktiivsust; uriini analüüsimisel on täheldatud albumiuria esinemist. Kiirelt ilmnevad vee ja elektrolüütide tasakaalu rikkumised, mis loob eeldused aju ödeemi tekkeks. ZNS on ägeda seisundi tõttu, mis nõuab patsiendi kiiret hospitaliseerimist intensiivse infusioonravis. NSA-de ravimine on kõige olulisem hüdratatsioon ja sümptomaatiline ravi. Sellises olukorras nõuavad kõik antipsühhootikumid, mis on välja kirjutatud viivitamatult. Mõnel juhul on dopamiiniretseptori agonistid (nt bromokriptiin) või lihasrelaksantidel positiivne mõju, ehkki nende efektiivsust ei ole uuritud. Pärast ravimi kõrvaltoime kõrvaldamist ei tohi te jätkata antipsühhootikumide võtmist vähemalt kahe nädala jooksul. Tulevikus on võimalik välja kirjutada vähese potentsiaalse antipsühhootikum, eelistatult uue põlvkonna ravim. Uue etteantud ravimi annust tuleks väga hoolikalt jälgida, jälgides elutähtsate funktsioonide seisundit ja laboratoorset teavet (vereanalüüsid, uriinianalüüsid).
Tüüpilised neuroleptikumid põhjustavad suhteliselt harva ohtlikke surmavaid komplikatsioone. Üleannustamise manifestatsioonid on peamiselt seotud ravimi anti-adrenergilise ja antikolinergilise toime individuaalse profiiliga. Kuna neil ainetel on tugev antiemeetiline toime, on näidustatud mao loputamine nende eemaldamiseks kehast, mitte etikettide manustamisest. Arteriaalne hüpotensioon on reeglina adrenoretseptorite blokeerimise tagajärg ja seda tuleb korrigeerida dopamiini ja norepinefriini manustamisega. Kui südame löögisagedus on häiritud, on näidatud lidokaiini kasutamine.
Tüüpiliste antipsühhootikumide toimemehhanism ja farmakoloogilised efektid
Psühhofarmakoloogia väljatöötamisel pakuti antipsühhootikumide mõju neuroretseptoritele mitmesuguseid variante. Peamine on hüpotees nende toime kohta dopamiini neuronstruktsioonidele (peamiselt D2 retseptoritele), mis põhineb andmete põhjal normaalse dopamiini metabolismi psühhooside häirete kohta aju struktuurides. Dopamiini D2 retseptorid asuvad basaalganglionides, külgnevas tuumas ja eesmiste labajalgade ajukoores, mängivad nad juhtivat rolli teabe voolu reguleerimisel korteksi ja talamiini vahel.
Joonis näitab rafineeritud esitlus rikkumise dopamiini transmissiooni koore ja Subkortikaalsetes piirkondades aju ja rolli nende häirete sümptomite tekke ja skisofreenia (kohandatud raamatust RV Jones, Buckley PF, 2006).
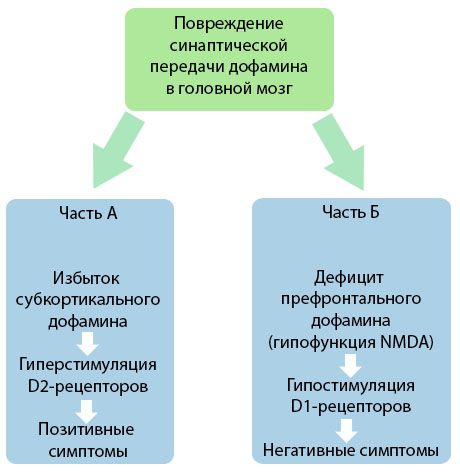
Osa "A" tähistab klassikalise, dopamiini varase teoreetilisest postuleerib liig dopamiini Subkortikaalsetes aladel hüperstimulatsiooni ja D2-retseptorite suhtes, mis toob kaasa produktiivne sümptomeid. Osa "B" näitab teoreetilist moderniseerimist 90ndate alguses. Eelmine sajand. Sel ajal saadud andmed näitasid, et dopamiini puudus retseptorites D; koos puudumine stimuleerimine prefrontaalses ajukoores retseptoritega viib negatiivsete sümptomite, kognitiivsed. Seetõttu leiab Praeguse arusaama mõlemat tüüpi häired dopamiinergilise jõuülekande - küllus ja Subkortikaalsetes dopamiinipuudust prefrontaalses ajukoores - kumuleeruvad tulemusena rikkumist sünaptilise ülekande prefrontaalses ja alatalitlus seostatakse N-metüül-N-aspartaat. Samuti eraldati algselt dopamiini, tuvastati hiljem ja teiste neurotransmitterite patogeneesis osalevate skisofreenia, nagu serotoniin, gammaaminobutirovaya happe, glutamaat, norepinefriini, atsetüülkoliin ja erinevate neuropeptides. Kuigi rolli nende vahendajate ei ole täielikult teada, kuid koos teadmiste arendamist selgub, et ilming arvukalt neurokeemilisi muutusi organismis. Seetõttu kliinilist toimet Antipsühhootikum mõjud on liitmise erinevate retseptorite moodustumist ja viia kõrvaldamiseks häirimist homeostaasi.
Viimastel aastatel on seoses uute ravimite uurimismeetodite ilmnemisega alates radioisotoopide ligandite sidumisest ja PET-i skaneerimisel tehtud märkimisväärseid edusamme neuroleptikumide peentne biokeemilise mehhanismi selgitamisel. Eriti määratakse kindlaks erinevate neuroretseptoritega seonduvate ravimite suhteline tugevus ja troopilisus aju erinevates piirkondades ja struktuurides. Näidatud on ravimi antipsühhootilise toime otsene sõltuvus selle blokeerivast toimest erinevate dopamiinergiliste retseptorite suhtes. Hiljuti eristatakse nelja tüüpi retseptoreid:
- D1 paiknevad peamiselt mustas aines ja kõhulahtis (nn nigrostrial piirkond), samuti eelfrontala piirkonnas;
- D2 - nigrostrial, mesolimbis ja anterior hüpofüüsi piirkonnas (prolaktiini sekretsioon);
- D3 (presünaptiline) - aju erinevates struktuurides kontrollib dopaminergilist aktiivsust vastavalt negatiivse tagasiside seadusele;
- D4 (presünaptiline) - peamiselt nigrostrial-ja mesolumbic piirkondades.
Kuid praegusel ajal ei saa pidada kinnitab fakt, et see blokaadi D2-retseptori põhjustab arengut antipsühhootilise, sekundaarsed rahustava toime ja ekstrapüramidaalsete kõrvaltoimete teistes kliinilisi ilminguid blokaadi selle retseptori tüüp on valuvaigistav ja oksendusvastase toime neuroleptikumid (vähendab iiveldust, oksendamist mille tulemusena pärsitakse oksendamise keskel) ja redutseerimine kasvuhormooni ja kasv prolaktiini (neuroendokriinse kõrvaltoimeid, sealhulgas ha laktoomia ja menstruaaltsükli häired). Pikaajaline blokaadi nigrostrialnyh D2-retseptoritega viib nende ülitundlikkus vastutab arengu hilisdüskineesiaid ja "psühhoosid ülitundlikkus." Presünaptiliste D3- ja D4-retseptorite blokaadi tõenäolised kliinilised ilmingud on peamiselt seotud neuroleptikumide stimuleeriva toimega. Tulenevalt osalist blokaadi Nende retseptorite nigrostrialnoy mezolimbokortikalnoy ja aktiveerides domeene ja teravaid (võimsad, kõrgel tasemel) neuroleptikumid väikestes annustes võib stimuleerida ja suurtes annustes pärsivad dopamiinergiliste edastamiseks.
Viimastel aastatel on järsult suurenenud huvi serotoniinergiliste aju süsteemide, sealhulgas serotoniini retseptorite funktsiooni üle. Tegelikult on see, et aju erinevates osades on serotoniinergiline süsteem moduleeriv mõju dopamiinergilistele struktuuridele. Täpsemalt, mesokortikalise piirkonna seas inhibeerib serotoniin dopamiini vabanemist vastavalt postsünaptiliste 5-HT retseptorite blokeerimisega, mis suurendab dopamiini taset. Nagu teada, on skisofreeniaga seotud negatiivsete sümptomite tekkimine seotud ajukoorte prefrontaalsete struktuuridega dopamiini neuronite hüpofunktsiooniga. Praegu on teada umbes 15 tüüpi keskmisi 5-HT retseptoreid. Eksperimentaalselt leiti, et neuroleptikumid seostuvad peamiselt kolme esimese tüübi 5-HT-retseptoritega.
5-HT1a-retseptoritel on need ravimid põhiliselt stimuleeriv (agonistlik) toime. Tõenäolised kliinilised tagajärjed; antipsühhootilise aktiivsuse intensiivistamine, kognitiivsete häirete raskusastme vähenemine, negatiivsete sümptomite korrigeerimine, antidepressantide mõju ja ekstrapüramidaalsete kõrvaltoimete arvu vähenemine.
Olulise tähtsusega on neuroleptikumide toime 5-HT2-retseptoritele, eriti 5-HT2A-alatüüpidele. Neid leidub peamiselt ajukoores ja nende tundlikkus skisofreeniaga patsientidel suureneb. Mugav blokaadi 5-HT2A retseptoriga seondumise võime uue põlvkonna antipsühhootikumide raskuse vähendamiseks negatiivsete sümptomitega parandada kognitiivseid funktsioone reguleerida une suurendades kogukestus aeglase laine (L-wave) unefaasid, et vähendada agressiivsusega ja summutavad depressioonisümptomeid ja migreeni (tekivad sosudisto ajuhäired) peavalud. Seevastu 5-HT2a-retseptorite blokeerimisega võib meestel esineda hüpotensiooniefektide ja ejakulatsiooni häirete suurenemist.
Usutakse, et kokkupuude neuroleptikumid 5-HT2c retseptorite põhjustab sedatsiooni (anksiolüütilist) mõju, söögiisu suurenemine (koos kehakaalu tõusu) ning väheneb prolaktiini.
5-HT3 retseptorid leitakse peamiselt limbilises piirkonnas ja nende blokaadil tekib peamiselt antiemeetiline toime ja see suurendab ka antipsühhootilist ja anksiolüütilist toimet.
Esinemise parkinsonismi sümptomite raviks sõltub ka jõu blokeeriva ravimi koliinergiliste retseptoritega. Holinoliticheskoe ja dofaminblokiruyuschee tegevus teatud määral on vastastikused suhted. On teada, et näiteks valdkonnas nigrostrialnoy D2-retseptorite pärsivad atsetüülkoliini vabanemist. Kui blokaadi üle 75% D2-retseptori nigrostrialnoy valdkonnas tasakaalu häirib kasuks kolinergilise süsteemi. See on põhjus, korrigeerimise mõju neuroleptikumi ekstrapüramidaalnähtude kõrvalmõjud antikolinergilisi ravimeid (asendamine). Kloorprotikseen, klosapiin ja olansapiin omavad kõrget afiinsust muskariini retseptoritega ja on praktiliselt vaba ekstrapüramidaalnähtude kõrvalmõjusid, sest nii ploki kolinergiliste ja dopamiinergiliste retseptorite suhtes. Haloperidooli ja fenotiasiinil piperasiin sarja avaldavad märkimisväärset mõju dopamiini retseptoreid, kuid väga väike mõju koliini. See on tingitud nende võimet indutseerida ekstrapüramidaalnähtude kõrvaltoimeid, mis on vähenenud, kui kasutatakse väga suurtes annustes kui holinoliticheskoe mõju muutub märgatavaks. Lisaks vähendavad dofaminblokiruyuschego toiminguid D2-retseptorite nigrostrialnoy piirkonna ja tasandus ekstrapüramidaalnähtude kõrvaltoimeid, tugeva koliinergilist mõju võib põhjustada halvenemist kognitiivseid funktsioone, sealhulgas mnestic häired ja perifeersed kõrvaltoimeid (keemiline limaskesti, nägemishäired majutust, kõhukinnisus, uriinipeetus, segadust jne). Küllaldaselt tugeva blokeerimine neuroleptikumid avaldavad mõju histamiiniretseptoritega I tüüpi, seostatakse mis eelkõige raskusest sedatsiooni ja kaalutõus tingitud suurenenud söögiisu. Allergiavastaseid ja antipruriitiline efekti antipsühhootikumide seostuda ka nende antihistaminiini omadused.
Lisaks dopamiini blokeerimisele, antiseerotonergilistele, antikolinergilistele ja antikolinergilistele toimetele on enamikul antipsühhootikumide adrenolüütilisi omadusi, st blokeerivad nii kesk- kui ka perifeersed a1-adrenergilised retseptorid. Sellised adrenoblokeerijad nagu kloorpromasiin ja kloorprotikseen omavad tugevat sedatiivset toimet. Lisaks on nende ravimite blokeeriv toime neurovegetatiivsete kõrvaltoimete (arteriaalne hüpotensioon, tahhükardia jne) põhjustaja ja adrenoblokaatorite antihüpertensiivse toime tugevdamine.
Paljude autorite töös on antud andmed üksikute neuroleptikumide seondumisvõime (afiinsuse kohta) mitmesuguste neuroretseptorite tüübiga.
Neurokeemilise profiili järgi võib tüüpiliste ja atüüpiliste antipsühhootikumide seas, mida peamiselt kasutatakse kliinilises praktikas, jaotada tinglikult kuueks rühmaks.
Esimesse rühma kuuluvad selektiivsed blokaatorid D2 ja D4-retseptori (sulpiriidiga, amisudprid haloperidool jt.) Rühmade propenüüllbensamiid ja Butürofenooni derivaadid. Väikestes annustes peamiselt blokaadi tõttu presünaptilistel D4-retseptorid aktiveerivad need dopamiinergiliste närviülekannet ja ergutama (dezingibiruyuschee) meetme suurtes annustes - ploki D2-retseptorite kõikides ajupiirkondades, mis kliiniliselt avaldub väljendunud antipsühhootilise toimega, samuti ekstrapüramidaalnähtude ja endokriinsed (tänu prolactinemia) küljel kahjustused.
Teise rühma kuuluvad kõrgelt D2-retseptori blokaatorid, samuti ravimid blokeerivad nõrgalt või keskmiselt NT2a - 5 ja 5-HT1A retseptoreid (flupentiksool, flufenasiin, zuklopentiksool jt.), St peamiselt fenotiasiini piperasiini derivaadid või nende stereokeemilises struktuuris nende lähedal asuvad tioksanteenid. Nagu esimese grupi ravimite puhul neuroleptikumid on kõigepealt avaldunud antipsühhootilise (teravaid) tegevuse, samuti põhjustada ekstrapüramidaalefekte ja peochnye prolactinemia. Väikestes annustes on neil mõõdukalt aktiveeriv (psühhostimuleeriv) toime.
Kolmas rühm koosneb; mitmevalentsed sedatiivsed neuroleptikumid, mittediferentseeritud enamus neuroretseptoritest. Need ravimid on eristatavalt väljendatakse blokeerivat toimet dopamiini retseptoreid ning indutseerida tugev ja kolinolüütilisi adrenolüütilisest mõjusid. Nendeks Kõige neuroleptikumid rahustavaid peamiselt alifaatsete ja piperidiinderivaatidest fenotiasiini ja nende lähedalt stereokeemiline struktuur tioksanteenide (kloörpromasiin levomepromasiin kloorprotiakseen jt.). Spekter psühhotroopsete aktiivsuse nendest ravimitest on ülekaalus peamiselt väljendunud rahustid primaarse mis arendab sõltumata doosist ja kerged antipsühhootilise toimega. Peale selle rühma ravimite tõttu väljendunud holinoliticheskogo põhjustada kerged või mõõdukad ekstrapüramidaalsete kõrvaltoimete ja neuroendokriinse, kuid põhjustavad sageli arengus ortostaatiline hüpotensioon ja muud autonoomse tekkeks väljendatakse a1-adrenoretseptorite blokaadi.
Neljas grupp hõlmab neuroleptikumid, tasakaalustatud, st võrdselt blokeerides D2 ja 5-HT2A retseptorite (viimane on mõnevõrra) ja mõõdukalt - .. A1-adrenoretseptorite suhtes. See rühm hõlmab esindajad uue põlvkonna atüüpiliste antipsühhootikumide (risperidoon ziprasidoonil, sertindool), millel on erinev keemiline struktuur. Neurokeemiline toimemehhanismi määrab nende selektiivne toime peamiselt mesolimbilist ajupiirkonda ja mesokortikaalne. Koos selge antipsühhootilise toime või puudumine nõrk ekstrapüramidaalsete kõrvaltoimete (kasutamisel terapeutilistes annustes), kerged või mõõdukad, ja mõõdukas prolactinemia adrenolüütilisest omadused (hüpotensiivne reaktsioon), kusjuures see rühm on võimeline parandama neuroleptikumid negatiivsete sümptomite vahendatud stimulatsiooni dopamiinergiliste transmissiooni ajukoore.
Viies rühm koosneb tritsüklilise dibensodiasepiini polüvalentsetele antipsühhootikumidele või selle lähedale (klosapiin, olansapiin ja kvetiapiin). Nagu kolmanda rühma ravimid, blokeerivad nad enamikku neuroretseptoritest mittedefektiivselt. Kuid 5-HT2a retseptorid blokeerivad tugevamini kui D2 ja D4 retseptorid, mis paiknevad eriti nigroosse piirkonnas. See määrab tõese puudumise või nõrga ekstrapüramidaalse toime ning neuroendokriinsetest kõrvaltoimetest, mis on seotud prolaktiini suurema tootmisega, millel on erinev antipsühhootiline toime ja võime vähendada negatiivsete sümptomite raskust. Lisaks sellele on kõigil selle rühma ravimeid esinenud adrenoliitilisi ja antihistamiinseid omadusi, mis määrab sedatiivse ja hüpotensiivse toime. Klosapiinil ja olansapiinil on üsna tugev blokeeriv toime ka muskariiniretseptoritele ja viivad kolinolüütiliste kõrvaltoimete tekkimiseni.
Seega võime blokeerida postsünaptiline dopamiinergiliste retseptorite kompenseeriv suurenenud sünteesi ja dopamiini metabolismi - ainus ühine biokeemiline omadus kõikide neuroleptikumide arutatud nendes rühmades.
Kuues rühmas on siiani ainus ebatüüpiline antipsühhootiline aripiprasool, mis ilmnes suhteliselt hiljuti kodumaisel psühhofarmakoloogilisel turul. See ravim - osaline agonist dopamiini D2-retseptori pealegi toimib funktsionaalse antagonisti giperdofaminergicheskom seisundist ja funktsionaalse agonist gipodofaminergicheskom profiile. Selle aripiprasooli ainulaadne retseptori profiil võimaldab ekstrapüramidaalsete häirete ja hüperprolaktineemia ohu vähendamist selle kasutamisel. Lisaks aripiprasool toimib 5-HT1a retseptorite osalise agonistiga ja samal ajal on see 5-HT2a retseptorite antagonist. Usutakse, et see interaktsioon retseptoritega viib üldiselt tasakaalustatud toimimiseks serotoniini ja dopamiini süsteemid aga toimemehhanismi aripiprasooli võidakse määrata stabiliseerivat dopamiini-serotoniinisüsteemi.
Niisiis võimaldab praegune teadmiste tase neuroleptikumide neurokeemiliste mehhanismide kohta pakkuda ettepanekut selle psühhotroopsete ravimite rühma uue patogeenselt paremini põhjendatud farmakodünaamilise klassifikatsiooni kohta. Selle klassifikatsiooni kasutamine võimaldab suurel määral ennustada antud ravimi psühhotroopse aktiivsuse spektrit, taluvust ja tõenäolisi ravimi koostoimeid. Teisisõnu määravad preparaadi neurokeemilise aktiivsuse omadused suuresti selle kliinilise aktiivsuse tunnused, mis peaks suunama antipsühhootilise ravimi valimist kindlale patsiendile.
Tõhusust tahes globaalse antipsühhootilise mõju neuroleptikumid hinnati niinimetatud samaväärse kloörpromasiin mida arvestati 1. Näiteks, haloperidool, kloorpromasiin samaväärse = 50. See tähendab, et 1 mg psühhoosivastase toime võrreldav haloperidool 50 mg kloorpromasiinile. Põhinedes sellel klassifikatsiooni indeksi väljatöötamine, milles esitatakse jaotamiseks neuroleptikumid, on kõrge (ekvivalentne kloorpromasiinile> 10,0), mõõdukas (vastab kloorpromasiinile = 1,0-10,0) ja madala (ekvivalentne kloorpromasiinile = 1,0) antipsühhootilise aktiivsusega, mida nimetatakse patenditavus. Tüüpilised antipsühhootilised ravimid (esimese põlvkonna antipsühhootikumide) peaaegu pool sajandit, on laialt kasutusel kliinilises farmakoteraapias. Terapeutiliste aktiivsuste spekter sisaldab:
- ülemaailmne psühhoosivastane toime, mis võimaldab diferentseeritult ja diferentseeritult vähendada psühhoosi erinevaid ilminguid:
- esmane rahusti (inhibeeriv) toime - ravimite võime kiiresti peatada psühhomotoorne agitatsioon;
- selektiivne, selektiivne antipsühhootikum, mis väljendub võimes mõjutada individuaalseid sümptomeid: deliirium, hallutsinatsioonid, ajude häireid jne;
- aktiveeriv (disinhibiting, disinhibiting, antiuretne) neurotroopne toime, mis avaldub ekstrapüramidaalsete sümptomite tekkega;
- somatotroopne toime neuroendokriinsete ja vegetatiivsete kõrvaltoimete kujul;
- mis mõjutavad mõne antipsühhootikumi võime põhjustada depressiivseid sümptomeid.
Korduvalt tõestatud ja nevsporima tõhusust esimese põlvkonna antipsühhootikumide psühhootiliste häirete ei ole ainult, vaid ka rikkumise piiri sees psühhiaatria. Seetõttu hoolimata ravi sagedastest kõrvaltoimetest, kui need on välja kirjutatud, kasutatakse neid jätkuvalt meditsiinipraktikas.
atüüpilised antipsühhootilised
Kaasaegsed juhised sisaldavad andmeid teise põlvkonna antipsühhootikumide kasutamise eelistest farmakoteraapias. Termin "atüüpiline" (teise põlvkonna sünonüüm - antipsühhootikumid) on tingimuslik ja kasutab seda peamiselt uue põlvkonna tähistamiseks. Drugs selles rühmas võrreldes tavaliste antipsühhootikumide efektiivsemad parandatakse ka negatiivsed afektiivne ja kognitiivseid häireid koos parema talutavuse ja väiksem risk ekstrapüramidaalsed sümptomid. Mitmete ebatüüpiliste antipsühhootikumide terapeutilise toime terapeutilise toime laadi erinevused, nagu tüüpiliste neuroleptikumide rühmas, seonduvad farmakoloogiliste toimete individuaalse profiiliga.
Psühhofarmakoterapia võimaluste selgitamiseks atüüpilisteks antipsühhootikumideks on soovitav keskenduda Venemaal registreeritud selle grupi ettevalmistustele.
 [29], [30], [31], [32], [33], [34],
[29], [30], [31], [32], [33], [34],
Klosapiin (drenzodiasepiin)
Atüüpiliste antipsühhootikumide rühma esivanem. Toimemehhanism klosapiinist erineb väiksemaid D2-retseptorite blokaadile samaaegselt suure antagonism 5-HT2A, A1, A2-adrenergiliste ja histamiini H1-retseptorite suhtes. Ta on osutunud tõhusaks antipsühhootikumiks resistentsuse suhtes teiste antipsühhootikumidega (reservrühma ravim) ja on näidustatud ka kroonilise maania, psühhootilise agitatsiooni, agressiivsuse raviks. Kodusedel tavapäraselt on klozapiin ette nähtud sedatsiooni saavutamiseks ja psühhootiliste patsientide hüpnoosiks. Tuleb tunnistada, et selline klosapiini kasutamine ei vasta ravile kasutatavate näidustuste peamisele profiilile. Võimalik, et suhtumine sellele psühhoosivastasele kui sekundaarse tähtsusega preparaadile tuleks uuesti läbi vaadata, sest täna on see ainus paranemine, millel on resistentsete patsientide tõhusus.
Erinevalt tüüpilistest neuroleptikumitest ei põhjusta klosapiin olulisi ekstsipramiidi häireid, kuna 02-retseptorite puhul on eespool kirjeldatud madala afiinsusega seotud. Samuti selgus, et seda saab kasutada hilises düstoonias ja raske akatiisia raviks. Pidades silmas ZNS-i arenemise väikest ohtu, võib klosapiini pidada ravimiks patsientidel, kes varem seda tüsistust kandnud.
Sellegipoolest võib klosapiinravi korral tekkida mitmeid tõsiseid kõrvaltoimeid. Kõige ohtlikumad neist (isegi väikeste annuste kasutamisel) on agranulotsütoos, mis esineb 0,5-1,0% patsientidest. Muude oluliste kõrvaltoimete puhul, mis võivad olla seotud ravimi kasutamisega, tuleb märkida unisus, hüpersalivatsioon ja kehakaalu tõus, mis sageli suureneb kloasapiini määramise ajal varasema antipsühhootikumide kasutamisel. Samuti tuleks pöörata tähelepanu tachikardia, arteriaalse hüpotensiooni ja epilepsiahoogude tekkega tekkimise võimalusele. Krampide esinemise tõenäosus sõltub annusest. Nende risk suureneb märkimisväärselt, kui klosapiini annus ületab 600 mg päevas. Krampide tekkimine ei ole vastunäidustuseks ravimi edasisele manustamisele, kuid see nõuab poole annuse vähendamist ja antikonvulsantide, nagu valproehapet, manustamist. Kloasapiinravi kõrvaltoimete ennetamine hõlmab valgevereliste piltide, samuti EKG ja endokriinsete parameetrite hoolikat jälgimist.
Üledooside klosapiin võimalikult depressiooni teadvuse kuni arengut koomat ja kaasnevate sümptomite antikolinergiliseks mõjusid (tahhükardia, deliirium), krambid, hingamise pärssimine, ekstrapüramidaalnähtude sündroomid. Kui annus ületab 2500 mg ravimit, võib tekkida surelik tulemus.
 [35], [36], [37], [38], [39], [40], [41], [42],
[35], [36], [37], [38], [39], [40], [41], [42],
Risperidoon
Bensisoksasooli derivaat, millel on kõrge afiinsus serotoniini ja dopamiini Dj retseptorite suhtes, millel on domineeriv mõju serotoniinisüsteemile. Ravimil on ulatuslikud kasutusnäitajad, sealhulgas leevendamise ägenemine, anti-retsidiivravi, esimese psühhootilise episoodi ravi, skisofreenia negatiivsete sümptomite korrigeerimine. Täheldatud on ravimi võime parandada skisofreeniaga patsientide kognitiivset toimet. On saadud esialgsed andmed, et risperidoon vähendab ka skisofreeniaga patsientidel kaasnevaid afektiivseid sümptomeid ja võib olla bipolaarsete afektiivsete häirete raviks valikuline ravim.
Risperidoonravi kõrvaltoimed, eriti ekstrapüramidaalsed häired, sõltuvad annusest ja esinevad sagedamini annuses üle 6 mg / päevas. Muud kõrvaltoimed on iiveldus, oksendamine, ärevus, unisus, prolaktiinisisalduse suurenemine seerumis. Risperidooni pikaajaline kasutamine võib põhjustada kehakaalu suurenemist ja II tüüpi suhkurtõve tekkimist, kuid vähem tõenäoliselt kui klosapiin, olansapiin.
Üleannustamise, unisuse, epilepsiahoogude, QT intervalli pikenemise ja QRS kompleksi laienemise korral on võimalik arteriaalne hüpotensioon. Kirjeldatud on risperidooni üleannustamise korral letaalse tulemuse juhtumeid.
Vaieldamatu eelis toodet - esinemine vedelikus hetkega (sublingvaalne) vorme, mille kasutamine kiirendab ravimi manustamise kohta patsiendi kehas ning lihtsustab kontrolli oma vastuvõtu. Samuti on ravimi pikaajaline vorm - pulber süstelahuse valmistamiseks intramuskulaarseks süstimiseks (constapperpiperidone mikrosfäärides). Seda on soovitatav skisofreenia patsientide toetavaks raviks, eriti patsientide puhul, kellel puudub vastavus. See on vajalik, et võtta arvesse asjaolu, et saada ravimi vereringesse võtab aega umbes kolm nädalat, nii alguses ravi Constat-risperidooni patsient lisaks vormis suukaudse risperidooni vähemalt 3 nädalat pärast esimest süsti.
Olansapiin
By farmakoloogilise toime sarnaneb Klosapiiniga pleyomorfnym retseptori profiil on märkimisväärne afiinsus serotoniini, muskariini, a1-adrenergiliste, histamiiniretseptoritega. Terapeutiline aktiivsus olansapiini on sarnasusi tõhusust klosapiin ja risperidooni mõju positiivseteks, negatiivseteks ja depressiivsete skisofreeniasümptomeid. Kuid andmed saadi suurema tõhususe olansapiini võrreldes teiste atüüpiliste antipsühhootikumide patsientidel esimese psühhootilise episoodi ja parandus kognitiivse soorituse. Pange tähele, et alguses teraapiat tableti kujul võib ravim dezingibiruyuschego kiiret välimust efekti suurendas agitatsiooni ja ärevus. Seetõttu on näidustatud ravimi süstimisvormi kasutamine krampide ravimisel koos tõsise psühhomotoorse agitatsiooniga.
Olansapiin põhjustab harva ekstrapüramidaalseid häireid või tarduvat düskineesia harva ning kõige sagedasemad kõrvaltoimed on metaboolsed häired ja kehakaalu tõus. Selgus, et patsientidel, kes saavad olansapiini sageli suurenenud kolesterooli taset plasmas lipiidid ja seal on eelsoodumus 2. Tüüpi diabeedi puhul, kuid samasugust tekkimisel võrdse sagedusega ravitud patsientidel olansapiin ja klosapiin. Kuid saadud andmeid, et suurenenud kehamassi korreleerub positiivse vastuse vastuvõtu olansapiini (st toimib tähtsa ennustaja ravim), ning muutub rasvumine - vaid 20-30% patsientidest, kes on kogutud ülekaalu ravi.
Üleannustamise korral on võimalik sedatiivset toimet, toksilist kolinolüütilist toimet, epileptilisi krampe, arteriaalset hüpotensiooni. Praeguseks ei ole veenvaid tõendeid surmaohu hindamiseks ravimi üledoosi korral.
Quetieapin
Vt dibensotiasepiini ühendeid. Selle retseptori profiil on mitmel viisil sarnane klosapiiniga. Kvetiapiini seondumine D2 retseptoritega on madal (vähem kui 50%) ja lühiajaline isegi siis, kui kasutatakse suuri annuseid. Ravim on efektiivne skisofreenia positiivsete, negatiivsete ja üldiste sümptomite raviks. On olemas andmed selle edukaks kasutamiseks nii ravi kõrge resistentsuse korral kui ka patsientide kognitiivse funktsiooni näitajate parandamiseks, mis annab õiguse seda soovitada skisofreenia säilitusravi esimese rea antipsühhootikumina. Lõpuks on kvetiapiinil mõõdukalt antidepressant, aktiveeriv toime. Seepärast on see näidustatud senesto-hüpokondriaalse ringi depressiivsete-pettumuste rünnakute ja häirete ravis.
Kvetiapiini kõrge tümotroopne aktiivsus selgitab, et see on registreeritud depressiivsete häirete leevendamise ja sekundaarse ennetamise vahendina. Maniakaalsete episoodide ravis I ja II tüüpi bipolaarsete häirete ravis kasutatakse kvetiapiini täiendava ainena. Süstevormide puudumine mõnevõrra piirab selle kasutamist ärritava ja agressiivse käitumisega patsientidel.
Quetiapiinil on suhteliselt hea talutavus, praktiliselt ei tekita ekstrapüramidaalseid sündroomi, välja arvatud juhul, kui kasutatakse maksimaalseid annuseid. Kvetiapiin ei põhjusta hüperprolaktineemiat, harvem kui olansapiin ja klosapiin põhjustab kehakaalu suurenemist ja glükoositaluvuse halvenemist.
Ziprasidon
Omab retseptori aktiivsuse ainulaadset profiili. Olles tugev 5HT2a retseptorite ja D2 retseptorite antagonist, on see ka aktiivne serotoniini ja norepinefriini tagasihaarde inhibiitor. Kliinilised uuringud on näidanud ziprasidooni olulist paremust selle toimele psühhootilisele sümptomile ja agressiivsele manifestatsioonile võrreldes haloperidooliga. Samuti saadi andmed ziprasidooni positiivse toime kohta skisofreenia patsientide kognitiivsetele funktsioonidele, samuti kaasuvate afektiivsete sümptomite, sotsiaalse funktsiooni näitajate kohta. Ziprasidoon on tavaliselt hästi talutav ja põhjustab väga harva ekstrapüramidaalseid sündroome, kehakaalu tõusu ja ainevahetushäireid. Sageli on QT-intervalli pikenemine pikem kui 460 ms, nii et seda ravimit saavad patsiendid, enne ravimi määramist on soovitatav teha EKG-uuring ja jälgida ravi jälgimist. Erilist tähelepanu tuleb pöörata samaaegsele ravile (antiarütmikumid), mis võib süvendada QT-intervalli pikenemist ja põhjustada südame rütmihäireid, ventrikulaarset fibrillatsiooni.
Sertindol
Vaadake fenüülindooli derivaate. Sellel on D2-, serotoniini (eriti 5-HT2a retseptorite) ja a1-adrenergiliste retseptoritega võrreldes kõrge funktsionaalne antagonism. Elektrooneurokeemiliste uuringute kohaselt inhibeerib sertindool selektiivselt dopamiini retseptoreid ventraalsete segmentide piirkonnas. See selektiivsus tekitab tõenäoliselt vähese ekstrapüramidaalsete sündroomide ja hüperprolaktineemia riski, kui seda ravimit kasutatakse. Võrdlevate uuringute tulemused on näidanud, et sertindool on antipsühhootilise toimega võrreldes võrreldav haloperidooliga. Ravimil on selgelt väljendunud disinhibeeriv toime negatiivsete ja depressiivsete sümptomitega patsientidele, mis ületab rispolept-i sarnase toime. Samuti on andmeid, mis kinnitavad sertindooli efektiivsust kognitiivse kahjustuse korrigeerimiseks skisofreeniaga patsientidel. Sertindool reeglina patsiendid hästi talutavad, harva põhjustab sedatsiooni ning seepärast soovitatakse seda kasutada asendusravimina kõrvaltoimete ilmnemisel teiste tänapäevaste antipsühhootikumidega ravi ajal.
Tõsistest kõrvaltoimetest täheldati ravimi võimet pikendada Q-T intervalli, mis võib põhjustada südame rütmihäireid. Turustamisjärgsete uuringute analüüsimisel ilmnes, et sertindooli kardioloogiline profiil ei erine teiste põlvkonna antipsühhootikumide omadustest.
Aripiprasool
On võrreldav teiste atüüpiliste ainetega antipsühhootilise toimega, kuid see mõjutab rohkem skisofreenia patsientide kognitiivse funktsiooni parameetreid. Ülaltoodud ravimi D2 retseptorite osalise agonisti ainulaadne farmakoloogiline toime võimaldab ekstrapüramidaalsete sündroomide ja hüperprolaktineemia ohtu, kui seda kasutatakse.
 [43], [44], [45], [46], [47], [48]
[43], [44], [45], [46], [47], [48]
Amisulpride
Need viitavad asendatud bensamiidide klassile. Ravim seondub selektiivselt alamtüübi D2 ja D3-dopamiini retseptoritele puudub afiinsus alatüüpide D1-, D4- ja D5-, samuti serotoniini, histamiini H1 ja adrenergilise a1-kolinoretseptoritega. Kui suurtes annustes blokeerib postsinaptpcheskie D2-retseptoreid. Väikestes annustes selgub dezingibiruyuschy efekti blokaadi tõttu presünaptilistel D2, D3-retseptori ja seetõttu kasutamine on ka efektiivne ravi negatiivsete sümptomite, kuigi see on - mitte Ühendatud D2-retseptori antagonisti ja serotoniini retseptoreid. Mitmed uuringud näitavad selgelt väljendunud antipsühhootilise ravimi aktiivsust suurtes annustes, mis on suurem kui traditsioonilised ravimid.
Antipsühhootilise ravi kõrvaltoimed
Tabelis on toodud atüüpiliste antipsühhootikumide ravi peamised kõrvaltoimed.
|
Ravim |
Extra-püramidaalsed |
Juhtimishäire EKG-s |
Ainevahetushäired (kehakaalu tõus, glükoosi, kolesterooli, triglütseriidide sisalduse tõus veres) |
||
|
Klosapiin |
. |
++ |
++ |
++ - |
|
|
Risperidoon |
++ |
+/- |
++ |
+/- |
|
|
Olansapiin |
+ |
+/- |
+++ |
++ |
+++ |
|
Quetieapin |
+/- |
+ |
+/- |
--- |
|
|
Ziprasidon |
+ |
++ |
+/- |
+/- |
+/- |
|
Sertindol |
++ |
- |
+/- |
- |
|
|
Ariliprasool |
- |
--- |
+/- |
- |
- |
|
Amisulpride |
++ |
+/- |
|||
Märkus: Kõrvaltoimete tõsidus: "+++" - kõrge: "++" - keskmise; "+" - madal; "+/-" - kaheldav; "-" - puudub.
Ekstrapüramidaalsed sündroomid
Erinevalt traditsioonilistest atüüpilistest antipsühhootikumidest on nende üks madalamaid võimeid põhjustada ekstrapüramidaalseid sündroome, mis oli läbimurre skisofreenia farmakoteraapia toetamisel. Kuid tabelist nähtub, et antud seeriatoodete (risperidoon, amisulpride) kasutamisel võivad tekkida sellised sümptomid, mis vajavad erilist tähelepanu nende määramisel.
 [3], [4], [5], [6], [7], [8], [9], [10],
[3], [4], [5], [6], [7], [8], [9], [10],
EKG häired
Kardioloogiliste kõrvaltoimete tekkimise võimalus on tõsiseks probleemiks, kui kasutada mõnda kaasaegset antipsühhootikumit ravi saamiseks. Sellistel juhtudel on see Q-T intervalli pikendamine, mis võib põhjustada arütmiat. Kliinilised häired, eriti Q-T intervalli pikenemine, esinevad kõige sagedamini klosapiini, sertindooli ja ziprasidooni puhul. Üheaegne patoloogia bradükardia kujul, atrioventrikulaarne blokaad, hüpotüreoidism võib kaasa aidata nimetatud komplikatsioonide esinemisele eespool nimetatud ravimite ravis. Praegu on soovitatav EKG jälgimine ligikaudu iga 3 kuu tagant patsientidel, kes saavad atüüpiliste antipsühhootikumidega ravi.
Endokriinsüsteemi häired
Praegu on suurimaks mureks ebatüüpiliste antipsühhootikumide võime põhjustada kaalutõusu. Kehakaal, glükoos, triglütseriidide sisaldus veres võib põhjustada ainevahetushäireid ja II tüüpi suhkurtõve tekkimist. Klosapiini ja olansapiiniravi ajal on vajalik eriti tähelepanelik ja iganädalane biokeemiliste parameetrite jälgimine. Vastavalt J. Geddes et al. (2000), R.V. Jones, PF Buckley (2006), seda tuleb tunnistada soovitatav põhjalikult läbi patsientide enne väljakirjutamist neid teatud antipsühhootilise kaasaegse põlvkonna, kuna on teada, et ainevahetushäiretega on sagedasem patsientidel, kellel oli perekonna ajalugu, ülekaalulisuse, lipiidide spekter ja hüperglükeemia enne ravi. P. V. Jonesi, PF Buckley (2006) välja pakutud seirealgoritm sisaldab mitmeid elemente.
- Anamneesi ja perekondlike tegurite kogumine seoses ainevahetuse häiretega.
- Enne ravi kehakaalu indeksi, EKG, vererõhu ja pulse registreerimine.
- Laboratoorsed andmed (glükoos, lipiidide spekter, kolesterool) enne ravi alustamist.
- Kere massiindeksi, elutähtsate näitajate regulaarsel jälgimisel ravi ajal.
- Laboratoorsete andmete kontroll ravi ajal.
Hüperprolaktineemia ilmnemine antipsühhootikumide ravis on tingitud hüpotalamuse dopamiini retseptorite keskblokatsioonist, mis põhjustab hüpofüüsi eesmise osajärgse prolaktiini vabanemist. Olansapiin, risperidoon ja amisulpride ravitakse kõige sagedasemat hüperprolakteemiat.
Agranulotsütoos
Teine tõsine psühhoosivastase ravi komplikatsioon. Seda võib täheldada koos klosapiiniga ja olansapiiniga. Vastavalt J. Geddes et al. (2000) oli ta diagnoositud esimese 3 kuu jooksul 1-2% -l patsientidest, kes neid ravimeid kasutasid. Sellega seoses soovitame neid ravimeid kasutavatel patsientidel esimesel 18 ravinädalal ja igakuisel seiret järgides teha iganädalast vereanalüüsi. Näidati, et kui ülalmainitud neuroleptikumide annus vähenes, jõudis kliiniline vereanalüüs taas normaalseks. Samal ajal tuleb tunnistada, et praegu puudub selge strateegia patsientide jaoks, kellel esinevad metaboolse häirega seotud kõrvaltoimed. Kõige sagedamini asendab teine atüüpiline antipsühhootikum. Veel üks paljutõotav valdkond peaks olema spetsiaalse parandusteraapia määramine, eriti ravimi bromokriptiini kasutamine hüperprolaktineemia korrigeerimiseks. Ideaalseid tuleks pidada olukorraks, kus selliste häiretega patsiendid ravitakse korrapäraselt interni, eriti endokrinoloogide, kardioloogide ja teiste spetsialistide kaasatusena.
Kokkuvõtteks tuleb märkida, et kohaldatakse vähendatud ülesande algoritme ja jälgimiseks mitte ainult vaimse, füüsilise seisundi, vaid ka patsientide ravimite kasutamise kohta teise põlvkonna on turvalisem kui tüüpiline neuroleptikumid.
Praegu arendatakse mitmeid antipsühhootikume. Järgmise põlvkonna ravimid on tõenäoliselt erinev toimemehhanism (nt on GABA profiil) ja suudab mõjutada erinevate väljendustega skisofreenia, sealhulgas tegelikku puudujääki häired.
Tähelepanu!
Teabe tajumise lihtsustamiseks tõlgendatakse seda juhendit ravimi "Antipsühhootikumid või antipsühhootikumid" kasutamiseks ja esitatakse erilisel kujul ravimite meditsiinilise kasutamise ametlike juhiste alusel. Enne kasutamist lugege otse ravimile lisatud märkust.
Kirjeldus on esitatud informatiivsel eesmärgil ja see ei ole juhend enesehoolduseks. Selle ravimi vajadust, raviskeemi eesmärki, ravimeetodeid ja annust määrab ainult raviarst. Enesehooldus on teie tervisele ohtlik.

