Uued väljaanded
Geneetilise põletikulise haiguse eest vastutav valk tuvastati
Viimati vaadatud: 02.07.2025

Kõik iLive'i sisu vaadatakse meditsiiniliselt läbi või seda kontrollitakse, et tagada võimalikult suur faktiline täpsus.
Meil on ranged allhanke juhised ja link ainult mainekate meediakanalite, akadeemiliste teadusasutuste ja võimaluse korral meditsiiniliselt vastastikuste eksperthinnangutega. Pange tähele, et sulgudes ([1], [2] jne) olevad numbrid on nende uuringute linkideks.
Kui tunnete, et mõni meie sisu on ebatäpne, aegunud või muul viisil küsitav, valige see ja vajutage Ctrl + Enter.
Kölni ülikooli CECADi vananemisuuringute tippkeskuse dr Hirotsugu Oda juhitud teadlaste meeskond on avastanud teatud valgukompleksi rolli immuunsüsteemi düsregulatsiooni teatud vormides. See tulemus võib viia uute ravimeetodite väljatöötamiseni, mille eesmärk on vähendada autoinflatsiooni ja "taastada" selle valgukompleksi geneetilise düsfunktsiooniga patsientide immuunsüsteem.
Uuring pealkirjaga "Inimese SHARPIN-i bialleelne funktsioonikaotus kutsub esile autoinflammatsiooni ja immuunpuudulikkuse" avaldati ajakirjas Nature Immunology.
Lineaarne ubikvitiini assemblerkompleks (LUBAC), mis koosneb valkudest HOIP, HOIL-1 ja SHARPIN, on juba ammu tuntud oma kriitilise rolli poolest immuunhomeostaasi säilitamisel. Varasemad uuringud hiirtega on näidanud SHARPIN-i kaotuse tõsiseid tagajärgi, mis viivad naharakkude liigsest surmast tingitud raske dermatiidini. SHARPIN-i puudulikkuse konkreetsed tervisemõjud inimestel on aga jäänud ebaselgeks.
Uurimisrühm teatas esmakordselt kahest SHARPIN-i puudulikkusega inimesest, kellel esinevad autoinflatsiooni ja immuunpuudulikkuse sümptomid, kuid ootamatult ei ilmne neil dermatoloogilisi probleeme, nagu hiirtel.
Edasisel uurimisel leiti, et neil isikutel on häiritud kanooniline NF-κB vastus, mis on oluline immuunvastuse rada. Neil oli ka suurenenud vastuvõtlikkus kasvaja nekroosifaktori (TNF) superperekonna liikmete poolt esile kutsutud rakusurmale. Ühe SHARPIN-defitsiidiga patsiendi ravi anti-TNF-raviga, mis spetsiifiliselt inhibeerib TNF-i poolt indutseeritud rakusurma, viis autoinflatsiooni täieliku lahenemiseni rakulisel tasandil ja kliinilises pildis.
Uuring näitab, et liigne ja kontrollimatu rakusurm mängib olulist rolli geneetilistes inimese põletikulistes haigustes. Oda meeskond lisas SHARPIN-i puudulikkuse uue liikmena geneetiliste inimese põletikuliste haiguste rühma, mida nad pakuvad välja nimetada "kaasasündinud rakusurma vead".
Kaitse immuunsüsteemi düsregulatsiooni eest Uuring algatati dr Dan Kastneri laboris Ameerika Ühendriikide Riiklikes Tervishoiuinstituutides (NIH). Sealsetel teadlastel oli võimalus jälgida ühte patsienti, kellel esinesid lapsepõlves seletamatud palaviku, artriidi, koliidi ja immuunpuudulikkuse episoodid.
Pärast teadliku nõusoleku saamist viisid nad patsiendil ja tema pereliikmetel läbi eksoomide sekveneerimise ning leidsid, et patsiendil oli SHARPIN-geenis laastav geneetiline variant, mis viis SHARPIN-valgu tuvastamatu tasemeni. Samuti leidsid nad, et patsiendi rakkudel oli nii kultiveeritud rakkudes kui ka patsiendi biopsiates suurenenud kalduvus surra.
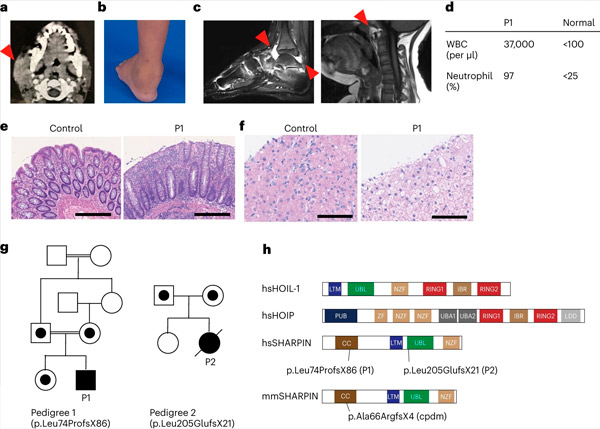
SHARPINi puudulikkus inimestel põhjustab autoinflammatsiooni ja maksa glükogenoosi. Allikas: Nature Immunology (2024). DOI: 10.1038/s41590-024-01817-w
Meeskond leidis ka, et lümfoidsete germinaalsete keskuste – adenoidides leiduvate spetsiifiliste mikrostruktuuride, mis on immuunsüsteemi B-rakkude küpsemise ja seega ka antikehade tootmise seisukohalt kriitilise tähtsusega – areng oli B-rakkude suurenenud surma tõttu oluliselt vähenenud. Need leiud selgitavad patsientide immuunpuudulikkust ja rõhutavad LUBAC-i olulist rolli immuunhomeostaasi säilitamisel inimestel.
„Meie uuring rõhutab LUBACi kriitilist tähtsust immuunsüsteemi düsregulatsiooni eest kaitsmisel. LUBACi puudulikkuse aluseks olevate molekulaarsete mehhanismide selgitamisega sillutame teed uutele ravistrateegiatele, mille eesmärk on taastada immuunsüsteemi homeostaas,“ ütles uuringu juhtiv autor Oda.
Ta lisas: „Üks SHARPIN-i puudulikkusega patsientidest oli aastaid enne meie esimest kohtumist ratastoolis olnud. Tema pahkluud olid põletikulised ja kõndimine oli liiga valus. Geneetiline diagnoos võimaldas meil sihtida tema seisundi aluseks olevat õiget molekulaarset rada.“
Pärast TNF-vastase ravi alustamist on patsient olnud peaaegu seitse aastat sümptomiteta. „Kliiniku ja teadlasena on mul hea meel, et mul on võimalus meie uuringu kaudu ühe patsiendi elu positiivselt mõjutada,“ lõpetas Oda.
