Uued väljaanded
Uued leiud aitavad paremini mõista Rett'i sündroomi põhjuseid
Viimati vaadatud: 02.07.2025

Kõik iLive'i sisu vaadatakse meditsiiniliselt läbi või seda kontrollitakse, et tagada võimalikult suur faktiline täpsus.
Meil on ranged allhanke juhised ja link ainult mainekate meediakanalite, akadeemiliste teadusasutuste ja võimaluse korral meditsiiniliselt vastastikuste eksperthinnangutega. Pange tähele, et sulgudes ([1], [2] jne) olevad numbrid on nende uuringute linkideks.
Kui tunnete, et mõni meie sisu on ebatäpne, aegunud või muul viisil küsitav, valige see ja vajutage Ctrl + Enter.

Retti sündroom on haruldane neuroloogilise arengu häire, millele praegu puudub ravi või hea ravi. See põhjustab raskeid füüsilisi ja kognitiivseid sümptomeid, millest paljud kattuvad autismispektri häiretega.
Retti sündroomi põhjustavad mutatsioonid MECP2 geenis, mis on ajus tugevalt ekspresseeritud ja millel näib olevat oluline roll neuronite tervise säilitamisel. Geen asub X-kromosoomis ja sündroom mõjutab peamiselt tüdrukuid. Retti sündroomi ravimeetodite väljatöötamiseks soovivad teadlased paremini mõista MECP2 geeni ja selle funktsioone ajus.
Teadlased, sealhulgas Whiteheadi Instituudi kaasasutaja Rudolf Jaenisch, on MECP2 geeni uurinud aastakümneid, kuid paljud geeni põhitõed on jäänud teadmata. Geeni kodeeritud valk MECP2 osaleb geeniregulatsioonis; see seondub DNA-ga ja mõjutab mitmete teiste geenide ekspressioonitaset ehk nende toodetava valgu hulka.
Siiski puudus teadlastel täielik nimekiri MECP2 poolt mõjutatud geenidest ja puudus üksmeel selles osas, kuidas MECP2 neid geene mõjutab.
MECP2 varased uuringud näitasid, et see on repressor, mis vähendab oma sihtgeenide ekspressiooni, kuid Jaenischi ja teiste uuringud olid varem näidanud, et MECP2 toimib ka aktivaatorina, suurendades oma sihtgeenide ekspressiooni – ja et see võib olla esiteks aktivaator. Samuti oli teadmata MECP2 toimemehhanism ehk see, kuidas valk täpselt geeniekspressiooni muutusi põhjustab.
Tehnoloogia piirangud on takistanud teadlastel nendele küsimustele selgust saamast. Kuid Yanish, tema labori järeldoktor Yi Liu ja Yanishi endine labori liige Anthony Flamier, kes on nüüd Montréali ülikooli CHU Sainte-Justine'i uurimiskeskuse dotsent, on kasutanud tipptasemel tehnikaid, et vastata neile MECP2 kohta allesjäänud küsimustele ja saada uusi teadmisi selle rollist aju tervises ja haigustes.
Nende tulemused avaldati ajakirjas Neuron ja teadlased lõid ka oma MECP2 andmete veebipõhise hoidla, MECP2-NeuroAtlas portaali, mis on ressurss teistele teadlastele.
„Ma arvan, et see artikkel muudab põhjalikult inimeste arusaama sellest, kuidas MECP2 Retti sündroomi põhjustab. Meil on mehhanismist täiesti uus arusaam ja see võib pakkuda uusi võimalusi haiguse ravimeetodite väljatöötamiseks,“ ütleb Janisch, kes on ka MIT bioloogiaprofessor.
MECP2 sügavam mõistmine ajus
Teadlased lõid esmalt detailse kaardi sellest, kus MECP2 inimese neuronite geenijärjestustes seondub, kas geenide sees või nende lähedal asuvates DNA regulatiivsetes piirkondades. Nad kasutasid meetodit nimega CUT&Tag, mis suudab suure täpsusega kindlaks teha valkude interaktsioone DNA-ga.
Teadlased leidsid MECP2-ga seotud üle 4000 geeni. Nad kordasid oma kaardistamist neuronites, millel esinesid Retti sündroomiga seotud tavalised MECP2 mutatsioonid, et teha kindlaks, kus MECP2 haigusseisundis ammendub.
Teadmine, milliste geenidega MECP2 seondub, võimaldas Liul ja Flamieril hakata looma seoseid MECP2 sihtmärkide ja aju tervise vahel. Nad leidsid, et paljud selle sihtmärgid on seotud neuronaalsete aksonite ja sünapside arengu ja toimimisega.
Samuti võrdlesid nad oma MECP2 sihtmärkide nimekirja Simons Foundation Autism Research Initiative'i (SFARI) autismiga seotud geenide andmebaasiga ja leidsid, et selles andmebaasis on 381 geeni MECP2 sihtmärgid.
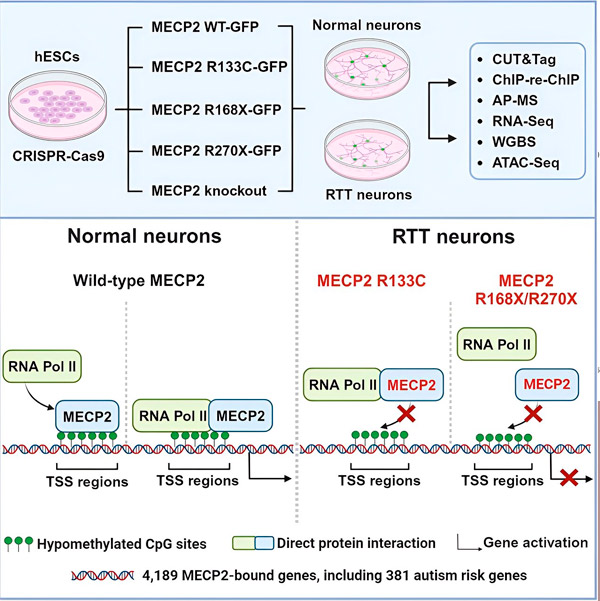
Allikas: Neuron (2024). DOI: 10.1016/j.neuron.2024.04.007
Need leiud võivad aidata selgitada Retti sündroomi autismi sümptomite aluseks olevaid mehhanisme ja pakkuda head lähtepunkti MECP2 võimaliku rolli uurimiseks autismis.
„Oleme loonud MECP2 epigenoomi esimese integreeritud kaardi tervises ja haigustes ning see kaart aitab suunata edasisi uuringuid,“ ütleb Liu. „Teadmine, millised geenid on MECP2 sihtmärgiks ja millised geenid haiguses otseselt häiritud on, annab kindla aluse Retti sündroomi mõistmiseks ja neuronite geeniregulatsiooni kohta küsimuste esitamiseks.“
Samuti uurisid teadlased, kas MECP2 suurendas või vähendas oma sihtgeenide ekspressiooni. Kooskõlas sellega, et MECP2 ajalugu on mõnede poolt identifitseeritud aktivaatorina ja teiste poolt repressorina, leidsid Liu ja Flamier näiteid, kus MECP2 täitis mõlemat rolli.
Kuigi MECP2-d peetakse sagedamini repressoriks, leidsid Liu ja Flamier, et see on enamasti aktivaator – kinnitades Jaenischi ja Liu varasemaid tulemusi. Üks uus katse näitas, et MECP2 aktiveerib vähemalt 80% oma sihtmärkidest ja teine leidis, et see aktiveerib kuni 88% oma sihtmärkidest.
Teadlaste loodud sihtgeenide kaart andis täiendava ülevaate MECP2 rollist aktivaatorina. Nad leidsid, et MECP2 aktiveeritavate geenide puhul seondub see tavaliselt geenist ülesvoolu asuva DNA piirkonnaga, mida nimetatakse transkriptsiooni alguspunktiks.
See on koht, kus raku mehhanism käivitab geeni RNA-ks transkriptsiooni protsessi, mille järel RNA transleeritakse funktsionaalseks valguks, mis on geeniekspressiooni produkt. MECP2 olemasolu transkriptsiooni alguspunktis, kus geeniekspressioon algab, on kooskõlas selle rolliga geeni aktivaatorina.
Seejärel asusid teadlased välja selgitama, millist rolli MECP2 geenide aktiveerimisel mängib. Nad uurisid lisaks DNA-le ka seda, milliste molekulidega MECP2 selles kohas seondub, ja leidsid, et MECP2 interakteerub otseselt valgukompleksiga, mida nimetatakse RNA polümeraas II-ks (RNA Pol II). RNA Pol II on võtmerakuline masin, mis transkribeerib DNA RNA-ks. RNA Pol II ei suuda ise geene leida, seega vajab see oma töö tegemiseks mitmesuguseid kofaktoreid ehk valgukoostööpartnereid.
Teadlased pakuvad välja, et MECP2 toimib ühe sellise kofaktorina, aidates RNA Pol II-l algatada transkriptsiooni geenides, kuhu MECP2 seondub. MECP2 struktuurianalüüs on tuvastanud molekuli osad, mis seonduvad RNA Pol II-ga, ja teised katsed on kinnitanud, et MECP2 kadumine vähendab RNA Pol II esinemist sobivates transkriptsiooni alguskohtades, samuti sihtgeenide ekspressioonitasemeid.
See viitab sellele, et Retti sündroomi võib põhjustada MECP2 sihtgeenide transkriptsiooni vähenemine MECP2 mutatsioonide tõttu, mis takistavad sellel seondumist RNA Pol II-ga või DNA-ga. Selle ideega kooskõlas on kõige levinumad haigustega seotud MECP2 mutatsioonid kärpimised: mutatsioonid, mille puhul osa valgust puudub, mis võib muuta MECP2 ja RNA Pol II vahelist interaktsiooni.
Teadlased loodavad, et nende leiud mitte ainult ei muuda meie arusaama MECP2-st, vaid et sügavam ja laiem arusaam sellest, kuidas MECP2 mõjutab aju arengut ja funktsiooni, võib viia uute teadmisteni, mis aitavad Retti sündroomi ja sellega seotud häiretega, sealhulgas autismiga inimesi.
„See projekt on suurepärane näide Janischi labori koostöövalmidusest,“ ütleb Flamier. „Rudolfil ja minul oli Retti sündroomiga seotud spetsiifiline probleem ja mul oli kogemusi CUT&Tag tehnoloogiaga, mis võiks probleemi lahendada. Arutelu käigus mõistsime, et saame oma jõupingutused ühendada ja nüüd on meil suurepärane teabehoidla MECP2 ja selle seoste kohta haigustega.“
