Uued väljaanded
Tüvirakkude kasvatamine laboris aitab ületada elundite immuunsüsteemi tõrjumist
Viimati vaadatud: 30.06.2025

Kõik iLive'i sisu vaadatakse meditsiiniliselt läbi või seda kontrollitakse, et tagada võimalikult suur faktiline täpsus.
Meil on ranged allhanke juhised ja link ainult mainekate meediakanalite, akadeemiliste teadusasutuste ja võimaluse korral meditsiiniliselt vastastikuste eksperthinnangutega. Pange tähele, et sulgudes ([1], [2] jne) olevad numbrid on nende uuringute linkideks.
Kui tunnete, et mõni meie sisu on ebatäpne, aegunud või muul viisil küsitav, valige see ja vajutage Ctrl + Enter.
Texase Ülikooli Edela Meditsiinikeskuse teadlaste uuring, mille Cell Press äsja ajakirjas Cell Stem Cell avaldas, võib aidata välja töötada paljulubavamaid hematopoeetiliste tüvirakkude siirdamise ravistrateegiaid. Nende rakkude eelkultiveerimine laboris umbes nädala jooksul võib aidata ületada ühe raskeima takistuse eduka siirdamise teel: immuunsüsteemi äratõukereaktsiooni.
Hematopoeetilised tüvirakud (HSC-d) on rakud, mis annavad alust igat tüüpi vererakkude tekkele. Hematopoeetiliste rakkude siirdamist kasutatakse leukeemia, lümfoomi ja teiste vähivormide, samuti autoimmuunhaiguste raviks.
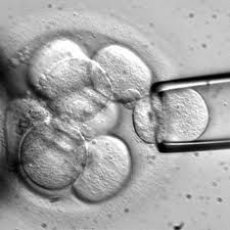
Luuüdi. Valgusmikropilt tüvirakkudest, millest arenevad vererakud. Valged verelibled on suured ja lillad, punased verelibled on kahvatud ning trombotsüüdid on väikesed lillad graanulid. Vererakke toodetakse luuüdis pidevalt, kuna nende eluiga on nii lühike. Punased verelibled, trombotsüüdid ja kõik kolm valgeliblede tüüpi (granulotsüüdid, lümfotsüüdid ja monotsüüdid) pärinevad kõik ühest esivanema rakust, multipotentsest tüvirakust. (Foto: Astrid & Hanns-Frieder Michler/Science Photo Library, P234/0030)
Hematopoeetiliste tüvirakkude ja retsipiendi immuunsüsteemi vastastikmõju puudulik mõistmine raskendab aga oluliselt nii tüvirakkude uurimist kui ka praktilise transplantoloogia arengut. On märkimisväärne oht, et peremeesorganism ei aktsepteeri siiratud rakke, st immuunsüsteem lükkab uued rakud tagasi . Allogeense siirdamise peamiste probleemide hulka kuuluvad doonortransplantaatide madal kohanemismäär ja eluohtliku transplantaadi-peremehe vastu võitlemise haiguse tekkimise kõrge risk. Puhastatud allogeensete HSC-de siirdamine vähendab viimase riski, kuid viib kohanemise vähenemiseni.
Kuigi teadlased teavad mõningaid selliste ebaõnnestumiste põhjuseid, jäävad paljud küsimused vastuseta. „Nende probleemide lahendamine aitab kaasa hematopoeetiliste tüvirakkude ja teiste tüvirakkude immunoloogia mõistmisele ning edendab oluliselt praktilist siirdamist,“ ütles uuringu juht dr Cheng Cheng Zhang.
Dr Zhang ja tema kolleegid on juba näidanud, et inimese ja hiire vereloome tüvirakke (HSC-sid) saab edukalt laboris kasvatada ja seejärel siirdamiseks kasutada. Samal ajal on selliste rakkude pinnal ekspresseeritud paljudes valkudes täheldatud teatud muutusi. Teadlasi huvitas, kas selline „kehaväline kogemus“ võiks muuta ka HSC-de funktsionaalseid omadusi ja muuta need siirdamiseks sobivamaks.
Transplantoloogid on eriti huvitatud kliiniliselt olulistest allogeensetest siirdamistest, mis on siirdamised geneetiliselt erinevate indiviidide, sealhulgas õdede-vendade ja mittesugulusavaldava doonori/retsipientpaaride vahel. Dr Zhangi töörühm siirdas hiirtele nii värskelt isoleeritud kui ka laboris kasvatatud HSC-sid ja leidis, et umbes nädal aega laboris olnud rakud häirisid oluliselt väiksema tõenäosusega retsipiendi immuunsüsteemi. Ex vivo kultiveeritud hiire hematopoeetilised tüvirakud ületasid edukalt peamise koesobivuskompleksi barjääri ja asustasid allogeensete retsipienthiirte luuüdi. Kaheksapäevase kultuuri abil suutsid allotransplantaadid 40-kordselt pookida.
Teadlased otsustasid selle efekti aluseks olevat mehhanismi üksikasjalikumalt uurida ja leidsid, et nii HSC-de arvu suurenemine kui ka kultuuri poolt indutseeritud spetsiifilise immuunsüsteemi inhibiitori CD274 (B7-H1 või PD-L1) ekspressiooni suurenemine rakupinnal aitasid sellele suurenemisele kaasa.
„See töö peaks heitma uut valgust hematopoeetiliste tüvirakkude ja teiste tüvirakkude immunoloogiale ning võib viia uute eduka allogeense siirdamise strateegiate väljatöötamiseni,“ lõpetas dr Zhang. „Võimalus laiendada doonori inimese HSC-sid kultuuris ja siirdada neid inimestele, kes on doonoritest geneetiliselt kaugel, vältides samal ajal transplantaadi-peremehe vastu suunatud haiguse teket, lahendab valdkonna olulise probleemi.“

 [
[