Inimese embrüonaalsete tüvirakkudest kasvatatakse võrkkesta
Viimati vaadatud: 23.04.2024

Kõik iLive'i sisu vaadatakse meditsiiniliselt läbi või seda kontrollitakse, et tagada võimalikult suur faktiline täpsus.
Meil on ranged allhanke juhised ja link ainult mainekate meediakanalite, akadeemiliste teadusasutuste ja võimaluse korral meditsiiniliselt vastastikuste eksperthinnangutega. Pange tähele, et sulgudes ([1], [2] jne) olevad numbrid on nende uuringute linkideks.
Kui tunnete, et mõni meie sisu on ebatäpne, aegunud või muul viisil küsitav, valige see ja vajutage Ctrl + Enter.
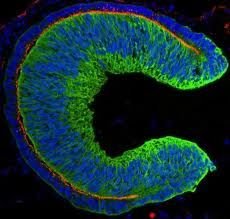
Inimese tüvirakud moodustavad spontaanselt koe, mis areneb võrkkestas - silma kudedesse, mis võimaldab meil näha. Seda on kirjeldatud artiklis ajakirjas Cell Cells. Sellise kolmemõõtmelise kude siirdamine tulevikus võib aidata nägemiskahjustusega patsiente.
"See on oluline verstapost uue arengustaadiumis regeneratiivse meditsiini", - kommenteeris uuringute tulemused peas direktor organogeneesi rühmade ja neurogeneesi professor love Sasai (love Sasai), MD, PhD, Keskus Biology, RIKEN Research Institute (RIKEN Keskus Biology ), Jaapan. "Meie lähenemine avab uued perspektiivid kasutada keerulisi koe pärinevad inimese tüvirakud raviks, samuti meditsiiniliste uuringute seotud patogeneesi ja ravimite väljatöötamine."
Väljatöötamisel on võrkkesta silma sisepinda ümbritsev valgustundlik kude, mis on moodustatud struktuurist, mis on tuntud kui visuaalne või silmaklaas. Jaapani teadlaste uues töös on see struktuur spontaanselt moodustatud inimese embrüonaalsetest tüvirakkudest (hESC) - inimembrüodest pärinevad rakud, millel on potentsiaal eristada erinevatesse kudedesse. See oli võimalik rakulise kasvatamise meetoditega, mida optimeeris professor Sasai ja tema rühm.
HESC-i tuletatud rakud on korrastatud õigesse kolmemõõtmeliseks struktuuriks, kus on kaks silmatippi kihti, millest üks sisaldab suures koguses valgustundlikke rakke - fotoretseptoreid. Kuna võrkkesta degeneratsioon tuleneb peamiselt fotoretseptorite kahjustusest, võib saadud hESC-kude olla ideaalne siirdamiseks mõeldud materjal.
Jaapani teadlaste uurimus avab taas tüvirakkude edasised väljavaated regeneratiivsele meditsiinis, kuid see kahtlemata kiirendab sellise loodusteaduste valdkonna arendamist kui bioloogilist arengut. Katsetuste käigus olid teadlased veendunud, et inimese embrüonaalsete tüvirakkudest moodustatud silmaklaas on palju enam paksem kui hiire embrüonaalsete rakkude puhul. Lisaks sisaldab see nii vardasid kui ka koonuseid, samas kui hiire ESC-des on diferentseerumine koonusteni haruldane. See tähendab, et embrüonaalsel rakul on selle silmade struktuuri loomisel liigi-spetsiifilised juhised.
"Meie uurimus avab võimaluse mõista silma arengu eripära, mis on inimese jaoks spetsiifiline ja mille uuring oli varem võimatu," professor Sasai on kindel.

See ei ole professor Sasai grupi esimene suur edu. Eelmise aasta lõpus on teadlased hiire embrüonaalsetest tüvirakkudest kasvanud hüpofüüsi (adenohüpofüüsi) funktsionaalse eesmise osa, mis koosneb mitmest erinevat tüüpi hormooni tootvate rakkudest. Artikkel selle töö tulemuste kohta. Funktsionaalse adenohüpofüüsi isemoodustamine kolmemõõtmelises kultuuris avaldati ajakirjas Nature.
Hüpofüüsi lõikus on väike sisesekretsioon, mis toodab mitmeid olulisi hormoone. See on eriti tähtis varajase arengu perioodil ja võime imiteerida oma haridust laboris aitab teadlastel paremini mõista embrüogeneesi. Hüpofüüsi häired on seotud kasvuhäiretega nagu gigantism ja nägemishäired, sealhulgas pimedus.
See katse pole võimalik ilma kolmemõõtmelise rakukultuurita. Hüpofüüsi vorm on eraldi elund, kuid selle väljatöötamiseks on vaja keemilisi signaale vahetult selle kohal paiknevast ajualusest - hüpotalamust. Kolmemõõtmelises kultuuris võiksid teadlased üheaegselt kasvatada kahte tüüpi kudesid, mille tulemusena tekitati kahe nädala jooksul hüpofüüsi organiseerunud tüvirakud.
Fluorestsentsvärvimine näitas, et kasvanud hüpofüüsi kude väljendab vastavaid biomarkereid ja sekrete, mis on tüüpilised eesmise hüpofüüsi hormoonide jaoks. Teadlased läksid edasi ja katsetasid nende poolt sünteesitud organite funktsionaalsust, asendades need hiirtega, kellelt oli hüpofüüsi. Eksperimendid lõppesid edukalt: bioengineerunud ajuripatsid taastavad glükokortikoidhormoonide taset loomade veres ja elimineerivad selliseid käitumishäireid nagu letargia. Siirdatud tüvirakkude struktuuridega hiirtel, kellel puudusid vajalikud signaalimaterjalid ja mis seetõttu ei muutunud funktsionaalseks hüpofüüsi, ei paranenud.
Professor Sasai ja tema kolleegid plaanivad inimese tüvirakkude eksperimente korrata ja nende arvates võtab see töö vähemalt kolm aastat.


 [
[