Teadlased on avastanud ajuvähi puhul uue immunosupressiivse mehhanismi
Viimati vaadatud: 14.06.2024

Kõik iLive'i sisu vaadatakse meditsiiniliselt läbi või seda kontrollitakse, et tagada võimalikult suur faktiline täpsus.
Meil on ranged allhanke juhised ja link ainult mainekate meediakanalite, akadeemiliste teadusasutuste ja võimaluse korral meditsiiniliselt vastastikuste eksperthinnangutega. Pange tähele, et sulgudes ([1], [2] jne) olevad numbrid on nende uuringute linkideks.
Kui tunnete, et mõni meie sisu on ebatäpne, aegunud või muul viisil küsitav, valige see ja vajutage Ctrl + Enter.
Dotsent Filippo Veglia, Ph.D., ja tema meeskond Wistari Instituudist on avastanud võtmemehhanismi, mille abil glioblastoom – tõsine ja sageli surmaga lõppev ajuvähk — pärsib immuunsüsteemi, nii et kasvaja saab kasvada ilma organismi kaitsemehhanismide vastupanuta.
Nende avastus avaldati Immunity artiklis "Glükoosist juhitud histooni laktüleerimine soodustab monotsüütist pärinevate makrofaagide immunosupressiivset aktiivsust glioblastoomi korral".
„Meie uuringud näitavad, et vähktõve enesesäilitamise mehhanisme, kui neid piisavalt mõistetakse, saab haiguse vastu väga tõhusalt kasutada,” ütles dr Veglia.
"Ootan huviga tulevasi uuringuid metaboolse immunosupressiooni mehhanismide kohta glioblastoomi korral ja loodan, et jätkame lisateavet selle kohta, kuidas seda vähki paremini mõista ja sellega võidelda."
Siiani on vähe uuritud, kuidas monotsüütidest pärinevad makrofaagid ja mikrogliia loovad glioblastoomi korral immunosupressiivse kasvaja mikrokeskkonna.
Weglia labor uuris glioblastoomi immuunsupressiooni rakulisi mehhanisme ja leidis, et glioblastoomi progresseerumisel hakkavad monotsüütidest pärinevad makrofaagid ületama mikrogliia, mis näitab, et monotsüütidest pärinevate makrofaagide ülekaal kasvaja mikrokeskkonnas on vähile kasulik. Immuunvastuse vältimine.
Tõepoolest, monotsüütidest pärinevad makrofaagid, kuid mitte mikroglia, blokeerisid T-rakkude (kasvajarakke hävitavate immuunrakkude) aktiivsust prekliinilistes mudelites ja patsientidel. Töörühm kinnitas seda, hinnates kunstlikult vähendatud monotsüütidest pärinevate makrofaagide arvu prekliinilisi glioblastoomimudeleid.
Ootuspäraselt näitasid mudelid, mille kasvaja mikrokeskkonnas oli vähem pahaloomulisi makrofaage, standardsete glioblastoomimudelitega võrreldes paremaid tulemusi.
Glioblastoom moodustab veidi üle poole kõigist ajus tekkivatest pahaloomulistest kasvajatest ja selle haigusega diagnoositud patsientide prognoos on äärmiselt halb: ainult 25% patsientidest jääb esimese aasta pärast diagnoosimist ellu. Glioblastoom ei ole ohtlik mitte ainult selle asukoha tõttu ajus, vaid ka immunosupressiivse kasvaja mikrokeskkonna tõttu, mis muudab glioblastoomi resistentseks paljulubavate immunoteraapiate suhtes.
Programmeerides teatud immuunrakud, nagu makrofaagid (monotsüütidest pärinevad makrofaagid ja mikroglia), töötama kasvaja kasuks, mitte selle vastu, loob glioblastoom endale kasvaja mikrokeskkonna, mis võimaldab vähil agressiivselt kasvada, vältides samal ajal vähivastast toimet. Immuunvastused.
Mehhanismi väljaselgitamine
Kinnitanud monotsüütidest pärinevate makrofaagide rolli, püüdis Weglia labor järgmisena mõista, kuidas need vähiga seotud immuunrakud immuunsüsteemi vastu töötavad.
Nad sekveneerisid makrofaage, et teha kindlaks, kas rakkudel on ebanormaalseid geeniekspressiooni mustreid, mis võivad viidata geenidele, mis mängivad rolli immunosupressioonis, ning uurisid ka makrofaagide metaboolseid mustreid, et mõista, kas ebanormaalne geeniekspressioon on seotud ainevahetusega.
Geeni ja ainevahetuse analüüs viisid nad glükoosi metabolismini. Testide seeria näitas, et suurenenud glükoosi metabolismi ja peamise glükoosi transporteri GLUT1 ekspressiooniga monotsüütidest pärinevad makrofaagid blokeerisid T-rakkude funktsiooni, vabastades interleukiin-10 (IL-10).
Tiim näitas, et glioblastoom häirib nendes makrofaagides glükoosi metabolismi, põhjustades nende immunosupressiivset seisundit.
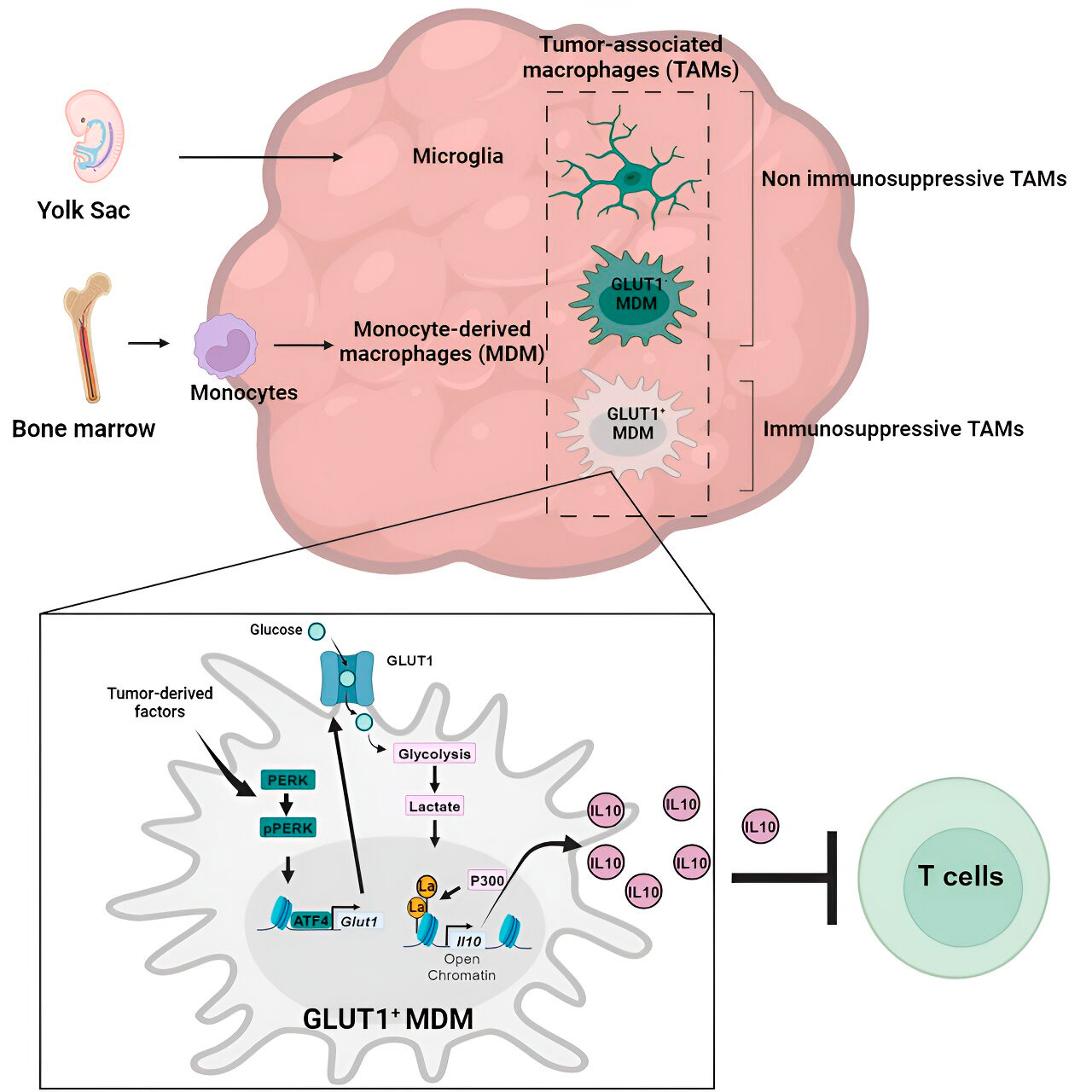
Histooni laktüülimine ja selle roll
Teadlased on avastanud, et glükoosi metabolismiga seotud monotsüütidest pärinevate makrofaagide immunosupressiivse toime võti peitub protsessis, mida nimetatakse "histooni laktüülimiseks". Histoonid on genoomis leiduvad struktuursed valgud, mis mängivad teatud kontekstides võtmerolli selliste geenide nagu IL-10 ekspressioonis.
Monotsüütidest pärinevad makrofaagid toodavad glükoosi kiiresti metaboliseerides laktaati, mis on glükoosi metabolismi kõrvalprodukt. Histoonid võivad "laktüleerida" (st laktaat integreerub histoonidesse), nii et histooni organisatsioon soodustab IL-10 ekspressiooni, mida toodavad monotsüütidest pärinevad makrofaagid vähirakkude kasvu toetamiseks.
Probleemi lahendus
Aga kuidas saate peatada glükoosi metabolismiga seotud monotsüütidest pärinevate makrofaagide immunosupressiivse aktiivsuse? Dr Veglia ja tema meeskond leidsid võimaliku lahenduse: PERK, ensüüm, mille nad tuvastasid glükoosi metabolismi ja GLUT1 ekspressiooni regulaatorina makrofaagides.
Glioblastoomi prekliinilistes mudelites häiris PERK-i sihtimine histooni laktüülimist ja makrofaagide immunosupressiivset aktiivsust ning kombineerituna immunoteraapiaga blokeeris glioblastoomi progresseerumise ja kutsus esile pikaajalise immuunsuse, mis kaitses aju kasvaja taaskasvu eest, mis viitab sellele, et PERK-histooni sihtimine laktülatsioonitelg võib olla elujõuline strateegia selle surmava ajuvähi vastu võitlemiseks.
