Uued väljaanded
Geenide redigeerimine herpese ravimiseks näitab edu laboriuuringutes
Viimati vaadatud: 02.07.2025

Kõik iLive'i sisu vaadatakse meditsiiniliselt läbi või seda kontrollitakse, et tagada võimalikult suur faktiline täpsus.
Meil on ranged allhanke juhised ja link ainult mainekate meediakanalite, akadeemiliste teadusasutuste ja võimaluse korral meditsiiniliselt vastastikuste eksperthinnangutega. Pange tähele, et sulgudes ([1], [2] jne) olevad numbrid on nende uuringute linkideks.
Kui tunnete, et mõni meie sisu on ebatäpne, aegunud või muul viisil küsitav, valige see ja vajutage Ctrl + Enter.
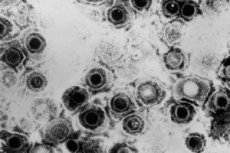
Fred Hutchi vähikeskuse teadlased on prekliinilistes uuringutes leidnud, et genitaal- ja suuherpese eksperimentaalne geeniteraapia elimineerib 90% või rohkem nakkusest ja vähendab viiruse hulka, mida nakatunud inimene suudab levitada. See viitab sellele, et ravi võib vähendada ka viiruse levikut.
„Herpes on väga salakaval. See peidab end närvirakkude vahel ja seejärel taasaktiveerub ning põhjustab valulikke nahaville,“ ütles Keith Jerome, MD, Fred Hutchi vaktsiinide ja nakkushaiguste professor. „Meie eesmärk on ravida inimesi sellest nakkusest, et nad ei elaks pidevas hirmus puhangute või viiruse kellelegi teisele edasiandmise ees.“
Avaldatud 13. mail ajakirjas Nature Communications, Jerome'i ja tema meeskonna uuring Fred Hutchi keskuses kujutab endast julgustavat sammu herpese geeniteraapia suunas.
Eksperimentaalne geeniteraapia hõlmab geene redigeerivate molekulide segu süstimist vereringesse, et leida herpesviiruse asukoht kehas. Segu sisaldab laboris modifitseeritud viiruseid, mida nimetatakse vektoriteks ja mida tavaliselt kasutatakse geeniteraapias, ning ensüüme, mis toimivad molekulaarsete kääridena. Kui vektor jõuab närvikobarateni, kus herpesviirus peidab end, lõikavad molekulaarsed käärid herpesviiruse geene läbi, kahjustades neid või eemaldades viiruse täielikult.
„Me kasutame meganukleaasi ensüümi, mis lõikab herpesviiruse DNA-d kahest erinevast kohast,“ ütles juhtiv autor, Fred Hutchi keskuse teadusjuht, PhD Martine Ober. „Need lõiked kahjustavad viirust nii rängalt, et see ei suuda ennast parandada. Seejärel tunnevad keha enda parandussüsteemid kahjustatud DNA võõrana ära ja vabanevad sellest.“
Hiirte infektsioonimudelite abil elimineeris eksperimentaalne ravi pärast näoinfektsiooni, tuntud ka kui suuõõne herpes, 90% herpes simplex viiruse tüübist 1 (HSV-1) ja pärast suguelundite infektsiooni 97% HSV-1-st. Ravitud hiirtel kulus nende vähenemiste ilmnemiseks umbes kuu aega ja viiruse vähenemine näis aja jooksul täielikumaks muutuvat.
Lisaks leidsid teadlased, et HSV-1 geenteraapia vähendas oluliselt nii viiruse leviku sagedust kui ka hulka.
Fred Hutchi viroloogid Martin Ober (PhD) ja Keith Jerome (MD) viivad läbi laborikatseid herpese ravimiseks mõeldud geeniteraapia väljatöötamiseks. „Kui rääkida herpesega elavate inimestega, siis paljud neist muretsevad, kas nende nakkus levib teistele,“ ütles Jerome. „Meie uus uuring näitab, et saame vähendada nii viiruse hulka organismis kui ka erituva viiruse hulka.“
Fred Hutchi meeskond lihtsustas ka geenitöötlusmeetodit, muutes selle ohutumaks ja lihtsamini toodetavaks. 2020. aasta uuringus kasutasid nad kolme vektorit ja kahte erinevat meganukleaasi. Viimases uuringus kasutatakse ainult ühte vektorit ja ühte meganukleaasi, mis suudavad viiruse DNA-d kahest kohast lõigata.
„Meie lihtsustatud geenitöötlusmeetod on herpesviiruse elimineerimisel efektiivne ning sellel on vähem kõrvaltoimeid maksale ja närvidele,“ ütles Jerome. „See viitab sellele, et teraapia on inimestele ohutum ja seda on lihtsam toota, kuna see sisaldab vähem komponente.“
Kuigi Fred Hutchi teadlased on julgustatud sellest, kui hästi geeniteraapia loommudelites toimib, ja soovivad oma tulemusi inimeste ravis rakendada, on nad samal ajal ettevaatlikud kliinilisteks uuringuteks ettevalmistamiseks vajalike sammude suhtes. Nad märkisid ka, et kuigi praegune uuring käsitles HSV-1 infektsioone, töötavad nad selle nimel, et kohandada geenitöötlustehnoloogiat HSV-2 infektsioonide sihtimiseks.
„Teeme kliiniliste uuringute suunas liikumisel koostööd paljude partneritega, et täita föderaalseid regulatiivseid nõudeid geeniteraapia ohutuse ja efektiivsuse tagamiseks,“ ütles Jerome. „Hindame sügavalt herpese ravimise pooldajate toetust, kes jagavad meie nägemust selle nakkuse ravimisest.“
Herpes simplex viirus (HSV) on levinud infektsioon, mis pärast nakatumist püsib kogu elu. Praegused ravimeetodid suudavad ainult sümptomeid, sealhulgas valulikke villid, maha suruda, kuid mitte neid täielikult kõrvaldada. Maailma Terviseorganisatsiooni andmetel on umbes 3,7 miljardil alla 50-aastasel inimesel (67%) HSV-1, mis põhjustab suuherpest. Umbes 491 miljonil inimesel vanuses 15–49 (13%) kogu maailmas on HSV-2, mis põhjustab genitaalherpest.
Herpes võib inimestel põhjustada ka teisi terviseprobleeme. HSV-2 suurendab HIV-nakkuse riski. Teised uuringud on seostanud dementsust HSV-1-ga.
