Uued väljaanded
Uued geneetilised mehhanismid võivad olla terapeutiline sihtmärk glioomi vastu
Viimati vaadatud: 02.07.2025

Kõik iLive'i sisu vaadatakse meditsiiniliselt läbi või seda kontrollitakse, et tagada võimalikult suur faktiline täpsus.
Meil on ranged allhanke juhised ja link ainult mainekate meediakanalite, akadeemiliste teadusasutuste ja võimaluse korral meditsiiniliselt vastastikuste eksperthinnangutega. Pange tähele, et sulgudes ([1], [2] jne) olevad numbrid on nende uuringute linkideks.
Kui tunnete, et mõni meie sisu on ebatäpne, aegunud või muul viisil küsitav, valige see ja vajutage Ctrl + Enter.
Neuroloogia osakonna neuroonkoloogia osakonna Ken ja Ruth Davey professori Shi-Yuan Chengi laboris läbi viidud uuring on tuvastanud uued mehhanismid, mis on aluseks alternatiivse RNA splaissingu sündmustele glioomi kasvajarakkudes ja mis võivad olla uued terapeutilised sihtmärgid. Uuringu tulemused avaldati ajakirjas Journal of Clinical Investigation.
„Oleme leidnud teistsuguse viisi glioomi raviks alternatiivse splaissingu läätse kaudu ja avastanud uusi sihtmärke, mida pole varem tuvastatud, kuid mis on glioomi pahaloomulisuse seisukohalt olulised,“ ütles Xiao Song, MD, PhD, neuroloogia dotsent ja uuringu juhtiv autor.
Glioom on täiskasvanutel kõige levinum primaarne ajukasvaja tüüp ning pärineb gliaalrakkudest, mis asuvad kesknärvisüsteemis ja toetavad naaberneuroneid. Glioom on standardsete ravimeetodite, sealhulgas kiiritusravi ja keemiaravi suhtes väga resistentne kasvaja geneetilise ja epigeneetilise heterogeensuse tõttu, mis rõhutab vajadust leida uusi terapeutilisi sihtmärke.
Chengi labori varasem uuring, mis avaldati ajakirjas Cancer Research, näitas, et oluline splaissingu faktor SRSF3 on glioomides võrreldes normaalsete ajudega oluliselt kõrgem ning SRSF3-reguleeritud RNA splaissingu soodustab glioomi kasvu ja progresseerumist, mõjutades kasvajarakkudes mitmeid rakulisi protsesse.
RNA splaissimine on protsess, mis hõlmab intronite (RNA mittekodeerivate piirkondade) eemaldamist ja eksonite (kodeerivate piirkondade) ühendamist, et moodustada küps mRNA molekul, mis toetab geeniekspressiooni rakus.
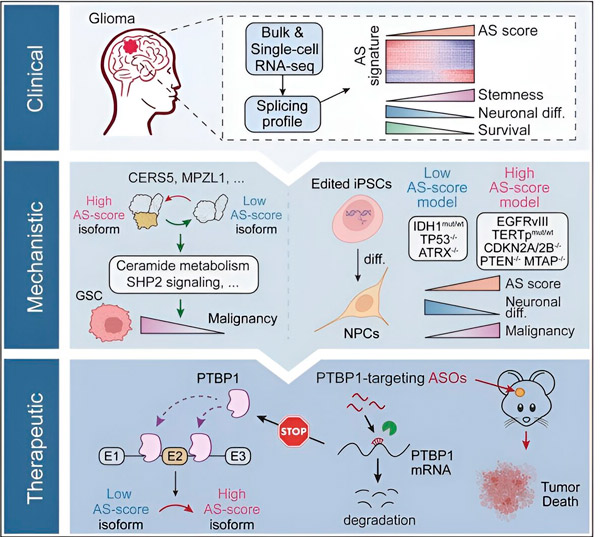
Käesolevas uuringus püüdsid teadlased tuvastada glioomi kasvajarakkude alternatiivse splaissingu muutusi, nende muutuste aluseks olevaid mehhanisme ja määrata nende potentsiaali terapeutiliste sihtmärkidena.
Arvutusmeetodeid ja RNA sekveneerimise tehnoloogiaid kasutades uurisid teadlased patsientide proovides võetud glioomi kasvajarakkude splaissingu muutusi. Nende muutuste kinnitamiseks kasutasid nad CRISPR geeni redigeerimise tehnoloogiaid, et viia inimese indutseeritud pluripotentsetest tüvirakkudest (iPSC-dest) saadud glioomimudelitesse erinevaid glioomi juhtmutatsioone.
Nad leidsid, et neid splaissingu muutusi võimendab epidermaalse kasvufaktori retseptori III (EGFRIII) variant, mis teadaolevalt on paljudes kasvajates, sealhulgas glioomides, üleekspresseeritud ja mida pärsib IDH1 geeni mutatsioon.
Teadlased on kinnitanud kahe RNA splaissingu sündmuse funktsiooni, mis loovad erinevaid valguisovorme erinevate aminohappejärjestustega.
"Ainult üks neist isovormidest võib soodustada kasvaja kasvu, erinevalt teisest isovormist, mida tavaliselt ekspresseeritakse normaalses ajus. Kasvajad kasutavad seda mehhanismi ära, et selektiivselt ekspresseerida kasvajat soodustavat isovormi normaalse aju isovormi kohal," ütles Song.
Seejärel analüüsis meeskond RNA-d siduvaid valke ja leidis, et PTBP1 geen reguleerib glioomirakkudes kasvajat soodustavat RNA splaissingut. Immuunpuudulikkusega hiirtel ortotoopilise glioomi mudeli abil sihtisid teadlased PTBP1-d antisenss-oligonukleotiididel (ASO) põhineva raviga, mis lõppkokkuvõttes pärssis kasvaja kasvu.
„Meie andmed toovad esile alternatiivse RNA splaissingu rolli glioomi pahaloomulisuse ja heterogeensuse mõjutamisel ning selle potentsiaali terapeutilise haavatavusena täiskasvanute glioomide ravis,“ kirjutasid uuringu autorid.
Teadlaste järgmine samm on uurida PTBP1 sihtimise potentsiaali kasvajavastase immuunvastuse esilekutsumiseks, ütles Song.
"Pikaajalise RNA sekveneerimise analüüsi abil leidsime, et PTBP1 sihtimine glioomirakkudes toob kaasa mitmete alternatiivselt splaissitud transkriptide tootmise, mis normaalsetes kudedes puuduvad. Seega on meie järgmine projekt välja selgitada, kas see isovorm suudab genereerida antigeene, et immuunsüsteem saaks kasvajat paremini ära tunda," ütles Song.
Song lisas ka, et nende meeskond on huvitatud glioomipatsientide mittekasvajarakkude, näiteks immuunrakkude, splaissingu muutuste analüüsimisest.
„Me juba teame, et splaissimine on raku funktsiooni reguleerimiseks väga oluline, seega ei tohiks see reguleerida mitte ainult kasvaja pahaloomulisust, vaid see võib reguleerida ka immuunrakkude funktsiooni, et teha kindlaks, kas need suudavad vähki tõhusalt hävitada. Seega teeme ka mõningaid bioinformaatilisi analüüse kasvajasse infiltreerunud immuunrakkudes, et näha, kas splaissimises on toimunud muutusi pärast seda, kui immuunrakk on kasvajasse infiltreerunud.“
"Meie eesmärk on määrata alternatiivse splaissingu rolli immuunsupressiivse kasvaja mikrokeskkonna kujundamisel ja tuvastada potentsiaalsed sihtmärgid immunoteraapiate efektiivsuse parandamiseks glioomi korral," ütles Song.
