Artikli meditsiiniline ekspert
Uued väljaanded
Äge hematogeenne osteomüeliit
Viimati vaadatud: 29.06.2025

Kõik iLive'i sisu vaadatakse meditsiiniliselt läbi või seda kontrollitakse, et tagada võimalikult suur faktiline täpsus.
Meil on ranged allhanke juhised ja link ainult mainekate meediakanalite, akadeemiliste teadusasutuste ja võimaluse korral meditsiiniliselt vastastikuste eksperthinnangutega. Pange tähele, et sulgudes ([1], [2] jne) olevad numbrid on nende uuringute linkideks.
Kui tunnete, et mõni meie sisu on ebatäpne, aegunud või muul viisil küsitav, valige see ja vajutage Ctrl + Enter.
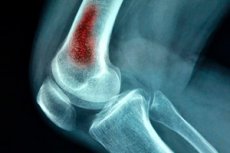
Üks eluohtlikumaid kirurgilise infektsiooni variante on äge hematogeenne osteomüeliit. See patoloogia esineb peamiselt lastel, kuigi ka täiskasvanud võivad haigestuda traumaatiliste vigastuste (kuulihaavad, operatsioonijärgsed tüsistused jne) tagajärjel. Patoloogia on mädane luusisene protsess, mille põhjustab nakkustekitaja sattumine vereringesse. [ 1 ]
Epidemioloogia
Mädase hematogeense osteomüeliidi korral toimub luus mädane põletikuline protsess. See hõlmab medullaarseid struktuure, luuümbrist ja kompaktset luukude. Mõnikord on haigus tingitud mädase reaktsiooni levikust luukoesse lähedalasuvatest organitest ja kudedest. Selline areng on iseloomulik hambakaariesest põhjustatud odontogeensele osteomüeliidile, pleura empüemiga seotud ribide osteomüeliidile, panariitsiumist põhjustatud falangi osteomüeliidile jne.
Enamikul juhtudel on põhjustajaks Staphylococcus aureus või selle kombinatsioonid teiste patogeenidega - eriti Proteuse või Pseudomonas bacillusega.
Ägedat hematogeenset osteomüeliiti peetakse valdavalt laste patoloogiaks. Peamine patsientide osakaal (üle 95%) on eelkooliealised ja algkooliealised lapsed. Selle selektiivsuse põhjus on lihtne ja seotud luu troofilisuse ja struktuuri vanusega seotud anatoomiliste iseärasustega, nimelt:
- Veresoonkonna võrgustiku tugev areng;
- Epifüüsi, metafüüsi ja diafüüsi verevarustuse autonoomia;
- Suur hulk väikeseid veresoonte hargnemisi, mis kulgevad mööda radiaalset rada läbi epifüüsi kõhre luustumistuumani.
Metafüüsi vereringevõrgustik moodustub üle 2-aastastel lastel ja kuni selle ajani on domineeriv epifüüsivõrgustik. Need võrgustikud eksisteerivad üksteisest eraldi, kuid on ühendatud anastomooside abil. Ühise veresoonte süsteemi moodustumine toimub epifüüsi kasvupiirkonna luustumisel. 2-3-aastastel patsientidel on mõjutatud metaepifüüsi piirkonnad, vanemas eas aga peamiselt diafüüsi.
Ägedat hematogeenset osteomüeliiti diagnoositakse sagedamini 7–15-aastastel lastel, poistel – kolm korda sagedamini kui tüdrukutel. Ka täiskasvanu võib haigestuda, kuid see on palju harvem.
Patoloogia teke vastsündinutel on sageli seotud nabanööri haava infektsiooniga. [ 2 ]
Põhjused äge hematogeenne osteomüeliit
Sellise tõsise patoloogia nagu äge hematogeenne osteomüeliit tekke tavaliseks põhjuseks on patogeenide tungimine luuüdisse, mis põhjustab mädase reaktsiooni teket. Nakkuskoldeks, millest patogeenid levivad vereringe kaudu ja satuvad luudesse, võivad olla keskkõrvapõletik, tonsilliit (mädane tonsilliit), furunkuloos, mädased haavad. Ja patoloogia ei teki kohe pärast esmast nakatumist: see võib võtta kuid ja isegi aastaid.
Ägeda hematogeense osteomüeliidi peamine tekitaja on Staphylococcus aureus: seda leidub umbes kaheksal patsiendil kümnest. Mõnel juhul on tegemist kombineeritud infektsiooniga, sealhulgas Proteuse ja Synegnaeuse batsillid.
Põletikulise protsessi intensiivsus on suuresti seotud luustruktuuri iseärasustega. Põletikuline reaktsioon areneb luuüdi struktuuris, mida ümbritseb tihedamate kortikaalsete seintega jäik keskkond. Sellistel asjaoludel puudub võimalus koerõhu vähendamiseks põletikulise piirkonna laiendamise teel, mistõttu levib reaktsioon veresoonte võrgustiku ja Haversia kanalite kaudu ohjeldamatult primaarse tsooni piiridest väljapoole.
Patoloogilise fookuse tekkimise hetkest alates võib osteomüeliiti pidada potentsiaalselt septiliseks protsessiks, mis hõlmab presepsist ja sepsist. [ 3 ]
Riskitegurid
Valdav enamus ägeda hematogeense osteomüeliidi juhtudest esineb lastel ja noorukitel ning üldiselt nõrga immuunsüsteemiga patsientidel. Riskirühmadesse kuuluvad järgmised kategooriad:
- Eelkooliealised ja algkooliealised lapsed;
- Eakad inimesed (üle kuuekümne aasta vanad);
- Kaasasündinud või omandatud immuunpuudulikkusega patsiendid;
- Septiliste seisunditega patsiendid;
- Vähihaiged;
- Krooniliste nakkus-põletikuliste patoloogiate all kannatavad patsiendid.
Provotseerivateks teguriteks võib liigitada kõik sisemised bakteriaalse invasiooni allikad. Nendeks võivad olla hambakaaries, tonsilliit (eriti mädane), uinumata põletikukolded, aga ka mitmesugused eelhaigused. Olulist rolli mängivad organismi allergiline eelsoodumus, immuunsuse langus mitme profülaktilise vaktsiini samaaegse manustamise tagajärjel, samuti trauma, hüpotermia ja stressirohked olukorrad. [ 4 ]
Pathogenesis
Ägeda hematogeense osteomüeliidi tekke patogeneetilist mehhanismi pole seni piisavalt uuritud. Arvatavasti on patogeneesi põhitegurid järgmised:
- Nakkustekitaja olemasolu organismis;
- Individuaalne luu anatoomia;
- Raske immuunpuudulikkus.
Ägeda hematogeense osteomüeliidi põletikulise reaktsiooni tunnuseks on selle kinnistumine luu kõvasse torusse, mis toob kaasa veresoonte võrgustiku tugeva kokkusurumise. Valusündroom tekib suurenenud rõhu tagajärjel luumedullaarses ruumis. Hüpertensiooni näitaja võib olla kuni 300–500 mm Hg (terve lapse norm on 60–100 mm Hg).
Kui patoloogiat ei avastata luuüdi kanali põletikulise protsessi staadiumis, siis neljandal või viiendal päeval pärast osteomüeliidi algust hakkavad mädased massid levima Haversi ja Volkmanni süsteemi kaudu periosteumi, mille tagajärjel see järk-järgult delamineerub.
Kaheksandal või kümnendal päeval jätkavad mädased massid koos lagunemisproduktidega luuümbrise kihistumist, mille järel toimub mäda läbimurre pehmete kudede struktuuridesse. See viib lihastevaheliste ja nahaaluste flegmoni tekkeni. Seda olukorda peetakse tähelepanuta jäetud haiguseks: hilja diagnoositud ägeda hematogeense osteomüeliidi ravi on keeruline ja pikk.
Valusündroom vaibub enamasti subperiostaalse abstsessi spontaanse läbimurde taustal lähedalasuvatesse struktuuridesse, millega kaasneb rõhu järsk langus medullaarses ruumis. [ 5 ]
Sümptomid äge hematogeenne osteomüeliit
Sümptomatoloogia sõltub teatud määral patoloogilise protsessi vormist, mis võib olla lokaliseeritud ja üldistatud.
Lokaliseeritud vormis on valu tugev, paisuv ja koondunud kahjustatud luu piirkonda. Jäseme puudutamine või koputamine põhjustab äärmiselt ebameeldivaid aistinguid, motoorne aktiivsus on järsult piiratud, nahk põletikupiirkonna kohal on kuum, punetav, sageli paistes.
Üldistatud vormis kombineeritakse lokaalseid ilminguid üldistega. Joobeseisundi tunnused süvenevad, palavik tõuseb, tekivad külmavärinad ja liigne higistamine. Mädaste fookuste edasise levikuga halveneb olukord märkimisväärselt. Võimalikud on mitmed luukahjustused, mädase perikardiidi või mädase destruktiivse kopsupõletiku teke.
Ägeda hematogeense osteomüeliidi lokaalse kulgemise korral domineerivad lokaalsed tunnused, kuid mitte ainsad: joobe sümptomid esinevad igal juhul. Patsiendi küsitlemisel esinevad tingimata kaebused ebarahuldava üldseisundi, külmavärinate ja palaviku kohta. Väliselt pööratakse tähelepanu naha tursele, kahvatusele või punetusele, nähtavale veresoonkonnale. Palpatsioonil tuvastatakse kasvav valulik piirkond, löökpillide proovimisel muutub valu eriti tugevaks. [ 6 ]
Esimesed märgid
Äge hematogeenne osteomüeliit algab äkki, sageli pärast traumat (isegi väikest) või mõnda muud provotseerivat tegurit (nt hüpotermia).
Patoloogia peamine ja püsiv tunnus on luuvalu, mis levib valutavast kuni eriti intensiivseni. Valu takistab inimesel magamast, teeb ta ärrituvaks ja närviliseks. Reeglina levivad äärmiselt ebameeldivad aistingud kogu kahjustatud jäsemesse, kuid valu fookust saab sageli eksimatult tuvastada. Selline valusündroom on tingitud luusisese rõhu suurenemisest luus kasvava põletikulise protsessi taustal. On tähelepanuväärne, et luuvalu iseloomustab püsivus.
Järgmine peamine ägeda osteomüeliidi tunnus on kõrge temperatuur. Esialgses patoloogilises staadiumis võivad indikaatorid olla vahemikus 37-38 °C, kuid generaliseerunud osteomüeliidi tekkega tõuseb temperatuur järsult ja ühtlaselt 39-41 °C-ni, mõnikord kaasneb sellega palavik. Samaaegselt generaliseerunud hüpertermiaga toimub kahjustuse piirkonnas lokaalne temperatuuri tõus.
Haiguse kolmas esialgne tunnus on kahjustatud jäseme funktsionaalne häire. Patsient hakkab lonkama, motoorne aktiivsus on järsult piiratud kuni täieliku võimatuseni. Isegi kahjustatud jäseme kerge liigutamine põhjustab tugevat valu, mis sunnib inimest leidma sundasendi maksimaalse võimaliku lihaslõdvestusega. Eelkõige puusaliigese kahjustuse korral eelistab patsient jalga painutada nii puusa- kui ka põlveliigestes: jäse on kergelt väljapoole pööratud. Kui see asend püsib pikka aega, võib tekkida painutusliigese kontraktuur.
Seejärel, umbes 48–96 tundi pärast ägeda osteomüeliidi algust, kahjustatud jäseme tursub. Aja jooksul levib turse teistesse kudedesse. Patoloogilise fookuse kohal olev nahk muutub pingeliseks ja tihedaks. See mõjutab oluliselt üldist heaolu. Patoloogia raske kulg võib kaasneda haigusprotsessi levikuga teistesse luudesse.
Ägeda hematogeense osteomüeliidi lokaalsed sümptomid
Äge hematogeenne osteomüeliit algab järsu temperatuuri tõusuga. Samaaegselt ilmneb patoloogilise fookuse piirkonnas valu. Haigestunud jäse kaotab liikumisvõime, patsient püüab sellele sundasendi anda. Piiratud ala paisub, nahk omandab pastoosi, palpeerimisel täheldatakse lokaalset temperatuuri tõusu. Lühikese aja jooksul muutub paistes piirkond punaseks, täheldatakse temperatuuri kõikumist.
Mikroosteoperforatsioon kinnitab luusisese rõhu tõusu, mis võimaldab diagnoosi panna isegi mädaste masside puudumisel luuüdiõõnes või luuümbrise all. Mõnes olukorras on asjakohane teha diagnostiline luupunktsioon koos saadud materjali edasise tsütoloogiaga.
Vereanalüüsides ilmneb leukotsütoos ja valemi nihkumine vasakule, samuti toksiline neutrofiilide granulaarsus. Erütrotsüütide settereaktsiooni kiirus on oluliselt suurenenud ja see tõus on stabiilne. Samuti on muutunud vere valguspekter: esineb düsproteineemia, suurenenud globuliinifraktsioonid, hüpoalbumineemia. Pikaajalise osteomüeliidiga kaasneb tserebrospinaalse toksilise depressiooniga seotud aneemia.
Valu iseloom ägeda hematogeense osteomüeliidi korral
Valu ägeda hematogeense osteomüeliidi korral:
- Tugev;
- Paisuv;
- Tugevneb palpatsiooni ja patoloogilise piirkonna koputamise teel;
- Mõne aja pärast muutuvad need äärmiselt teravaks, talumatuks, ärrituvus tekib väikseimagi liigutuse korral kohe.
Tugeva valu tõttu võtab patsient sundasendi, ta ei saa süüa ega magada, muutub ärrituvaks. Kui abi ei osutata, on võimalik vaimne segadus, deliirium ja hallutsinatsioonid.
Klassifikatsioon
Sõltuvalt haiguse käigust eristatakse ägedat ja kroonilist osteomüeliiti.
Patoloogia arengu mehhanism kajastub ka klassifikatsioonis:
- Endogeenne osteomüeliit (hematogeenne);
- Eksogeenne (trauma, kirurgilise sekkumise, laskehaava jne tagajärjel);
- Neurogeenne (kontaktkompressioon).
Sõltuvalt kliinilisest staadiumist eristatakse:
- Äge osteomüeliit (kestab kuni 14-21 päeva);
- Subakuutne (kuni 22–28 päeva);
- Krooniline (üle 28 päeva).
Haiguse atüüpilisi vorme esindavad Brody abstsess, Ollieri albumiinne osteomüeliit ja Garre'i skleroseeriv osteomüeliit.
Kliinilise pildi kohaselt läbib äge hematogeenne osteomüeliit järgmisi etappe:
- Patsiendi heaolu halveneb, isutus kaob, tekib seletamatu apaatia.
- Esineb unetus, palavik, võimalikud düspepsia nähtused.
- Umbes 24 tunni pärast tõuseb temperatuur kõrgele (umbes 39 °C).
- Mürgistus süveneb, nahk muutub kahvatuks kuni sinakaks. Valu on väljendunud, terav, aktiivsed liigutused puuduvad, passiivsed liigutused on tugevalt piiratud.
Kui patoloogiline fookus puruneb, muutub nahk hüpereemiliseks, patsiendi seisund paraneb mõnevõrra. Võimalik on mitmete luukollete moodustumine - umbes 1-2 nädalat pärast esmase fookuse ilmnemist.
Vormid
Ägeda mädase hematogeense osteomüeliidi patoloogilise fookuse lokaliseerimispiirkonna järgi on tegemist epifüüsi, metafüüsi ja diafüüsiga, kusjuures kahjustused esinevad käsnjate, lamedate ja lühikeste luudega. Patoloogilise protsessi sümptomatoloogia ja ravi iseärasused sõltuvad nii patsiendi vanusest ja üldisest tervislikust seisundist kui ka põletikutsooni asukohast. Pikkade toruluude metafüüsid ja diafüüsid on mõjutatud peamiselt eelkoolieas ja algkoolieas. Patoloogia pilt on mitmetahuline ja tihedalt seotud selliste teguritega nagu patogeense mikroorganismi immuunsus ja virulentsus.
Ägeda hematogeense osteomüeliidi lokaalne vorm ei ole "puhas", kuna see ühendab nii lokaalseid kui ka üldiseid ilminguid, kuigi lokaalsed tunnused on mõnevõrra domineerivad. Luu piirkonnas on ere krigisev valu, mis juhib tähelepanu intensiivsele tursele (nahk on paistes, pinges). Koputamisel näitab patsient selget valureaktsiooni. Lokaalse vormi korral võib motoorne võimekus mõnda aega säilida.
Patoloogia mõjutab peamiselt pikki torukujulisi luid. Lamedaid ja lühikesi luid on palju harvemini kahjustatud. Enamasti on kahjustatud luud:
- Reieluu (kuni 40% juhtudest);
- Sääreluu (umbes 30% juhtudest);
- Õlavarreluu (umbes 10%).
Palju harvemini esineb probleem jala, vaagna ja ülemise lõualuu luudes.
Pikkade toruluude ägedal hematogeensel osteomüeliidil on erinev levik. Seega võime rääkida järgmistest haiguse variantidest:
- Metadiafüüsi äge hematogeenne osteomüeliit - mõjutab metafüüsi ja enam kui 50% diafüüsist;
- Metaepifüüsi äge hematogeenne osteomüeliit - mõjutab metafüüsi ja suuremat osa epifüüsist;
- Metafüüsi osteomüeliit - ulatub epifüüsi või diafüüsi servani;
- Totaalne osteomüeliit – mõjutab diafüüsi ja mõlemat metafüüsi.
Ägeda hematogeense osteomüeliidi septikopeemiline vorm on haiguse eriti levinud variant, mis avaldub ägeda sepsise tekkes. Mõnedel patsientidel täheldatakse lühikest prodromaalset intervalli, mida iseloomustab väsimus, nõrkus ja peavalu. Temperatuur tõuseb 39°C-ni, märkimisväärsete päevaste kõikumistega 1,5-2°C. Valu kahjustuse piirkonnas ilmneb paar tundi pärast patoloogilise protsessi algust. Valusündroomil on kähe iseloom, seda iseloomustab kõrge intensiivsus, patsient ei saa süüa ega magada, on pidevalt sundasendis, vältides igati igasugust puudutamist kahjustatud jäsemele. Üldine heaolu on äärmiselt halb, esinevad selged raske joobe tunnused. Kohalikud ilmingud avastatakse järk-järgult, valu lokaliseerub alles teisel päeval, kuid reaktsioon puudutusele ilmneb peaaegu kohe. Turse ja lokaalne pilt muutuvad selgeks alles kolmandal või neljandal päeval. Kui arstiabi ei osutata, lisandub turse piirkonda punetus ja värisemine. Selle vormiga kaasneb sageli mädase-nakkusliku protsessi metastaas, mille käigus tekivad mädased fookused teistes kudedes ja organites (luustruktuurid, kopsud, neerud, maks).
Ägeda hematogeense osteomüeliidi toksilist vormi (teised nimetused - välk, adünaamiline) iseloomustab kõige raskem kulg, domineerivate üldiste toksiliste ilmingutega. Patoloogia areneb kiiresti, hüpertermia on äge, saavutades kiiresti kõrgeid väärtusi 40-41 °C. Seisundil on eriline raskusaste, võimalik teadvusehäire, luulu-hallutsinatoorsed episoodid. Südametegevus on häiritud: esineb tahhükardia, nõrk pulsi täitumine, summutatud südametoonid. Sümptomite ebatüüpilisuse tõttu on seda vormi sageli raske diagnoosida. Patsiendi seisund on väga raske, mis paljudel juhtudel muudab primaarse põletikulise fookuse määramise võimatuks.
Tüsistused ja tagajärjed
Ägeda hematogeense osteomüeliidi tüsistused on lokaalsed ja üldised.
Kohalike hulgas on kõige levinumad:
- Deformatsioonid, luudefektid;
- Patoloogilised luumurrud;
- Valede liigeste moodustumine;
- Anküloos;
- Mädane artriit, flegmonid;
- Osteomüeliitilised haavandid;
- Fistuli seina pahaloomuline kasvaja.
Võimalikud levinud tüsistused:
- Septilised seisundid;
- Neeru amüloidoos;
- Siseorganite düstroofia.
Kõige sagedasem tüsistus on sepsis: selle teket täheldatakse hilinenud või ebaõige ravi korral.
Mädase artriidi esinemine on tingitud nakkustekitaja levikust kahjustatud luust läbi lümfisüsteemi või mädase läbimurdega liigeseõõnde.
Patoloogiline luumurd tekib kahjustatud luu hävimise tõttu. Sellisel juhul moodustub mõnikord vale liiges - patoloogia, mida iseloomustab luuelemendi järjepidevuse ja liikuvuse stabiilne häire, mis ei ole spetsiifiline konkreetsele osakonnale.
Epifüüsi ja metafüüsi hematogeenne patoloogia võib põhjustada kasvuhäireid ja luu tugevat moonutust (lühenemist), mis on tingitud fookuse otsesest asukohast kasvutsooni lähedal. [ 7 ]
Diagnostika äge hematogeenne osteomüeliit
Diagnostilised meetmed algavad kaebuste ja anamneesi kogumisega.
Patsient kurdab palaviku, kahjustatud luu valu ja motoorse funktsiooni häirete üle. Anamneesis võib viidata traumale, kirurgilistele sekkumistele, samuti muudele nakkuskolletele organismis.
Füüsilise läbivaatuse käigus märgatakse patoloogilise fookuse projektsiooni piirkonnas suurenenud valu palpatsioonil ja löökpillidel, palavikku, hüpereemiat ja turset.
Testid näitavad põletikulise protsessi olemasolu organismis: veres on leukotsütoos nihkega vasakule, samuti erütrotsüütide settereaktsiooni kiiruse suurenemine. Uriinis on valku, erütrotsüüte ja silindreid.
Instrumentaalne diagnostika hõlmab järgmisi uuringuid:
- Radiograafia - määratleb ägeda hematogeense osteomüeliidi tüüpilise pildi. See hõlmab: luu ähmast kujutist, luu risttalade virvendust ja seejärel - luu hõrenemise ja paksenemise vahelduvaid tsoone, luuümbrise paksenemist. Ägeda hematogeense osteomüeliidi radioloogilised tunnused avastatakse järk-järgult, 2-3 nädala jooksul alates haiguse algusest. Esmalt avastatakse luuümbrise irdumine koos periostiidi ilmingutega. Seejärel tekivad metafüüsi tsoonis hõreda koe alad. 8-16 nädala pärast tekivad sekvestratsioonid ja õõnsused.
- Ägeda hematogeense osteomüeliidi radioloogilist diagnoosi saab täiendada kontrastainega fistulograafiaga. Tänu uuringule selgub luuõõnsuste ja ümbritsevate pehmete kudede struktuuride täituvuse aste kontrastainega.
- Ultraheli abil saab hinnata põletikulise reaktsiooni leviku astet pehmetes kudedes, tuvastada sekvestratsioone ja paraosseoosseid mädaseid fookuseid.
- Angiograafiat kasutatakse avaskulaarsete luusegmentide tuvastamiseks ja flebotromboosi välistamiseks.
Tekitaja tuvastamiseks tehakse eraldi bakterioloogiline uuring. Enamikul patsientidest isoleeritakse Staphylococcus aureus, mõnevõrra harvemini Pseudomonas bacillus või Proteus, veelgi harvemini Enterobacteriaceae või anaeroobsed bakterid. [ 8 ]
Diferentseeritud diagnoos
Diferentsiaaldiagnoos tehakse hematogeense ja traumajärgse osteomüeliidi vahel.
Hematogeenne põletik |
Posttraumaatiline põletik |
|
Nad haigestuvad sagedamini |
Lapsed ja noorukid |
Enamasti täiskasvanud patsiendid |
Nakkuse tüüp |
Endogeenne-hematogeenne |
Eksogeenne |
Etioloogiline tegur |
Hematogeenne infektsioon |
Trauma koos infektsiooniga |
Domineeriv patogeen |
Kokid, Escherichia coli või Pseudomonas, Proteus, segainfektsioon |
|
Reaktiivne olek |
Keha reaktsioonivõime järsk tõus |
Normaalne keha reaktsioonivõime |
Morfoloogiline tegur |
Primaarne osteomüeliit |
Teisene mädane ostiit |
Sekvestreerimine |
Tõelised sekvestratsioonid toimuvad kogu patoloogilise protsessi vältel. |
Pseudoquestrianid tekivad esimesena, tõelised hiljem |
Luumurd |
See on haruldane |
Esineb aluseks oleva patoloogiana |
Liigese infektsioon |
See on üsna tavaline nähtus |
Harva, ainult liigesesisese murru korral |
Septilised tüsistused |
Sageli |
Harva |
Kellega ühendust võtta?
Ravi äge hematogeenne osteomüeliit
Terapeutilised meetmed on kiireloomulised ja keerukad, need hõlmavad võimalikult varast mõju tekitajale, väldivad septilisi tüsistusi ja piiravad infektsiooni lokaalset fookust. Oluline on leevendada joovet nii kiiresti kui võimalik, minimeerida elutähtsate organite koormust, optimeerida patsiendi kaitsepotentsiaali ja valmistada teda ette eelseisvaks kirurgiliseks sekkumiseks. [ 9 ]
Esiteks on vaja normaliseerida kehatemperatuuri ja ennetada tokseemia teket, mis on eriti oluline lastel. Kasutage füüsikalisi jahutusmeetodeid, laiendage perifeerseid veresooni meditsiiniliselt (Drotaveriin, Papaveriin) ja alandage temperatuuri (manustage 4% amidopüriini koguses 0,1 ml/kg, 50% analgiini koguses 0,1 ml lapse eluaasta kohta). Homöostaasi korrigeeritakse intravenoosse infusiooniga, et kõrvaldada hüpovoleemia ja stabiliseerida vee-soola ja happe-aluse tasakaal.
Infusioonravi alustatakse glükoosilahuse ja keskmise ja madala molekulmassiga detoksifitseeriva toimega polümeeride (Reopolyglukin, Hemodez jne) ning valgulahuste (natiivne plasma, albumiin, veri) manustamisega. Vedeliku mahtu täiendatakse elektrolüüdilahustega. Atsidootilise seisundi korrigeerimine viiakse läbi 4% naatriumvesinikkarbonaadi või trisamiini manustamisega. Raske mürgistuse korral koos düspepsia ja hüpokaleemiaga manustatakse kaaliumkloriidi. Vajadusel kasutatakse spetsiaalseid tehnikaid, viiakse läbi hemosorptsioon - kehaväline vere puhastamine.
Kõige keerulisemate patsientide puhul tehakse vahetustransfusioon, mille käigus asendatakse 1,5–2 mahuosa ringlevat verd. Kasutatakse ka forsseeritud diureesi, suurendades veekoormust 5% glükoosilahuse, Ringer-Locke'i lahuse ning mannitooli ja Lasixi edasise manustamisega.
Mõned patsiendid praktiseerivad edukalt plasmafereesi, kasutavad proteolüüsi inhibiitoreid (Trasylol, Contrical). Levinud intravaskulaarse koagulatsiooni sündroomi kõrvaldamiseks manustatakse hepariini intravenoosselt koguses 1--=150 ühikut kg kohta 6 tunni jooksul (mitte varem kui 12 tundi pärast operatsiooni). Kapillaaride läbilaskvuse vähendamiseks kasutatakse C-vitamiini, rutiini ja kaltsiumi sisaldavaid ravimeid.
Ainevahetuse aktiveerimiseks on ette nähtud pentoksool, metüüluratsiil, kaaliumorotaat. Immunoterapeutilised meetmed hõlmavad hüperimmuunse stafülokokivastase plasma, stafülokoki vaktsiini ja hüperimmuunse stafülokokivastase γ-globuliini infusiooni.
Parenteraalse toitumise pakkumine on kohustuslik, arvutades arvesse valkude, rasvade, süsivesikute soovitatavat kalorisisaldust ja tasakaalu. Võimaluse korral viiakse patsient järk-järgult üle normaalsele dieedile.
Antibiootikumravi viiakse läbi samaaegselt infusioonidega (intravenoosne, intramuskulaarne) ja intraosseousselt (kahjustatud luusse). Enne tekitaja tuvastamist manustatakse aja raiskamata penitsilliini naatriumsoola intravenoosselt suurtes annustes. Intraosseousne manustamine hõlmab laia toimespektriga antibiootikumide kasutamist.
48 tundi pärast bakteriaalsete testide hindamist manustatakse intraosseaalset süsti, olenevalt resistentsusest: tsefalosporiini preparaate, gentamütsiini, klaforaani jne. Võimalik on täiendav 5–10 miljoni ühiku penitsilliini süstimine koos 20 ml 0,25% novokaiiniga reiearterisse.
Intraosseaalseks süstimiseks mõeldud preparaadid jahutatakse eelnevalt temperatuurini +20°C.
Ägeda hematogeense osteomüeliidi lokaalne ravi
Kohaliku ravi peamine eesmärk on vähendada kõrget luusisest rõhku ja vältida patoloogilise protsessi edasist levikut. Periostoomiat täiendavad spetsiifilised mikroskoopilised trepanatsioonid, mis võimaldavad õõnsust tühjendada ilma luustruktuuri häirimata.
Tehnika hõlmab järgmisi manipulatsioone:
- Naha ja PJC lõikamine suurima valu piirkonnas;
- Lihaste eraldamine mööda kiude;
- Periosteumi flegmoni avamine ja selle puudumisel - periosteumi dissektsioon;
- Perforatsiooniaukude tegemine spetsiaalsete freesidega, mille keskele asetatakse nõel intraosseosse antibiootikumravi jaoks;
- Kipsist lahas.
Totaalsete luukahjustuste korral tehakse ülaltoodud manipulatsioonid kahes metafüüsi piirkonnas. Postoperatiivses staadiumis patsienti riietatakse ja uuritakse iga päev ning vajadusel tehakse haava revisjon. Samuti uuritakse kogu skeleti süsteemi, et õigeaegselt kindlaks teha tõenäolised sekundaarselt nakatunud fookused. Selliste fookuste leidmisel tehakse luu punktsioon koos temperatuuri ja rõhu mõõtmisega.
Ägeda põletikulise protsessi taandumisel saab rakendada füsioteraapiat. Antibakteriaalsete ravimite elektroforees, UVA, ülikõrgsageduslik ravi on ette nähtud.
Umbes kuu aega hiljem tehakse kontrollröntgenograafia ja hinnatakse ravi dünaamikat.
Ägeda hematogeense osteomüeliidi kirurgiline ravi
Kirurgiline sekkumine hematogeense osteomüeliidi korral on ette nähtud järgmistel juhtudel:
- Sekvestreerimine;
- Osteomüeliitiline luuõõnsus;
- Fistulid või haavandid;
- Muutused parenhümatoossetes organites (osteomüeliidi tõttu);
- Lokaliseeritud pahaloomulisuse korral.
Ägeda hematogeense osteomüeliidi kirurgiline ravi võib olla radikaalne, tavapäraselt radikaalne ja rekonstruktiivne.
Radikaalsed sekkumised hõlmavad järgmist:
- Mõjutatud luusegmendi marginaalne resektsioon;
- Pika luu osa lõplik resektsioon keerulise traumaatilise osteomüeliidi korral;
- Pika luu osa segmentaalne resektsioon;
- Segmendi disartikulatsioon või eemaldamine koos kahjustatud luuga.
Tingimuslikult radikaliseerunud sekkumised hõlmavad järgmist:
- Fistulosekvestrektoomia - hõlmab fistuli kanalite ekstsisiooni koos luu sekvestratsiooniga;
- Sekvestrnekrektoomia - seisneb luu trepanatsiooni järgselt tihendatud karbist sekvestratsioonide resektsioonis või luuõõnsuse eemaldamises navikulaarse lamestamise vormis;
- Fistuloosekvestrnekrektoomia (teine nimetus: laiendatud nekrektoomia) - hõlmab nekroosi, sekvestrumi, granulatsiooni, fistuli või armkoe tüki eemaldamist tervete struktuuride sees;
- Luuüdi kanalis oleva tihendatud kasti ligipääsemiseks ja selle läbitavuse edasiseks taastamiseks teostatakse pika toruluu trepanatsioon sekvestrnekrektoomiaga;
- Osteomüeliidi fookuse eemaldamine, millele järgneb bilokaalne perkutaanne kompressioon-distraktsiooniosteosüntees luudefekti asendamiseks.
Taastavad sekkumised hõlmavad väljendunud koedefektide asendamist ja võivad olla järgmised:
- Pehmete kudede plastmaterjalid (klapiülekanded);
- Plastist asendamine vaskulariseeritud koega;
- Kombineeritud tehnikad;
- Jäänud õõnsuse täitmine;
- Luuõõnsuste plastika verega toidetud kudedega (nt müoplastika);
- Asendusoperatsioon Ilizarovi meetodil, ekstraaksiaalne osteosüntees.
Ärahoidmine
Ennetamine seisneb varajases diagnoosimises, õigeaegses hospitaliseerimises, täieliku terapeutilise ja kirurgilise abi osutamises nakkus-põletikuliste protsessidega patsientidele. Vajadusel määratakse antibiootikumravi kuurid, stafülokokivastane plasma ja immuniseerimine stafülokoki toksiiniga, autovaktsineerimine, retikuloendoteliaalsüsteemi funktsioonide stimuleerimine. Kohustuslik on välistada provotseerivate tegurite, näiteks ümbrise temperatuuri järsk muutus (hüpotermia, ülekuumenemine), trauma jne, agressiivse mõju võimalus.
Ägeda hematogeense osteomüeliidi teket saab vältida potentsiaalselt ebasoodsate tegurite mõju vältimisega. Näiteks räägime vahelduvatest nakkusprotsessidest, stressirohketest olukordadest, liigsest füüsilisest aktiivsusest, liigsest külmast või kuumast.
Levinud terapeutiliste sekkumiste hulka kuuluvad:
- Tervisliku eluviisi juhtimine;
- Täisväärtuslik, mitmekesine ja kvaliteetne toitumine;
- Stressirohkete olukordade vältimine;
- Regulaarne immuunsüsteemi toetamine;
- Nakkushaiguste õigeaegne puhastamine;
- Õigeaegne arstiabi otsimine vigastuste, traumade ja haavade korral.
Olulist rolli mängib ja väldib eneseravimist: patoloogiliste protsesside tekkes on vigastuste (nii suletud kui ka avatud) korral arstidega konsulteerimine kohustuslik.
Prognoos
Kõik patsiendid, kes on läbinud ägeda hematogeense osteomüeliidi, tuleb tingimata registreerida ambulatooriumi andmetes. See on vajalik haiguse kordumise (ägenemise) õigeaegseks avastamiseks, ravi tulemuste hindamiseks ja ennetavaks antibiootikumraviks (näiteks kõige "ohtlikumal" perioodil - kevadel ja sügisel). Haiguse põdenud inimene peaks külastama oma perearsti vähemalt kaks korda aastas.
Alates esimesest päevast pärast hematogeense osteomüeliidi operatsiooni suurendatakse patsiendi motoorset aktiivsust järk-järgult:
- Luba voodi piires pöördeid;
- Tehke hingamisharjutusi (staatilised ja dünaamilised harjutused);
- Soovitatav on torso tõsta, hoides samal ajal kinni voodi kohal olevast riputusseadmest.
Taastusravi kiirendamiseks, troofiliste ja ainevahetusprotsesside parandamiseks on ette nähtud füüsikalised protseduurid - eelkõige magnetoteraapia ja UVB. Füsioteraapia terapeutiline kuur võib hõlmata viit kuni kümmet protseduuri.
Üldiselt on ägedal hematogeensel osteomüeliidil tingimuslikult soodne prognoos. Patsiendi taastumisvõimalused ja lihasluukonna mehhanismide funktsionaalsuse täielik taastumine sõltuvad patoloogilise protsessi astmest ja valitud ravi edukusest, samuti kirurgilise ravi õigeaegsusest ja radikaalsusest.
Ägeda hematogeense osteomüeliidi uurimisega seotud autoriteetsete raamatute ja uuringute loetelu
- "Luu- ja liigeseinfektsioonid: mikrobioloogiast diagnostika ja ravini" - autorid: W. Zimmerli, ME Corti (aasta: 2015)
- "Osteomüeliit: diagnoosimine, ravi ja prognoos" - autor Mahmut Nedim Doral (aasta: 2012)
- "Laste osteoartikulaarsed infektsioonid" - autorid Pierre Lascombes, Antoine GS Lascombes (aasta: 2017)
- "Osteomüeliit: riskifaktorid, diagnoosimine ja ravivõimalused" - autor Thore Zantop (aasta: 2016)
- "Osteomüeliit - meditsiiniline sõnastik, bibliograafia ja internetiviidete selgitustega uurimisjuhend" - Icon Health Publications (aasta: 2004)
- "Osteomüeliit: sümptomid, põhjused ja ravi" - autor Alton Carr (aasta: 2012)
- "Osteomüeliidi uuringute edusammud" - autor Carlos A. Leonard (aasta: 2007)
- "Luu- ja liigeseinfektsioonid: bakterioloogiast diagnostika ja ravini" - autor Andreas F. Mavrogenis (aasta: 2018)
- Amy L. Leberi "Kliinilise mikrobioloogia protseduuride käsiraamat, 1. köide" (aasta: 2016)
- "Osteomüeliit: uued teadmised tervishoiutöötajatele: 2012. aasta väljaanne" - autor Q. Ashton Acton (aasta: 2012)
Kirjandus
Kotelnikov, traumatoloogia perearst / toimetanud Kotelnikov perearst, Mironovi tehniline kliinik - Moskva: GEOTAR-Media, 2018.

