Artikli meditsiiniline ekspert
Uued väljaanded
Fibroelastoos
Viimati vaadatud: 05.07.2025

Kõik iLive'i sisu vaadatakse meditsiiniliselt läbi või seda kontrollitakse, et tagada võimalikult suur faktiline täpsus.
Meil on ranged allhanke juhised ja link ainult mainekate meediakanalite, akadeemiliste teadusasutuste ja võimaluse korral meditsiiniliselt vastastikuste eksperthinnangutega. Pange tähele, et sulgudes ([1], [2] jne) olevad numbrid on nende uuringute linkideks.
Kui tunnete, et mõni meie sisu on ebatäpne, aegunud või muul viisil küsitav, valige see ja vajutage Ctrl + Enter.
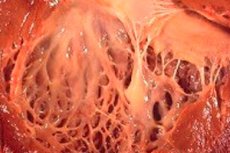
Meditsiinis viitab termin "fibroelastoos" keha siseorganite ja veresoonte pinda katva sidekoe muutustele, mis on põhjustatud elastsete kiudude kasvu häiretest. Samal ajal täheldatakse elundite seinte ja nende struktuuride paksenemist, mis mõjutab paratamatult keha elutähtsate süsteemide, eriti südame-veresoonkonna ja hingamissüsteemi toimimist. See omakorda toob kaasa patsiendi heaolu halvenemise, eriti füüsilise koormuse ajal, mis mõjutab elukvaliteeti ja -kestust.
Epidemioloogia
Üldiselt võib haigused, millega kaasnevad sidekoe muutused, mille tulemuseks on siseorganite membraanide ja vaheseinte paksenemine, jagada kahte rühma: südame fibroelastoos ja kopsufibroelastoos. Südamepatoloogia võib olla nii kaasasündinud kui ka omandatud; haiguse kopsuvormi puhul räägime omandatud haigusest.
Kopsu fibroelastoos hakkab arenema keskeas (lähemal 55–57. eluaastal), kuigi pooltel juhtudel tuleb haiguse päritolu otsida lapsepõlves. Iseloomulik on „kerge“ periood, mil haiguse sümptomid puuduvad. Samal ajal ei ole haigusel soolisi eelistusi ja see võib võrdselt mõjutada nii naisi kui ka mehi. Seda üsna haruldast patoloogiat iseloomustavad muutused kopsu pleura ja parenhüümi (funktsionaalsete rakkude) kudedes, peamiselt kopsu ülemises osas. Kuna haiguse etioloogia ja patogenees on endiselt ebaselged, liigitatakse see idiopaatiliseks patoloogiaks. Meditsiinilise terminoloogia kohaselt nimetatakse seda „pleuroparenhümatoosseks fibroelastoosiks“. [ 1 ]
Südame fibroelastoos on üldistatud nimetus südamemembraanide patoloogiale, mida iseloomustab nende paksenemine ja funktsionaalsuse vähenemine. Patoloogia kaasasündinud vorme iseloomustab südame sisemembraani difuusne (laialt levinud) paksenemine. See on õhuke sidekude, mis vooderdab südameõõnsust (selle sektsioone) ja moodustab selle klapid.
Täiskasvanud patsientidel diagnoositakse tavaliselt haiguse fokaalne vorm, kui südame sisepind näib olevat kaetud tugevama ja paksema koe laikudega (see võib hõlmata mitte ainult ülekasvanud kiude, vaid ka trombootilisi masse).
Pooltel südame fibroelastoosi juhtudest pakseneb mitte ainult elundi sein, vaid ka klapid (kaksikklapp mitraalklapis samanimelise koja ja vatsakese vahel, trikuspidaalklapis aordiklapis vasaku vatsakese ja aordi vahel ning kopsuklapis parema vatsakese ja kopsuarteri vahel). See omakorda võib häirida klappide tööd ja põhjustada arteriaalse ava ahenemist, mis on südame teiste õõnsustega võrreldes juba niigi väike.
Meditsiinilises terminoloogias nimetatakse endokardiaalset fibroelastoosi endokardiaalseks fibroelastoosiks (prenataalne fibroelastoos, endokardiaalne skleroos, loote endokardiit jne). Kuid üsna sageli võib protsessis osaleda ka südamemembraani keskmine lihaskiht. [ 2 ]
Müokardi (südame lihaskiht, mis koosneb kardiomüotsüütidest) struktuuri anomaaliad, geenimutatsioonid ja rasked nakkusprotsessid võivad põhjustada fibroelastoosi levinud vormi, kui protsessis osaleb lisaks endokardile ka müokardi membraan. Tavaliselt tekivad endokardi düsplastilised protsessid, mis on põhjustatud erinevatel põhjustel, selle kokkupuute piiril lihasmembraaniga, häirides selle kihi kontraktiilsust. Mõnel juhul esineb isegi sisemise kihi sissekasvamist müokardi, kardiomüotsüütide asendumist fibroblastide ja kiududega, mis mõjutab närviimpulsside juhtivust ja südame rütmilist tööd.
Südamemembraani paksuse veresoonte kokkusurumine paksenenud müokardi poolt häirib müokardi toitumist (müokardi isheemia), mis omakorda võib viia südamelihase kudede nekroosini.
Südamelihase kahjustusega endokardiaalset fibroelastoosi nimetatakse subendokardiaalseks või endomüokardiaalseks fibroelastoosiks.
Statistika kohaselt diagnoositakse enamikul selle haruldase haiguse juhtudest (ainult 0,007% vastsündinute koguarvust) südame vasaku vatsakese fibroelastoos, kuigi mõnel juhul levib protsess ka paremasse vatsakesse ja kodadesse, sealhulgas neid eraldavatesse klappidesse.
Südame fibroelastoosiga kaasneb sageli suurte koronaarveresoonte kahjustus, mis on samuti kaetud sidekoega. Täiskasvanueas esineb see sageli progresseeruva veresoonte ateroskleroosi taustal.
Haigus registreeritakse sagedamini troopilises Aafrika riikides madala elatustasemega elanikkonna seas, mida soodustab halb toitumine, sagedased infektsioonid ning teatud toiduained ja taimed, mida tarbitakse toiduna.
Endokardi paksenemist täheldatakse ka Löffleri fibroplastilise endokardiidi viimases staadiumis, mis mõjutab peamiselt keskealisi mehi. Selle haiguse patogenees on seotud ka nakkushaigustega, mis põhjustavad raske eosinofiilia arengut, mis on tüüpilisem sisemiste parasiitide infektsioonide korral. Sellisel juhul hakkavad keha koed (peamiselt südamelihas ja aju) kogema hapnikupuudust (hüpoksiat). Vaatamata südame fibroelastoosi ja Löffleri fibroosse endokardiidi sümptomite sarnasusele peavad arstid neid täiesti erinevateks haigusteks.
Põhjused fibroelastoos
Fibroelastoos viitab sidekoe muutustele elutähtsates organites: südames ja kopsudes, millega kaasneb organite funktsiooni häire ning mis kajastub patsiendi välimuses ja seisundis. Arstid on sellest haigusest teadnud aastakümneid. Südame sisemise vohamise (endokardi) fibroelastoosi kirjeldati juba 18. sajandi alguses ja sarnaseid muutusi kopsudes hakati arutama kaks ja pool sajandit hiljem. Siiski pole arstid sidekoe patoloogilise vohamise põhjuste osas veel lõplikule kokkuleppele jõudnud.
Jääb selgusetuks, mis täpselt põhjustab sidekoe kasvu ja arengu häireid. Kuid teadlased tuvastavad selliste muutuste teatud riskifaktorid, pidades neid haiguse võimalikeks (kuid mitte lõplikeks) põhjusteks.
Seega on kopsufibroelastoosi patogeneesis, mida peetakse küpsete inimeste haiguseks, eriline roll elundi korduvatel nakkushaigustel, mida esineb pooltel patsientidest. Infektsioonid provotseerivad kopsukoe ja pleura põletikku ning pikaajaline põletik soodustab nende kiulist muundumist.
Mõnedel patsientidel on fibroelastoosi perekondlik anamnees, mis viitab pärilikule eelsoodumusele. Nende kehas on leitud mittespetsiifilisi autoantikehi, mis provotseerivad pikaajalisi ebaselge etioloogiaga põletikulisi protsesse.
On olemas arvamus, et kopsukoe fibroossed muutused võivad olla põhjustatud gastroösofageaalsest reflukshaigusest. Kuigi see seos on tõenäoliselt kaudne. Samuti arvatakse, et fibroelastoosi risk on suurem neil, kes kannatavad südame-veresoonkonna haiguste või kopsutromboosi all.
Pulmonaalne fibroelastoos noores ja noorukieas võib end raseduse ajal meenutada. Tavaliselt on haigus varjatud umbes 10 aastat või kauem, kuid see võib avalduda ka varem, võimalik, et tänu lapseootel ema keha suurenenud koormusele ja hormonaalsetele muutustele, kuid täpset selgitust pole veel. Sellest hoolimata täheldati sarnast haiguse arengu pilti 30%-l uuritud reproduktiivses eas patsientidest.
Rasedus ise ei saa haigust põhjustada, kuid see võib kiirendada sündmuste arengut, mis on väga kurb, sest haiguse suremus on väga kõrge ja fibroelastoosiga eluiga on lühike.
Enamasti võib südame fibroelastoosi seostada lastehaigustega. Kaasasündinud patoloogia avastatakse sünnieelsel perioodil 4-7 kuu vanusel lootel, kuid diagnoosi saab kinnitada alles pärast lapse sündi. Selle haigusvormi patogeneesis arvestatakse mitmete võimalike negatiivsete teguritega: lootele edasi antud ema nakkus- ja põletikulised haigused, südamemembraanide arengu kõrvalekalded, südamekoe verevarustuse häired, geneetilised mutatsioonid, hapnikupuudus.
Arvatakse, et infektsioonide seas annavad viirused südame fibroelastoosi tekkesse suurima patogeneetilise panuse, kuna nad kinnistuvad keha rakkudesse, hävitavad neid ja muudavad kudede omadusi. Loote vormimata immuunsüsteem ei suuda teda nende patogeenide eest kaitsta, erinevalt lapseootel ema immuunsusest. Viimane ei pruugi viirusnakkuse tagajärgi kogeda, samas kui lootel võib emakasisene infektsioon esile kutsuda mitmesuguste anomaaliate ilmnemise.
Mõned teadlased usuvad, et fibroelastoosi nakkusliku vormi patogeneesis mängib otsustavat rolli infektsioon, mis mõjutab loodet kuni 7 kuu vanuselt. Hiljem võib see põhjustada ainult südame põletikulisi haigusi (müokardiit, endokardiit).
Südame membraanide ja klappide arengu anomaaliaid võib esile kutsuda nii põletikuline protsess kui ka ebapiisavad autoimmuunreaktsioonid, mille tagajärjel hakkavad immuunsüsteemi rakud ründama organismi enda rakke.
Geenimutatsioonid põhjustavad sidekoe ebanormaalset arengut, kuna geenid sisaldavad teavet valgustruktuuride (eriti kollageeni- ja elastiinivalkude) struktuuri ja käitumise kohta.
Südamekoe hüpoksia ja isheemia võivad olla südame ebanormaalse arengu tagajärg. Sellisel juhul räägime sekundaarsest fibroelastoosist, mida provotseerivad kaasasündinud südamerikked. Nende hulka kuuluvad sellised anomaaliad, mis põhjustavad obstruktsiooni (südame ja selle veresoonte läbitavuse halvenemine):
- aordi stenoos või ahenemine klapi lähedal,
- aordi koarktatsioon või segmentaalne ahenemine selle kaare ja laskuva osa ristumiskohas,
- atresia või aordi loomuliku ava puudumine,
- südamekoe (kõige sagedamini vasaku vatsakese, harvemini parema vatsakese ja kodade) vähearenenud areng, mis mõjutab südame pumpamisfunktsiooni.
On arvamus, et toksikoos raseduse ajal võib olla ka loote fibroelastoosi soodustavaks teguriks.
Postnataalsel perioodil võivad südame fibroelastoosi arengut soodustada elundimembraanide nakkus- ja põletikulised haigused, vigastuste tagajärjel tekkinud hemodünaamilised häired, veresoonte trombemboolia, müokardi hemorraagia, ainevahetushäired (suurenenud fibriini moodustumine, valkude ja raua ainevahetushäired: amüloidoos, hemokromatoos). Samad põhjused põhjustavad haiguse arengut ka täiskasvanutel.
Pathogenesis
Sidekude on inimkeha eriline kude, mis on osa peaaegu kõigist organitest, kuid ei osale aktiivselt nende funktsioonides. Sidekoele omistatakse tugi- ja kaitsefunktsioone. Moodustades omamoodi skeleti (raamistiku, strooma) ja piirates organi funktsionaalseid rakke, tagab see selle lõpliku kuju ja suuruse. Piisava tugevusega sidekude kaitseb ka organi rakke hävimise ja vigastuste eest, takistab patogeenide tungimist ning spetsiaalsete makrofaagide rakkude abil absorbeerib vananenud struktuure: surnud koerakke, võõrvalke, vere jääkaineid jne.
Seda kude võib nimetada abikoeks, kuna see ei sisalda rakulisi elemente, mis tagaksid ühe või teise organi funktsionaalsuse. Sellest hoolimata on selle roll keha elus üsna suur. Veresoonte membraanide osana tagab sidekude nende struktuuride ohutuse ja funktsionaalsuse, tänu millele toimub keha sisekeskkonna ümbritsevate kudede toitumine ja hingamine (trofism).
Sidekude on mitut tüüpi. Siseorganeid katvat membraani nimetatakse lahtiseks sidekoeks. See on poolvedel, värvitu aine, mis sisaldab lainelisi kollageenkiude ja sirgeid elastiinkiude, mille vahel on juhuslikult hajutatud erinevat tüüpi rakke. Mõned neist rakkudest (fibroblastid) vastutavad kiuliste struktuuride moodustumise eest, teised (endoteliotsüüdid ja nuumrakud) moodustavad poolläbipaistva sidekoe maatriksi ja toodavad spetsiaalseid aineid (hepariin, histamiin), teised (makrofaagid) pakuvad fagotsütoosi jne.
Teist tüüpi kiuline kude on tihe sidekude, mis ei sisalda suurt hulka üksikuid rakke ja mis omakorda jaguneb valgeks ja kollaseks. Valge kude koosneb tihedalt pakitud kollageenkiududest (sidemed, kõõlused, luuümbris) ja kollane kude koosneb kaootiliselt põimunud elastiinkiududest koos fibroblastide kaasamistega (osa sidemetest, veresoonte membraanidest, kopsudest).
Sidekudede hulka kuuluvad ka veri, rasv, luu- ja kõhrkude, kuid need meid veel ei huvita, kuna fibroelastoosi all peame silmas muutusi kiudstruktuurides. Elastsed ja elastsed kiud sisalduvad ainult lahtistes ja tihedates sidekudedes.
Fibroblastide süntees ja neist sidekoe kiudude moodustumine reguleeritakse aju tasandil. See tagab selle omaduste (tugevus, elastsus, paksus) püsivuse. Kui mingite patoloogiliste põhjuste tõttu on abikoe süntees ja areng häiritud (fibroblastide arv suureneb, nende "käitumine" muutub), toimub tugevate kollageenikiudude vohamine või elastsete kiudude kasvu muutus (need jäävad lühikeseks, keerduvad), mis viib elundi membraani ja mõnede sidekoega kaetud sisemiste struktuuride omaduste muutumiseni. Need omandavad vajalikust suurema paksuse, muutuvad tihedamaks, tugevamaks ja elastsemaks, meenutades sidemetes ja kõõlustes olevat kiulist kude, mille venitamiseks on vaja suuri pingutusi.
Selline kude ei veni hästi, piirates elundi liikumist (südame ja veresoonte automaatsed rütmilised liigutused, kopsude suuruse muutused sisse- ja väljahingamisel), seega häiritakse verevarustust ja hingamiselundeid, mis viib hapnikupuuduseni.
Fakt on see, et keha verevarustus toimub tänu südamele, mis töötab pumbana, ja kahele vereringe ringile. Kopsuvereringe vastutab verevarustuse ja gaasivahetuse eest kopsudes, kust hapnik toimetatakse verevooluga südamesse ja sealt edasi süsteemsesse vereringesse ning jaotub kogu kehas, pakkudes hingamist organitele ja kudedele.
Elastne membraan, mis piirab südamelihase kokkutõmbumist, vähendab südame funktsionaalsust, mistõttu süda ei pumpa verd ja koos sellega hapnikku nii aktiivselt. Kopsude fibroelastoosi korral on nende ventilatsioon (osigenatsioon) häiritud, mistõttu verre hakkab sisenema vähem hapnikku, mis isegi normaalse südamefunktsiooni korral aitab kaasa kudede ja organite hapnikupuudusele (hüpoksiale). [ 3 ]
Sümptomid fibroelastoos
Südame- ja kopsufibroelastoos on kahte tüüpi haigusi, mida iseloomustab sidekoe kiudude sünteesi häire. Neil on erinev lokaliseerimine, kuid mõlemad on potentsiaalselt eluohtlikud, kuna on seotud progresseeruva või raske südame- ja hingamispuudulikkusega.
Kopsu fibroelastoos on haruldane interstitsiaalne haigus selles olulises hingamissüsteemi organis. Nende hulka kuuluvad kopsu parenhüümi kroonilised patoloogiad, mis kahjustavad alveolaarseinte seinu (põletik, nende struktuuri ja struktuuri häired), kopsu kapillaaride sisemist voodrit jne. Fibroelastoos peetakse sageli haruldaseks progresseeruva kopsupõletiku erivormiks, millel on kalduvus fibroossetele muutustele kopsu ja pleura kudedes.
Haigust on peaaegu võimatu alguses avastada, sest see ei pruugi endast umbes 10 aastat meelde tuletada. Seda perioodi nimetatakse selgeks intervalliks. Patoloogiliste muutuste algust, mis veel ei mõjuta kopsude mahtu ja gaasivahetust, saab tuvastada juhuslikult, kopsude üksikasjaliku uurimise käigus seoses mõne muu hingamissüsteemi haiguse või vigastusega.
Haigusele on iseloomulik sümptomite aeglane progresseerumine, seega võivad haiguse esimesed ilmingud selle algusest märkimisväärselt edasi lükkuda. Sümptomid süvenevad järk-järgult.
Haiguse esimesed tunnused, millele tasub tähelepanu pöörata, on köha ja süvenev õhupuudus. Sellised sümptomid on sageli varasema hingamisteede haiguse tagajärg, seega võivad need pikka aega olla seotud külmetuse ja selle tagajärgedega. Õhupuudust tajutakse sageli südamehaiguse või vanusega seotud muutustena. Lõppude lõpuks diagnoositakse haigust eakatel inimestel.
Vigu võivad teha nii patsiendid kui ka neid uurivad arstid, mis viib ohtliku haiguse hilise avastamiseni. Tasub pöörata tähelepanu köhale, mis on fibroelastoosi korral ebaproduktiivne, kuid mida ei stimuleeri mukolüütikumid ja rögalahtistid, vaid peatavad köhavastased ravimid. Sellist laadi pikaajaline köha on kopsufibroelastoosi iseloomulik sümptom.
Düspnoe tekib progresseeruva hingamispuudulikkuse tõttu, mis on tingitud alveolaarseinte ja pleura paksenemisest, kopsu alveolaarsete õõnsuste mahu ja arvu vähenemisest (elundi parenhüüm on röntgenpildil nähtav kärgstruktuurina). Sümptom intensiivistub füüsilise koormuse mõjul, algul märkimisväärsel ja seejärel isegi väikesel määral. Haiguse progresseerumisel see süveneb, mis põhjustab patsiendi puude ja surma.
Fibroelastoosi progresseerumisega kaasneb üldise seisundi halvenemine: hüpoksia põhjustab nõrkust ja pearinglust, kehakaal väheneb (tekib isutus), küünefalangid muutuvad trummipulkade tüübiks, nahk muutub kahvatuks ja haiglase välimusega.
Pooltel patsientidest tekivad mittespetsiifilised sümptomid nagu hingamisraskused ja valu rinnus, mis on iseloomulikud pneumotooraksile( gaaside kogunemine pleuraõõnde).See anomaalia võib tekkida ka vigastuste, primaarsete ja sekundaarsete kopsuhaiguste, ebaõige ravi tagajärjel, mistõttu seda ei saa diagnoosida.
Südame fibroelastoosi, aga ka kopsude sidekoe kasvu patoloogiat iseloomustab: kahvatu nahk, kaalulangus, nõrkus, mis on sageli paroksüsmaalne, õhupuudus. Samuti võib täheldada püsivat subfebriili temperatuuri ilma külmetuse või infektsiooni tunnusteta.
Paljudel patsientidel esineb muutusi maksa suuruses. See suureneb ilma düsfunktsiooni sümptomiteta. Samuti on võimalik jalgade, näo, käte ja ristluu piirkonna turse.
Haiguse iseloomulikuks ilminguks peetakse südame töö häirega seotud süvenevat vereringepuudulikkust. Sellisel juhul diagnoositakse tahhükardia (südame löögisageduse tõus, sageli koos arütmiaga), õhupuudus (sealhulgas füüsilise aktiivsuse puudumisel), kudede tsüanoos (sinakas värvus, mis on põhjustatud karboksühemoglobiini kogunemisest veres, st hemoglobiini ja süsinikdioksiidi ühendist häiritud verevoolu ja vastavalt ka gaasivahetuse tõttu).
Sellisel juhul võivad sümptomid ilmneda kas kohe pärast selle patoloogiaga lapse sündi või aja jooksul. Vanemate laste ja täiskasvanute puhul ilmnevad raske südamepuudulikkuse tunnused tavaliselt hingamisteede infektsiooni taustal, mis toimib päästikuna. [ 4 ]
Fibroelastoos lastel
Kui kopsufibroelastoos on täiskasvanute haigus, mis sageli pärineb lapsepõlvest, kuid ei anna endast pikka aega märku, siis sarnane südame endokardi patoloogia ilmneb sageli juba enne lapse sündi ja mõjutab tema elu esimestest sünnihetkedest alates. See haruldane, kuid raske patoloogia on imikute raskesti korrigeeritava südamepuudulikkuse tekke põhjuseks, kellest paljud surevad 2 aasta jooksul. [ 5 ]
Vastsündinute endokardiaalne fibroelastoos on enamasti lapse kehas sünnieelses eas toimuvate patoloogiliste protsesside tagajärg. Emalt saadud infektsioonid, geneetilised mutatsioonid, südame-veresoonkonna arengu kõrvalekalded, pärilikud ainevahetushaigused – kõik see võib teadlaste sõnul viia südame membraanide sidekoe muutusteni. Eriti kui 4–7-kuune loode puutub kokku kahe või enama teguriga korraga.
Näiteks südame ja pärgarterite arengus esinevate kõrvalekallete (stenoos, atresia, aordi koarktatsioon, müokardirakkude ebanormaalne areng, endokardi nõrkus jne) kombinatsioon, mis soodustab koeisheemiat, koos infektsioonist tingitud põletikulise protsessiga, jätab lapse praktiliselt ilma suurema või väiksema ellujäämisvõimaluseta. Kuigi elundite arenguhäireid saab veel kiiresti korrigeerida, saab progresseeruvat fibroelastoosi ainult aeglustada, kuid mitte ravida.
Tavaliselt avastatakse loote südame fibroelastoos juba raseduse ajal teisel või kolmandal trimestril ultraheli diagnostika käigus. 20.–38. nädalal tehtud ultraheli ja ehhokardiograafia näitasid hüperehhogeensust, mis näitab endokardi paksenemist ja tihenemist (tavaliselt difuusne, harvemini fokaalne), südame suuruse ja kuju muutust (elund on suurenenud ja võtab palli või kuuli kuju, sisemised struktuurid siluvad järk-järgult). [ 6 ]
30–35% juhtudest avastati fibroelastoos enne 26. rasedusnädalat, 65–70% juhtudest järgneval perioodil. Enam kui 80% vastsündinutest on fibroelastoos kombineeritud obstruktiivsete südameriketega, st see on sekundaarne, hoolimata selle avastamise varasest staadiumist. Vasaku vatsakese hüperplaasia avastati pooltel haigestunud lastest, mis selgitab fibroelastoosi suurt levimust just selles südamestruktuuris. Aordi ja selle klapi patoloogiad, mis on kindlaks tehtud kolmandikul endokardi proliferatsiooniga lastest, põhjustavad samuti vasaku vatsakese kambri suurenemist (laienemist) ja selle funktsionaalsuse häireid.
Instrumentaalselt kinnitatud südame fibroelastoosi korral soovitavad arstid rasedus katkestada. Peaaegu kõigil lastel, kelle emad keeldusid meditsiinilisest abordist, leidsid haiguse tunnused kinnitust. Fibroelastoosile iseloomulikud südamepuudulikkuse sümptomid ilmnevad aasta jooksul (harvemini 2.-3. eluaastal). Kombineeritud haiguse vormiga lastel avastatakse südamepuudulikkuse tunnuseid juba esimestel elupäevadel.
Laste kaasasündinud primaarse ja kombineeritud fibroelastoosi vormid kulgevad kõige sagedamini kiiresti koos raske südamepuudulikkuse tekkega. Madal aktiivsus, lapse letargia, imetamisest keeldumine kiire väsimuse tõttu, isutus, suurenenud higistamine viitavad halvale tervisele. Kõik see viib asjaoluni, et laps ei võta hästi kaalus juurde. Imiku nahk on valusalt kahvatu, mõnel sinaka varjundiga, kõige sagedamini nasolabiaalses kolmnurgas.
Esineb nõrga immuunsuse märke, mistõttu sellised lapsed haigestuvad sageli ja kiiresti hingamisteede infektsioonidesse, mis raskendab olukorda. Mõnikord ei esine lapsel esimestel elupäevadel ja -kuudel mingeid vereringehäireid, kuid sagedased infektsioonid ja kopsuhaigused muutuvad südame paispuudulikkuse tekke vallandajaks.
Vastsündinute ja väikelaste, kellel kahtlustati fibroelastoos või kellel oli eelnevalt diagnoositud, täiendavad terviseuuringud näitasid madalat vererõhku (hüpotensiooni), südame suurenemist (kardiomegaalia), südame kuulamisel summutatud toone, mõnikord mitraalklapi puudulikkusele iseloomulikku süstoolset kahinat, tahhükardiat, õhupuudust. Kopsude kuulamisel ilmneb vilistav hingamine, mis viitab ummikutele.
Vasaku vatsakese endokardiaalne kahjustus viib sageli südame lihaskihi (müokardi) nõrgenemiseni. Normaalne südamerütm koosneb kahest rütmiliselt vahelduvast toonist. Fibroelastoosi korral võib ilmneda kolmas (ja mõnikord ka neljas) toon. Selline patoloogiline rütm on selgelt kuuldav ja meenutab oma helilt hobuse kolmetaktilist kõnnakut (galopi), mistõttu seda nimetatakse galopirütmiks.
Teine fibroelastoosi sümptom väikelastel on südame küüru ilmumine. Fakt on see, et lapse ribid varases postnataalses perioodis jäävad luustumata ja on esindatud kõhrekoega. Südame suuruse suurenemine viib selleni, et see hakkab suruma "pehmetele" ribidele, mille tagajärjel need painduvad ja võtavad püsiva ettepoole kaardus kuju (südame küür). Täiskasvanutel fibroelastoosi korral ei teki südame küüru ribide luukoe tugevuse ja jäikuse tõttu isegi siis, kui kõik südame struktuurid on suurenenud.
Südame kühmu teke iseenesest viitab ainult kaasasündinud südamerikkele, täpsustamata selle olemust. Kuid igal juhul on see seotud südame ja selle vatsakeste suuruse suurenemisega.
Laste fibroelastoosiga seotud ödeemi sündroomi diagnoositakse harva, kuid paljudel lastel esineb suurenenud maks, mis hakkab ulatuma keskmiselt 3 cm kaugusele rinnakaare servast.
Kui fibroelastoos on omandatud (näiteks südamemembraanide põletikuliste haiguste tagajärg), on kliiniline pilt enamasti aeglaselt progresseeruv. Mõnda aega võivad sümptomid üldse puududa, seejärel ilmnevad nõrgad südamefunktsiooni häire tunnused füüsilise koormuse ajal tekkiva õhupuuduse, südame löögisageduse tõusu, kiire väsimuse ja madala füüsilise vastupidavuse näol. Veidi hiljem hakkab maks suurenema, ilmnevad tursed ja pearinglus.
Kõik omandatud fibroelastoosi sümptomid on mittespetsiifilised, mis raskendab haiguse diagnoosimist, meenutades kardiomüopaatiat, maksa- ja neeruhaigusi. Haigus diagnoositakse kõige sagedamini raske südamepuudulikkuse staadiumis, mis mõjutab ravi tulemusi negatiivselt.
Tüsistused ja tagajärjed
Tuleb öelda, et südame ja kopsude fibroelastoos on tõsised patoloogiad, mille kulg sõltub erinevatest asjaoludest. Kaasasündinud südamerikked raskendavad olukorda oluliselt, mida saab kirurgiliselt kõrvaldada juba varases eas, kuid samal ajal on endiselt üsna suur surmaoht (umbes 10%).
Arvatakse, et mida varem haigus areneb, seda raskemad on selle tagajärjed. Seda kinnitab asjaolu, et kaasasündinud fibroelastoos kulgeb enamasti äge või ägeda kulguga, millega kaasneb südamepuudulikkuse kiire progresseerumine. Ägeda südamepuudulikkuse teket alla 6 kuu vanusel lapsel peetakse halvaks prognostiliseks märgiks.
Siiski ei garanteeri ravi südamefunktsiooni täielikku taastumist, vaid aeglustab ainult südamepuudulikkuse sümptomite progresseerumist. Teisest küljest aga viib sellise toetava ravi puudumine lapse surmani esimese kahe eluaasta jooksul.
Kui südamepuudulikkus avastatakse beebi elu esimestel päevadel ja kuudel, ei ela laps suure tõenäosusega isegi nädalat. Ravivastus on lastel erinev. Terapeutilise efekti puudumisel pole praktiliselt mingit lootust. Kuid pakutava abi korral on haige lapse eluiga lühike (mitmest kuust mitme aastani).
Fibroelastoosi põhjustanud kaasasündinud südamerikete operatsioon ja korrigeerimine parandavad tavaliselt patsiendi seisundit. Vasaku vatsakese hüperplaasia eduka kirurgilise ravi ja arsti nõuete järgimise korral võib haigus omandada healoomulise kulu: südamepuudulikkusel on krooniline kulg ilma progresseerumise tunnusteta. Kuigi lootus sellisele tulemusele on väike.
Mis puutub südame fibroelastoosi omandatud vormi, siis see muutub kiiresti krooniliseks ja progresseerub järk-järgult. Ravimid võivad protsessi aeglustada, kuid mitte peatada.
Pulmonaalne fibroelastoos, olenemata sellest, millal muutused elundi parenhüümis ja membraanides pärast valgusperioodi ilmnevad, hakkab kiiresti progresseeruma ja tapab inimese paari aasta jooksul, põhjustades rasket hingamispuudulikkust. Kurb on see, et haiguse tõhusaid ravimeetodeid pole veel välja töötatud. [ 7 ]
Diagnostika fibroelastoos
Endomüokardiaalne fibroelastoos, mille sümptomid avastatakse enamasti varases eas, on kaasasündinud haigus. Kui välistada need haruldased juhtumid, mil haigus hakkas arenema hilises lapsepõlves ja täiskasvanueas vigastuste ja somaatiliste haiguste tüsistusena, on võimalik patoloogiat tuvastada sünnieelsel perioodil, st enne lapse sündi.
Arstid usuvad, et fibroelastoosile iseloomulikke endokardi kudede patoloogilisi muutusi, loote südame kuju muutusi ja mõningaid selle toimimise tunnuseid saab määrata juba 14. rasedusnädalal. Kuid see on siiski üsna lühike periood ja ei saa välistada, et haigus võib avalduda mõnevõrra hiljem, raseduse kolmanda trimestri lähedal ja mõnikord paar kuud enne sünnitust. Seetõttu on rasedate naiste jälgimisel soovitatav teha loote südame kliinilisi ultraheliuuringuid mitme nädala tagant.
Milliste tunnuste järgi saavad arstid järgmise ultraheli ajal haigust kahtlustada? Palju sõltub haiguse vormist. Kõige sagedamini diagnoositakse fibroelastoosi vasaku vatsakese piirkonnas, kuid see struktuur ei ole alati suurenenud. Haiguse laienenud vormi, mille korral on südame vasak vatsake suurenenud, on ultraheliuuringul lihtne kindlaks teha südame sfäärilise kuju järgi, mille tippu esindab vasak vatsake, elundi üldise suuruse suurenemise ja vatsakestevahelise vaheseina kumerdumise järgi parema vatsakese suunas. Kuid fibroelastoosi peamine tunnus on endokardi ja südamevaheseinte paksenemine, millele on iseloomulik nende struktuuride ehhogeensuse suurenemine, mis määratakse spetsiifilise ultraheliuuringuga.
Uuring viiakse läbi spetsiaalse ultraheliaparaadi abil koos kardioloogiliste programmidega. Loote ehhokardiograafia ei kahjusta ema ega sündimata last, vaid võimaldab mitte ainult tuvastada südame anatoomilisi muutusi, vaid ka määrata koronaarveresoonte seisundit, verehüüvete olemasolu neis ja südamemembraanide paksuse muutusi.
Loote ehhokardiograafiat määratakse mitte ainult ultraheli tulemuste dekodeerimisel esinevate kõrvalekallete korral, vaid ka ema infektsiooni (eriti viirusliku) korral, tugevate ravimite võtmise, päriliku eelsoodumuse, ainevahetushäirete esinemise ja kaasasündinud südamepatoloogiate korral vanematel lastel.
Loote ehhokardiograafia abil saab tuvastada ka teisi kaasasündinud fibroelastoosi vorme. Näiteks parema vatsakese fibroelastoos, laialt levinud protsess, mille puhul samaaegselt kahjustub vasak vatsake ja sellega külgnevad struktuurid: parem vatsake, südameklapid, kodad, fibroelastoosi kombineeritud vormid, endomüokardiaalne fibroelastoos, millega kaasneb vatsakeste sisemise voodri paksenemine ja osa müokardi kaasamine patoloogilisse protsessi (tavaliselt koos seina tromboosiga).
Sünnieelses eas avastatud endokardiaalne fibroelastoos on väga halva prognoosiga, seega soovitavad arstid sel juhul rasedus katkestada. Vale diagnoosi võimaluse välistab loote südame korduv ultraheliuuring, mis tehakse 4 nädalat pärast esimest patoloogiat paljastanud uuringut. On selge, et lõplik otsus raseduse katkestamise või säilitamise kohta jääb vanematele, kuid nad peavad olema teadlikud, millisesse elusse nad lapse mõistavad.
Endokardi fibroelastoosi ei avastata raseduse ajal alati, eriti arvestades asjaolu, et mitte kõik lapseootel emad ei registreeru naistekliinikus ega läbi ennetavat ultraheli diagnostikat. Lapse haigus tema kõhus ei mõjuta praktiliselt raseda naise seisundit, seega muutub haige lapse sünd sageli ebameeldivaks üllatuseks.
Mõnel juhul saavad nii vanemad kui ka arstid lapse haigusest teada mitu kuud pärast lapse sündi. Sellisel juhul ei pruugi laboratoorsed vereanalüüsid midagi muud näidata kui naatriumikontsentratsiooni suurenemist (hüpernatreemia). Kuid nende tulemused on kasulikud diferentsiaaldiagnostika läbiviimisel põletikuliste haiguste välistamiseks.
Instrumentaalse diagnostika osas on veel lootust. Südame standarduuring (EKG) ei ole fibroelastoosi korral eriti oluline. See aitab tuvastada südame ja südamelihase elektrijuhtivuse häireid, kuid ei täpsusta nende häirete põhjuseid. Seega EKG pinge muutus (nooremas eas on see tavaliselt alahinnatud, vanemas eas - vastupidi, liiga kõrge) viitab kardiomüopaatiale, mis võib olla seotud mitte ainult südamepatoloogiatega, vaid ka ainevahetushäiretega. Tahhükardia on südamehaiguste sümptom. Ja kui mõlemad südamevatsakesed on mõjutatud, võib kardiogramm üldiselt tunduda normaalne. [ 8 ]
Kompuutertomograafia (KT) on suurepärane mitteinvasiivne meetod südame-veresoonkonna kaltsifikatsiooni avastamiseks ja perikardiidi välistamiseks.[ 9 ]
Magnetresonantstomograafia (MRI) võib olla kasulik fibroelastoosi avastamisel, kuna biopsia on invasiivne. Müokardi perfusioonijärjestuse hüpointensiivne äär ja hilinenud kontrastsusega järjestusel hüperintensiivne äär viitavad fibroelastoosile.[ 10 ]
Kuid see ei tähenda, et uuringust tuleks loobuda, sest see aitab kindlaks teha südame töö olemust ja südamepuudulikkuse tekkimise astet.
Kui ilmnevad südamepuudulikkuse sümptomid ja patsient konsulteerib sellega seoses arstiga, määratakse patsiendile ka: rindkere röntgen, südame kompuutertomograafia või magnetresonantstomograafia, ehhokardiograafia (EchoCG). Kahtlastel juhtudel on vaja pöörduda südamekoe biopsia poole koos järgneva histoloogilise uuringuga. Diagnoos on väga tõsine, seega nõuab see diagnoosimisel sama lähenemisviisi, kuigi ravi ei erine palju koronaararterite haiguse ja südamepuudulikkuse sümptomaatilisest ravist.
Kuid isegi selline hoolikas uuring ei ole kasulik, kui selle tulemusi ei kasutata diferentsiaaldiagnostikas. EKG tulemusi saab kasutada ägeda fibroelastoosi eristamiseks idiopaatilisest müokardiidist, eksudatiivsest perikardiidist ja aordistenoosist. Samal ajal ei näita laborikatsed põletiku tunnuseid (leukotsütoos, suurenenud ESR jne) ja temperatuuri mõõtmised ei näita hüpertermiat.
Südame helide ja nurina analüüs, kodade suuruse muutused ja anamneesi uuring aitavad eristada endokardiaalset fibroelastoosi isoleeritud mitraalklapi puudulikkusest ja mitraalklapi defektist.
Anamnestiliste andmete analüüs on kasulik fibroelastoosi ja südame ning aordistenoosi eristamiseks. Aordistenoosi korral tasub pöörata tähelepanu ka siinusrütmi säilimisele ja trombemboolia puudumisele. Südamerütmihäireid ja trombi ladestumist ei täheldata ka eksudatiivse perikardiidi korral, kuid haigus avaldub temperatuuri ja palaviku tõusuna.
Suurim raskus seisneb endokardiaalse fibroelastoosi ja kongestiivse kardiomüopaatia eristamisel. Sellisel juhul on fibroelastoosil, kuigi enamasti ei kaasne sellega väljendunud südamejuhtivuse häireid, raviprognoos ebasoodsam.
Kombineeritud patoloogiate korral on vaja pöörata tähelepanu kõikidele südame tomogrammi või ultraheli käigus ilmnevatele kõrvalekalletele, sest kaasasündinud defektid raskendavad oluliselt fibroelastoosi kulgu. Kui kombineeritud endokardiaalne fibroelastoos avastatakse emakasisese perioodi jooksul, on raseduse säilitamine sobimatu. Palju humaansem on see katkestada.
Kopsu fibroelastoosi diagnoosimine
Kopsufibroelastoosi diagnoosimine nõuab arstilt samuti teatud teadmisi ja oskusi. Tõsiasi on see, et haiguse sümptomid on üsna heterogeensed. Ühelt poolt viitavad need kopsude kongestiivsetele haigustele (mitteproduktiivne köha, õhupuudus) ja teiselt poolt võivad need olla ka südamepatoloogia ilming. Seetõttu ei saa haiguse diagnoosimist taandada ainult sümptomite konstateerimisele ja auskultatsioonile.
Patsiendi vereanalüüsid aitavad välistada põletikulisi kopsuhaigusi, kuid ei anna teavet kudede kvantitatiivsete ja kvalitatiivsete muutuste kohta. Eosinofiilia tunnuste olemasolu aitab eristada haigust kopsufibroosist, mis on ilmingute poolest sarnane, kuid ei lükka ümber ega kinnita fibroelastoosi fakti.
Indikatiivsemaks peetakse instrumentaalseid uuringuid: rindkere röntgenülesvõtet ja hingamisteede tomograafilist uuringut, samuti funktsionaalseid analüüse, mis seisnevad hingamismahtude, kopsude elutähtsa mahutavuse ja elundi rõhu määramises.
Kopsufibroelastoosi korral tasub pöörata tähelepanu spiromeetria ajal mõõdetud välise hingamise funktsiooni langusele. Aktiivsete alveolaarõõnsuste vähenemine mõjutab oluliselt kopsude elutähtsat mahtuvust (VCL) ja sisemiste struktuuride seinte paksenemine mõjutab elundi difusioonivõimet (DCL), mis tagab ventilatsiooni ja gaasivahetusfunktsioonid (lihtsustatult öeldes süsinikdioksiidi neeldumine verest ja hapniku eraldamine).
Pleuroparenhümaalse fibroelastoosi iseloomulikeks tunnusteks on piiratud õhuvoolu kombinatsioon kopsudesse (obstruktsioon) ja kopsu laienemise häire sissehingamisel (piirang), välise hingamisfunktsiooni halvenemine, mõõdukas pulmonaalne hüpertensioon (kopsude rõhu tõus), mis diagnoositakse pooltel patsientidel.
Kopsukoe biopsia näitab iseloomulikke muutusi elundi sisemises struktuuris. Nende hulka kuuluvad: pleura ja parenhüümi fibroos koos alveolaarseinte elastoosiga, lümfotsüütide kogunemine tihendatud alveolaarseinte piirkonnas, fibroblastide muutumine lihaskoeks, mis pole neile tüüpiline, ja tursevedeliku olemasolu.
Tomogramm näitab kopsude kahjustusi ülemistes osades pleura tihenemise fookuste ja parenhüümi struktuurimuutuste näol. Kopsude suurenenud sidekude meenutab värvuse ja omaduste poolest lihaskoe, kuid kopsude maht väheneb. Parenhüümis leidub üsna suuri õhku sisaldavaid õõnsusi (tsüste). Iseloomulikud on bronhide ja bronhioolide pöördumatu fokaalne (või difuusne) laienemine (traktsioonibronhiektaasia) ja diafragma kupli madal asend.
Radioloogilistel uuringutel ilmnevad paljudel patsientidel „lihvklaasi“ ja „kärjekoe“ sarnased piirkonnad, mis viitavad kopsude ebaühtlasele ventilatsioonile kudede tihenemise fookuste tõttu. Ligikaudu pooltel patsientidest on suurenenud lümfisõlmed ja maks.
Kopsufibroelastoosi tuleks eristada parasiitinfektsioonist ja sellega kaasnevast eosinofiiliast põhjustatud fibroosist, endokardiaalsest fibroelastoosist, ventilatsioonihäirete ja "kärgstruktuurilise kopsu" pildiga kopsuhaigustest, autoimmuunhaigusest histikotiidist X (selle kopsukahjustusega patoloogia ühte vormi nimetatakse Hand-Schüller-Christiani tõveks), sarkoidoosi ja kopsutuberkuloosi ilmingutest.
Ravi fibroelastoos
Fibroelastoosi, olenemata selle asukohast, peetakse ohtlikuks ja praktiliselt ravimatuks haiguseks. Patoloogilisi muutusi pleuras ja kopsuparenhüümis ei saa ravimitega taastada. Ja isegi hormonaalsete põletikuvastaste ravimite (kortikosteroidide) kasutamine koos bronhodilataatoritega ei anna soovitud tulemust. Bronhodilataatorid aitavad patsiendi seisundit veidi leevendada, leevendades obstruktiivset sündroomi, kuid need ei mõjuta kopsudes toimuvaid protsesse, seega saab neid kasutada ainult toetava ravina.
Kopsu fibroelastoosi kirurgiline ravi on samuti ebaefektiivne. Ainus operatsioon, mis olukorda muuta võiks, on doonororgani siirdamine. Kuid kopsu siirdamisel on kahjuks sama ebasoodne prognoos. [ 11 ]
Välismaalaste teadlaste sõnul võib fibroelastoosi pidada ka üheks sagedasemaks kopsu- või luuüdi tüvirakkude siirdamise tüsistuseks. Mõlemal juhul tekivad muutused kopsude sidekoe kiududes, mis mõjutavad välise hingamise funktsiooni.
Haigus progresseerub ilma ravita (ja efektiivne ravi praegu puudub) ning umbes 40% patsientidest sureb hingamispuudulikkuse tõttu 1,5–2 aasta jooksul. Ka allesjäänute eluiga on oluliselt piiratud (kuni 10–20 aastat) ja nende töövõime. Inimene muutub puudeks.
Südame fibroelastoosi peetakse samuti meditsiiniliselt ravimatuks haiguseks, eriti kui tegemist on kaasasündinud patoloogiaga. Tavaliselt ei ela lapsed 2-aastaseks. Neid saab päästa ainult südamesiirdamisega, mis iseenesest on keeruline operatsioon, millel on suur risk ja ettearvamatud tagajärjed, eriti nii noores eas.
Mõnedel imikutel on võimalik kaasasündinud südamerikkeid kirurgiliselt korrigeerida, et need ei halvendaks haige lapse seisundit. Arteri stenoosi korral paigaldatakse veresoonte laiendaja - šunt (aortokoronaarne šunt). Südame vasaku vatsakese laienemise korral taastub selle kuju kiiresti. Kuid isegi selline operatsioon ei garanteeri, et laps saab ilma siirdamiseta hakkama. Umbes 20-25% imikutest jääb ellu ja nad kannatavad südamepuudulikkuse all kogu elu ehk neid ei peeta terveks.
Kui haigus on omandatud, tasub lapse elu eest võidelda ravimite abil. Kuid on oluline mõista, et mida varem haigus avaldub, seda raskem on sellega võidelda.
Uimastiravi eesmärk on võidelda südamepuudulikkuse ägenemiste vastu ja neid ennetada. Patsientidele määratakse järgmised südameravimid:
- angiotensiini konverteeriva ensüümi (AKE) inhibiitorid, mis mõjutavad vererõhku ja hoiavad seda normi piires (kaptopriil, enalapriil, benasepriil jne),
- beetablokaatorid, mida kasutatakse südame rütmihäirete, arteriaalse hüpertensiooni raviks ja müokardiinfarkti ennetamiseks (anapriliin, bisoprolool, metoprolool),
- südameglükosiidid, mis pikaajalisel kasutamisel mitte ainult ei toeta südame tööd (suurendavad kardiomüotsüütide kaaliumisisaldust ja parandavad müokardi juhtivust), vaid on võimelised ka mõnevõrra vähendama endokardi paksenemise astet (digoksiin, gitoksiin, strofantiin),
- kaaliumi säästvad diureetikumid (spironolaktoon, veroshpiron, decriz), mis ennetavad kudede turset,
- antitrombootiline ravi antikoagulantidega (cardiomagnyl, magnicor), mis hoiab ära verehüüvete tekke ja vereringehäired koronaarveresoontes.
Endokardiaalse fibroelastoosi kaasasündinud vormis ei soodusta toetav ravi taastumist, kuid vähendab südamepuudulikkuse või trombemboolia tagajärjel suremise riski 70–75% [ 12 ].
Ravimid
Nagu näeme, ei erine endokardiaalse fibroelastoosi ravi praktiliselt südamepuudulikkuse ravist. Mõlemal juhul võtavad kardioloogid arvesse kardiopaatia raskusastet. Ravimite väljakirjutamine on rangelt individuaalne, võttes arvesse patsiendi vanust, kaasuvaid haigusi, südamepuudulikkuse vormi ja astet.
Omandatud endokardiaalse fibroelastoosi ravis kasutatakse 5 rühma ravimeid. Vaatleme igast rühmast ühte ravimit.
"Enalapriil" on AKE inhibiitorite rühma kuuluv ravim, mida toodetakse erinevate annustega tablettide kujul. Ravim suurendab koronaarverevoolu, laiendab artereid, alandab vererõhku, mõjutamata ajuvereringet, aeglustab ja vähendab südame vasaku vatsakese laienemist. Ravim parandab müokardi verevarustust, vähendades isheemia mõju, vähendab veidi vere hüübimist, takistades verehüüvete teket, omab kerget diureetilist toimet.
Südamepuudulikkuse korral määratakse ravim pikemaks ajaks kui kuus kuud või püsivalt. Ravimit alustatakse minimaalse annusega (2,5 mg), suurendades seda järk-järgult 2,5–5 mg kaupa iga 3–4 päeva järel. Püsiv annus on see, mida patsient hästi talub ja mis hoiab vererõhku normi piires.
Maksimaalne ööpäevane annus on 40 mg. Seda võib võtta üks kord või jagada kaheks annuseks.
Kui vererõhk on alla normi, vähendatakse annust järk-järgult. Ravi Enalapriliga ei tohi järsku lõpetada. Soovitatav on võtta säilitusannus 5 mg päevas.
Ravim on ette nähtud täiskasvanud patsientide raviks, kuid seda võib määrata ka lapsele (ohutus ei ole ametlikult kindlaks tehtud, kuid fibroelastoosi korral on kaalul väikese patsiendi elu, seega võetakse arvesse riski suhet). AKE inhibiitorit ei määrata patsientidele, kellel on ravimi komponentide talumatus, porfüüria, rasedus ja imetamise ajal. Kui patsiendil on varem selle rühma ravimite võtmise ajal olnud Quincke ödeem, on enalapriil keelatud.
Ravimi määramisel samaaegsete patoloogiatega patsientidele tuleb olla ettevaatlik: rasked neeru- ja maksahaigused, hüperkaleemia, hüperaldosteronism, aordi- või mitraalklapi stenoos, süsteemsed sidekoe patoloogiad, südame isheemiatõbi, ajuhaigus, suhkurtõbi.
Ravimiga ravimisel ei tohiks dehüdratsiooni ja tugeva hüpotensiivse toime vältimiseks võtta tavapäraseid diureetikume. Samaaegne manustamine kaaliumi säästvate diureetikumidega nõuab annuse kohandamist, kuna on suur hüperkaleemia oht, mis omakorda kutsub esile südame rütmihäireid, krampe, lihastoonuse langust, suurenenud nõrkust jne.
Ravim "Enalapril" on tavaliselt hästi talutav, kuid mõnedel patsientidel võivad esineda kõrvaltoimed. Kõige sagedasemad on: tugev vererõhu langus kuni kollapsini, peavalud ja pearinglus, unehäired, suurenenud väsimus, pöörduv tasakaalu-, kuulmis- ja nägemiskaotus, tinnituse teke, õhupuudus, köha ilma rögaerituseta, muutused vere ja uriini koostises, mis tavaliselt viitavad maksa ja neerude talitlushäiretele. Võimalik: juuste väljalangemine, vähenenud sugutung, "kuumahoogude" sümptomid (soojus- ja südamepekslemistunne, näonaha hüpereemia jne).
"Bisoprolool" on selektiivse toimega beetablokaator, millel on hüpotensiivne ja isheemiavastane toime, mis aitab võidelda tahhükardia ja arütmia ilmingute vastu. Tablettide kujul olev eelarveravim, mis ennetab südamepuudulikkuse progresseerumist endokardiaalse fibroelastoosi korral. [ 13 ]
Nagu paljud teised südame isheemiatõve ja CHF raviks välja kirjutatud ravimid, määratakse bisoprolool pikaajaliseks kasutamiseks. Soovitatav on seda võtta hommikul enne sööki või söögi ajal.
Mis puutub soovituslikesse annustesse, siis need valitakse individuaalselt, olenevalt vererõhu näitudest ja ravimitest, mida selle ravimiga paralleelselt välja kirjutatakse. Keskmiselt on ühekordne (ka päevane) annus 5-10 mg, kuid rõhu kerge tõusuga saab seda vähendada 2,5 mg-ni. Maksimaalne annus, mida saab normaalselt toimivate neerudega patsiendile välja kirjutada, on 20 mg, kuid ainult püsivalt kõrge vererõhu korral.
Näidatud annuste suurendamine on võimalik ainult arsti loal. Kuid raskete maksa- ja neeruhaiguste korral peetakse maksimaalseks lubatud annuseks 10 mg.
Vasaku vatsakese düsfunktsiooni taustal esineva südamepuudulikkuse keerulises ravis, mis esineb kõige sagedamini fibroelastoosiga, valitakse efektiivne annus annuse järkjärgulise suurendamise teel 1,25 mg võrra. Sellisel juhul alustatakse minimaalse võimaliku annusega (1,25 mg). Annust suurendatakse 1-nädalaste intervallidega.
Kui annus jõuab 5 mg-ni, suurendatakse intervalli 28 päevani. 4 nädala pärast suurendatakse annust 2,5 mg võrra. Sellest intervallist ja normist kinni pidades saavutatakse 10 mg, mida patsient peab võtma pikka aega või pidevalt.
Kui selline annus on halvasti talutav, vähendatakse seda järk-järgult mugava tasemeni. Beetablokaatoriga ravi lõpetamine ei tohiks samuti olla järsk.
Ravimit ei tohiks välja kirjutada ülitundlikkuse korral ravimi toimeainete ja abiainete suhtes, ägeda ja dekompenseeritud südamepuudulikkuse, kardiogeense šoki, 2.-3. astme atrioventrikulaarse blokaadi, bradükardia, püsivalt madala vererõhu ja mõnede muude südamepatoloogiate, raske bronhiaalastma, bronhide obstruktsiooni, raskete perifeerse vereringe häirete, metaboolse atsidoosi korral.
Kompleksse ravi määramisel tuleb olla ettevaatlik. Seega ei ole bisoprolooli kombinatsioon mõnede antiarütmikumide (kinidiin, lidokaiin, fenütoiin jne), kaltsiumi antagonistide ja tsentraalse vererõhu alandajate ravimitega soovitatav.
Bisoprolooliga ravi ajal võivad esineda ebameeldivad sümptomid ja häired: suurenenud väsimus, peavalud, kuumahood, unehäired, vererõhu langus ja pearinglus voodist tõustes, kuulmislangus, seedetrakti sümptomid, maksa- ja neeruhäired, potentsi langus, lihasnõrkus ja -krambid. Mõnikord kurdavad patsiendid perifeerse vereringe häirete üle, mis avalduvad temperatuuri languse või jäsemete, eriti sõrmede ja varvaste tuimusena.
Bronhopulmonaalsüsteemi, neerude, maksa ja suhkurtõve samaaegsete haiguste esinemisel on kõrvaltoimete risk suurem, mis näitab haiguse ägenemist.
"Digoksiin" on populaarne eelarvesõbralik südameglükosiid, mis põhineb sõrmkübara taimel ja mida väljastatakse rangelt retsepti alusel (tablettidena) ning mida tuleks kasutada tema järelevalve all. Süstimisravi viiakse läbi haiglas südame isheemiatõve ja südame paispuudulikkuse ägenemise ajal, tablette määratakse pidevalt minimaalselt efektiivsetes annustes, kuna ravimil on toksiline ja narkootiline toime.
Terapeutiline toime seisneb müokardi kokkutõmmete tugevuse ja amplituudi muutmises (annab südamele energiat, toetab seda isheemilistes tingimustes). Ravimil on ka vasodilateeriv (vähendab ummikuid) ja teatav diureetiline toime, mis aitab leevendada turset ja vähendada hingamispuudulikkuse raskust, mis avaldub õhupuudusena.
Digoksiini ja teiste südameglükosiidide oht seisneb selles, et üleannustamise korral võivad need esile kutsuda südame rütmihäireid, mis on põhjustatud müokardi suurenenud erutuvusest.
Südamepuudulikkuse ägenemise korral määratakse ravim süstide kujul, valides individuaalse annuse, võttes arvesse seisundi raskust ja patsiendi vanust. Kui seisund stabiliseerub, lähevad nad üle tablettidele.
Tavaliselt on ravimi standardne ühekordne annus 0,25 mg. Manustamise sagedus võib varieeruda 1 kuni 5 korda päevas võrdsete intervallidega. CHF ägedas staadiumis võib päevane annus ulatuda 1,25 mg-ni, kui seisund stabiliseerub püsivalt, on vaja võtta säilitusannus 0,25 (harvemini 0,5) mg päevas.
Ravimi määramisel lastele võetakse arvesse patsiendi kehakaalu. Efektiivne ja ohutu annus arvutatakse 0,05–0,08 mg kehakaalu kilogrammi kohta. Kuid ravimit ei määrata pidevalt, vaid 1–7 päeva jooksul.
Südameglükosiidi annust peaks määrama arst, võttes arvesse patsiendi seisundit ja vanust. Samal ajal on väga ohtlik annuseid iseseisvalt reguleerida või võtta samaaegselt kahte sellist toimet omavat ravimit.
"Digoksiini" ei ole ette nähtud ebastabiilse stenokardia, raskete südame rütmihäirete, 2.-3. astme AV-blokaadi, südametamponaadi, Adams-Stokes-Morgagni sündroomi, isoleeritud bikuspidaalklapi stenoosi ja aordistenoosi, kaasasündinud südameanomaalia, mida nimetatakse Wolff-Parkinson-White'i sündroomiks, hüpertroofilise obstruktiivse kardiomüopaatia, endo-, peri- ja müokardiidi, rindkere aordi aneurüsmi, hüperkaltseemia, hüpokaleemia ja mõnede teiste patoloogiate korral. Vastunäidustuste loetelu on üsna suur ja hõlmab sündroome, millel on mitu ilmingut, seega saab otsuse selle ravimi kasutamise võimalikkuse kohta teha ainult spetsialist.
Digoksiinil on ka kõrvaltoimeid. Nende hulka kuuluvad südame rütmihäired (valesti valitud annuse ja üleannustamise tagajärjel), isutus, iiveldus (sageli koos oksendamisega), soolehäired, tugev nõrkus ja suur väsimus, peavalud, "kärbeste" ilmumine silmade ette, trombotsüütide arvu vähenemine ja vere hüübimishäired, allergilised reaktsioonid. Enamasti on nende ja teiste sümptomite ilmnemine seotud ravimi suurte annuste võtmisega, harvemini pikaajalise raviga.
"Spironolaktoon" on mineralokortikoidide antagonist. Sellel on diureetiline toime, mis soodustab naatriumi, kloori ja vee eritumist, kuid säilitab kaaliumi, mis on vajalik südame normaalseks toimimiseks, kuna selle juhtivusfunktsioon põhineb peamiselt sellel elemendil. See aitab leevendada turseid. Seda kasutatakse südame paispuudulikkuse abiainena.
Südamepuudulikkuse korral määratakse ravim sõltuvalt haiguse faasist. Ägenemise korral võib ravimit välja kirjutada nii süstide kui ka tablettide kujul annuses 50–100 mg päevas. Kui seisund stabiliseerub, määratakse pikaajaline säilitusannus 25–50 mg. Kui kaaliumi ja naatriumi tasakaal on häiritud esimese vähenemise suunas, võib annust suurendada, kuni mikroelementide normaalne kontsentratsioon saavutatakse.
Pediaatrias arvutatakse efektiivne annus suhtega 1-3 mg spironolaktooni patsiendi kehakaalu kilogrammi kohta.
Nagu näeme, on ka siin soovitatava annuse valik individuaalne, nagu ka paljude teiste kardioloogias kasutatavate ravimite väljakirjutamisel.
Diureetikumi kasutamise vastunäidustused võivad olla: liigne kaaliumi- või madal naatriumisisaldus organismis, urineerimise puudumisega seotud patoloogia (anuuria), raske neeruhaigus koos halvenenud sooritusvõimega. Ravimit ei ole ette nähtud rasedatele ja imetavatele emadele, samuti neile, kellel on ravimi komponentide talumatus.
Ravimi kasutamisel tuleb olla ettevaatlik patsientidel, kellel on AV-südameblokaad (võib süveneda), liigne kaltsium (hüperkaltseemia), metaboolne atsidoos, suhkurtõbi, menstruaaltsükli häired ja maksahaigus.
Ravimi võtmine võib põhjustada peavalu, unisust, tasakaalu ja liigutuste koordinatsiooni kaotust (ataksiat), piimanäärmete suurenemist meestel (günekomastia) ja impotentsust, menstruatsiooni iseloomu muutusi, hääle karedust ja liigset karvakasvu naistel (hirsutismi), valu ülakõhus ja seedetrakti häireid, soolekoolikke, neerufunktsiooni häireid ja mineraalide tasakaaluhäireid. Võimalikud on naha- ja allergilised reaktsioonid.
Kõrvaltoimeid täheldatakse tavaliselt vajaliku annuse ületamisel. Ebapiisava annuse korral võib tekkida turse.
"Magnicor" on atsetüülsalitsüülhappel ja magneesiumhüdroksiidil põhinev ravim, mis hoiab ära verehüüvete tekke. See on üks südamepuudulikkuse korral välja kirjutatud tõhusamaid tromboosivastaseid ravimeid. Sellel on valuvaigistav, põletikuvastane ja trombotsüütidevastane toime ning see mõjutab hingamisfunktsiooni. Magneesiumhüdroksiid vähendab atsetüülsalitsüülhappe negatiivset mõju seedetrakti limaskestale.
Endomüokardiaalse fibroelastoosi korral määratakse ravim profülaktilistel eesmärkidel, seega järgitakse minimaalset efektiivset annust - 75 mg, mis vastab 1 tabletile. Trombi moodustumise ja sellele järgneva koronaarveresoonte valendiku ahenemise tõttu tekkinud südameisheemia korral on algannus 2 tabletti ja säilitusannus vastab profülaktilisele annusele.
Soovitatava annuse ületamine suurendab oluliselt raskesti peatatava verejooksu riski.
Annused on näidustatud täiskasvanud patsientidele, kuna ravim sisaldab atsetüülsalitsüülhapet, mille kasutamine alla 15-aastastel lastel võib põhjustada tõsiseid tagajärgi.
Ravimit ei ole ette nähtud lapsepõlves ja varases noorukieas patsientidele, atsetüülsalitsüülhappe ja teiste ravimi komponentide talumatuse, aspiriinist tingitud astma (anamneesis), ägeda erosioonilise gastriidi, peptilise haavandi, hemorraagilise diateesi, raskete maksa- ja neeruhaiguste ning raske dekompenseeritud südamepuudulikkuse korral.
Raseduse ajal määratakse Magnicori ainult äärmise vajaduse korral ja ainult 1.-2. trimestril, võttes arvesse võimalikku negatiivset mõju lootele ja raseduse kulule. Raseduse 3. trimestril on selline ravi ebasoovitav, kuna see aitab kaasa emaka kontraktiilsuse vähenemisele (pikaajaline sünnitus) ja võib põhjustada tugevat verejooksu. Lootel võib esineda kopsuhüpertensioon ja neerufunktsiooni häire.
Ravimi kõrvaltoimete hulka kuuluvad seedetrakti sümptomid (düspepsia, epigastriline ja kõhuvalu, mao verejooksu oht koos rauavaegusaneemia tekkega). Ravimi võtmise taustal on võimalik ninaverejooks, igemete veritsus ja kuseteede organite verejooks.
Üleannustamine võib põhjustada pearinglust, minestust ja tinnitus. Allergilised reaktsioonid ei ole haruldased, eriti salitsülaatide suhtes ülitundlikkuse korral. Anafülaksia ja hingamispuudulikkus on aga haruldased kõrvaltoimed.
Kompleksses ravis kasutatavate ravimite valik ja soovitatavad annused peaksid olema rangelt individuaalsed. Eriti ettevaatlik tuleb olla rasedate, imetavate emade, laste ja eakate patsientide ravis.
Traditsiooniline meditsiin ja homöopaatia
Südame fibroelastoos on tõsine ja raske haigus, millel on iseloomulik progresseeruv kulg ja praktiliselt puudub taastumisvõimalus. On selge, et sellise haiguse efektiivne ravi rahvapäraste ravimitega on võimatu. Traditsioonilise meditsiini retsepte, mis taanduvad peamiselt taimsele ravile, saab kasutada ainult abivahendina ja ainult arsti loal, et mitte niigi halba prognoosi keerulisemaks muuta.
Mis puutub homöopaatilistesse ravimitesse, siis nende kasutamine ei ole keelatud ja see võib olla osa südamepuudulikkuse terviklikust ravist. Kuid antud juhul ei räägi me niivõrd ravist, kuivõrd südamepuudulikkuse progresseerumise ennetamisest.
Ravimeid peaks määrama kogenud homöopaat ja küsimus nende kaasamise võimalusest kompleksravisse kuulub raviarsti pädevusse.
Millised homöopaatilised ravimid aitavad fibroelastoosi korral südamepuudulikkuse progresseerumist edasi lükata? Ägeda südamepuudulikkuse korral pöörduvad homöopaadid järgmiste ravimite poole: Arsenicum album, Antimonium tartaricum, Carbo vegetabilis, Acidum oxalicum. Vaatamata näidustuste sarnasusele tuginevad arstid efektiivse ravimi valimisel isheemia välistele ilmingutele tsüanoosi kujul (selle aste ja levimus) ning valusündroomi iseloomule.
Südamepuudulikkuse korral võib säilitusravi hulka kuuluda järgmised ravimid: Lachesis ja Nayu, Lycopus (südame suurenemise algstaadiumis), Laurocerasus (õhupuuduse korral puhkeolekus), Latrodectus mactans (klapipatoloogiate korral), viirpuupreparaadid (eriti kasulikud endomüokardi kahjustuste korral).
Tugeva südamelöögi korral võib sümptomaatiliseks raviks määrata järgmist: Spigelia, Glonoinum (tahhükardia korral), Aurum metallicum (hüpertensiooni korral).
Õhupuuduse raskuse vähendamiseks aitavad järgmised taimed: Grindelia, Spongia ja Lahegis. Südamevalu leevendamiseks võib välja kirjutada järgmisi taimesid: Cactus, Cereus, Naya, Cuprum, ärevuse leevendamiseks sellel taustal - Aconitum. Südameastma tekke korral on näidustatud järgmised taimed: Digitalis, Laurocerasus, Lycopus.
Ärahoidmine
Südame ja kopsude omandatud fibroelastoosi ennetamine seisneb nakkus- ja põletikuliste haiguste ennetamises ja õigeaegses ravis, eriti kui tegemist on elutähtsate organite kahjustusega. Põhihaiguse efektiivne ravi aitab vältida ohtlikke tagajärgi, mille hulka kuulub ka fibroelastoosi. See on suurepärane põhjus, miks hoolitseda oma ja tulevaste põlvkondade tervise eest, teha nn tööd terve tuleviku ja pikaealisuse nimel.
Prognoos
Südame- ja kopsufibroelastoosiga seotud sidekoe muutusi peetakse pöördumatuteks. Kuigi mõned ravimid võivad pikaajalise ravi korral endokardi paksust mõnevõrra vähendada, ei garanteeri need tervenemist. Kuigi seisund ei ole alati surmav, on prognoos siiski suhteliselt halb. Nelja-aastane elulemus on 77%. [ 14 ]
Nagu juba mainitud, on halvim prognoos kaasasündinud südame fibroelastoosi korral, mille südamepuudulikkuse ilmingud on nähtavad juba lapse elu esimestel nädalatel ja kuudel. Ainult südamesiirdamine saab last päästa, mis iseenesest on nii varases perioodis riskantne operatsioon ja see tuleb teha enne 2. eluaastat. Sellised lapsed tavaliselt kauem ei ela.
Teised operatsioonid aitavad vältida lapse varajast surma (ja mitte alati), kuid ei suuda teda südamepuudulikkusest täielikult ravida. Surm saabub dekompensatsiooni ja hingamispuudulikkuse tekkega.
Kopsufibroelastoosi prognoos sõltub haiguse omadustest. Kui sümptomid arenevad kiiresti, on tõenäosus äärmiselt väike. Kui haigus progresseerub järk-järgult, võib patsient elada umbes 10-20 aastat, kuni tekib hingamispuudulikkus kopsude alveoolide muutuste tõttu.
Ennetavate meetmete abil saab vältida paljusid raskesti ravitavaid patoloogiaid. Südame fibroelastoosi puhul on see ennekõike nende tegurite ennetamine, mis võivad mõjutada loote südame ja vereringesüsteemi arengut (välja arvatud pärilik eelsoodumus ja mutatsioonid, mille vastu arstid on võimetud). Kui neid ei ole võimalik vältida, aitab varajane diagnostika patoloogiat tuvastada staadiumis, kus raseduse katkestamine on võimalik, mida selles olukorras peetakse humaanseks.

