Artikli meditsiiniline ekspert
Uued väljaanded
Follikulaarne lümfoom
Last reviewed: 05.07.2025

Kõik iLive'i sisu vaadatakse meditsiiniliselt läbi või seda kontrollitakse, et tagada võimalikult suur faktiline täpsus.
Meil on ranged allhanke juhised ja link ainult mainekate meediakanalite, akadeemiliste teadusasutuste ja võimaluse korral meditsiiniliselt vastastikuste eksperthinnangutega. Pange tähele, et sulgudes ([1], [2] jne) olevad numbrid on nende uuringute linkideks.
Kui tunnete, et mõni meie sisu on ebatäpne, aegunud või muul viisil küsitav, valige see ja vajutage Ctrl + Enter.
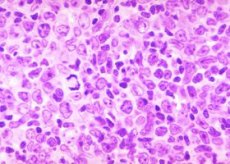
Diagnoos on follikulaarne lümfoom. Selline esmapilgul arusaamatu ja hirmutav haigus kuulub pahaloomuliste kasvajatega seotud kõige leebemate ja suhteliselt ohutumate patoloogiate kategooriasse. Samal ajal on meeldiv see, et kõnealune patoloogia allub hästi keerulisele medikamentoossele ravile ja on seetõttu ravitav.
Põhjused follikulaarne lümfoom
Kohe tasub mainida, et liigseks rõõmustamiseks pole põhjust. Kaasaegne meditsiin pole veel suutnud täielikku remissiooni saavutada. Seda ei saa oodata isegi siis, kui kirurgiline ravi läks hästi ja kasvaja eemaldati täielikult. Isegi sellise ravi tulemuse korral taastub haigus tavaliselt kolme aasta pärast, parimal juhul viie aasta pärast.
Kõnealune haigus sai selle terminoloogia, sest enamasti hakkas pahaloomuline kasvaja tekkima ja arenema epidermise katterakkudes, muutes patoloogiliselt juuksefolliikuleid ehk nagu neid nimetatakse ka folliikuliteks.
Praeguseks ei võta ükski onkoloog ette kõiki follikulaarse lümfoomi põhjuseid nimetada, kuna selle olemust pole veel täielikult uuritud. Saame vaid öelda, et üks rakkude patoloogilist degeneratsiooni provotseerivatest allikatest on geenimutatsioonid. Kuid mis oli nende metamorfooside katalüsaatoriks - see küsimus jääb esialgu lahtiseks.
Siiski võib nimetada mitmeid põhjuseid, mida arstid on suutnud kindlaks teha:
- Elundite siirdamisega seotud kirurgiline sekkumine.
- Endoproteesimine on operatsioon, mille käigus asendatakse liiges implantaatidega.
- Teatud farmakoloogiliste ainete, näiteks immunosupressantide pikaajaline kasutamine.
- Kaasasündinud kromosomaalne anomaalia, kuid sellest üksi ei piisa follikulaarse lümfoomi tekke vallandamiseks. Selleks peavad patoloogiaga kaasnema ka muud tegurid. Näiteks võib see olla trisoomia ja/või monosoomia, mis on samuti seotud geneetiliste kõrvalekalletega.
- Erinevad autoimmuunhaigused.
- Pestitsiididega töötamisel on tegemist üsna tiheda kontaktiga, mis on tänapäeval inimtegevuse põllumajandussektoris peaaegu vältimatu.
- Halbade harjumuste olemasolu inimesel. See kehtib eriti nikotiini kohta.
- Ioniseeriva kiirguse doosi saamise tagajärjel.
- Igasugune kokkupuude mürgiste keemiliste ühendite, kantserogeensete ainetega.
- Kõnealuse haiguse tekkerisk suureneb, kui inimesed elavad ökoloogiliselt saastunud piirkonnas. See võib olla suurlinn suurte tööstusrajatistega. Või näiteks inimesed, kes elavad keemiatehase ohtlikus läheduses.
- Omandatud või kaasasündinud haigus, mis mõjutab inimese immuunsüsteemi.
Sümptomid follikulaarne lümfoom
Kõnealuse haiguse lokaliseerimise kõige levinumad piirkonnad on: kaenlaalused, kubemepiirkond, inimese pea ja kael. Kummalisel kombel esineb see haigus peamiselt noortel, kes kuuluvad vanusekategooriasse kuni nelikümmend aastat.
Selle patoloogia, nagu ka teiste onkoloogiliste haiguste salakavalus seisneb selles, et selle progresseerumise algstaadiumis ei häiri patsienti miski ja haigust saab diagnoosida ainult juhuslikult, rutiinse ennetava uuringu käigus või uuringute käigus, mis määrati seoses teise haiguse raviga.
Kui kasvaja jätkab progresseerumist, saab seda palpatsiooni teel ära tunda. Hiljem hakkavad ilmnema follikulaarse lümfoomi sümptomid:
- Pahaloomuline moodustis võib ulatuda nahapinnast kõrgemale.
- "Tursel" on selged piirjooned.
- Neoplasmi värvus võib olla kergelt roosakas või lilla-punane.
- Suurenenud tihedusega aine.
- Kasvaja asukohas ilmnevad valulikud aistingud.
- Neoplasm on võimeline veritsema.
- Epidermis muutub haavandiliseks.
- Patsient hakkab tundma nõrkust kogu kehas.
- Lümfisõlmede põletiku (nakkushaigusest) erinevus seisneb selles, et need pole mitte ainult valusad, vaid ka antibiootikumide suhtes tundlikud.
- Suurenenud higi tootmine vastavate näärmete poolt.
- Arstid täheldavad kromosomaalset translokatsiooni t(14:18).
- Võib täheldada kehatemperatuuri tõusu.
- Inimene hakkab ilma igasuguse põhjuseta kaalust alla võtma.
- Ilmnevad probleemid seedetraktiga.
- Vähenenud jõudlus.
- Iiveldus.
- Võib esineda täiskõhutunnet kõhus, survetunnet näos või kaelas, hingamisraskusi. See võib olla tingitud suurenenud survest seedeorganitele põrnast, maksast või otse lümfisõlmest (kasvaja teatud lokaliseerimise korral) või teistele inimkeha organitele.
- Pearinglus, isegi minestamiseni.
- Sõltuvalt asukohast võib patsiendil olla probleeme neelamisega, mis on seotud neelu lümfirõnga mahu suurenemisega.
- Palavik võib ilmneda ilma nähtava põhjuseta.
- Kuulmislangus.
Väärib märkimist, et sümptomid, olenevalt kahjustatud lümfisõlme asukohast, võivad kombineerida erinevaid ilminguid eespool loetletud ilmingutest.
Mõnikord saab seda haigust avastada ja diagnoosida alles siis, kui pahaloomuline protsess hakkab mõjutama luuüdi. Hea on see, et asümptomaatiline lümfoom on üsna haruldane.
Mitte-Hodgkini follikulaarne lümfoom
Follikulaarne lümfoom ise kuulub meditsiinilise klassifikatsiooni kohaselt mitte-Hodgkini tüüpi. Nii kurb kui see ka ei kõla, suudab tänapäeva meditsiin haigust varajases staadiumis ära tunda vaid mõnel juhul. 70% juhtudest pöördub patsient spetsialisti poole, kui algavad haiguse ilmingud. Näiteks sagedane iiveldus ja inimene hakkab minestama. See on tingitud asjaolust, et häired on juba luuüdi haaranud.
Sageli diagnoositakse mitte-Hodgkini follikulaarne lümfoom varajases arengujärgus põhjaliku tervisekontrolli käigus, kasutades kaasaegseid ülitäpseid diagnostikaseadmeid. Just sellega seoses nõuavad arstid, et inimene läbiks vähemalt kord aastas täieliku ennetava läbivaatuse. Selline lähenemine oma tervisele vähendab oluliselt inimkeha täieliku kahjustuse ja pöördumatute patoloogiliste muutuste ohtu.
Mitte-Hodgkini lümfoomid on põhjustatud B- ja T-rakutüübi vähkkasvajatest. Sellise patoloogia allikas võib pärineda mis tahes lümfisõlmest või muust organist ja seejärel lümfi "nakatada". Seejärel toimub metastaas kolmel viisil: hematogeenne, lümfogeenne, hematogeen-lümfogeenne.
Sellistel lümfoomidel on oma kvalifikatsioon, mis erineb morfoloogia, kliiniliste sümptomite ja ka haiguse parameetrite poolest. Sõltuvalt lokaliseerimise piirkonnast eristavad arstid lümfoome - primaarse päritoluga vähkkasvajaid, mis mõjutavad lümfoidkihte ja ei mõjuta luuüdi, ning leukeemiaid - vähkkasvajaid, mis mõjutavad peamiselt luuüdi kihte.
Kõik elanikkonna vanusekategooriad on selle haiguse suhtes vastuvõtlikud, kuid suurem protsent langeb siiski inimestele, kes on juba 60-aastaseks saanud.
Lümfosarkoomide etioloogia ei ole tänaseni täielikult teada. Seetõttu on haiguse esilekutsumise põhjuste käsitlemisel vaja rääkida aspektidest, mis suurendavad selle tekkimise ja arengu riski. Nende hulka kuuluvad:
- Viiruslikud patoloogiad. Näiteks AIDS, Epsteini-Barri viirus, hepatiit, eriti C-hepatiit.
- Helicobacter pylori nakkav kahjustus, mis, nagu mõned teadlased usuvad, on seedetrakti limaskesta haavandiliste kahjustuste "süüdlane".
- Kaasasündinud või omandatud immuunpuudulikkus võib suurendada haiguse tekkimise tõenäosust.
- Ja muud juba eespool mainitud põhjused.
Mitte-Hodgkini follikulaarse lümfoomi tüübil on oma üsna ulatuslik klassifikatsioon:
Lümfisõlmedes lokaliseeritud lümfisarkoomi nimetatakse sõlmelisteks, muude lokaliseerimiste (süljenäärmed, mandlid, kilpnääre, epidermis, aju, kopsud jne) korral - ekstranodaalseteks. Follikulaarse (nodulaarse) ehk difuusse moodustab kasvaja struktuurikomponent.
Samuti on olemas jaotus vastavalt haiguse kiirusele:
- Indolentne - progresseerumine on sujuv. Ilma ravita võib selline patsient elada seitse kuni kümme aastat. Ravi annab üsna soodsa prognoosi.
- Haiguse agressiivne ja väga agressiivne kulg. Ilma meditsiinilise ravita võib selline patsient elada mitu kuud kuni poolteist kuni kaks. Ravi annab üsna soodsa prognoosi.
Tänapäeval on onkoloogias üle 30 erineva mitte-Hodgkini lümfoomi tüübi. Enamik neist (umbes 85%) on B-rakulised lümfoomid (B-lümfotsütoomid) ja ülejäänud 15% on T-rakulised lümfoomid (T-lümfotsütoomid). Igal neist tüüpidest on oma alatüübid.
B-rakkude follikulaarne lümfoom
Seda tüüpi haigus domineerib haiguse diagnoosimisel selgelt. Lastel seda tüüpi lümfisüsteemi häiret peaaegu kunagi ei kohta.
Arstid liigitavad B-rakulise lümfoomi järgmiselt:
- Difuusne suurerakuline B-rakuline lümfoom on haiguse kõige levinum tüüp. 31% diagnoositud mitte-Hodgkini lümfoomidest on seda tüüpi. Haiguse peamised parameetrid on agressiivsus ja kõrge progresseerumiskiirus. Kuid hoolimata sellistest negatiivsetest omadustest on õigeaegse meditsiinilise sekkumise korral täielikuks paranemiseks head eeldused.
- Rakulise follikulaarse lümfoomi korral on selle tüübi diagnoosimise tase 22 juhtu sajast tuvastatud mitte-Hodgkini lümfoomist. Patoloogia kulg on indolentne, kuid on juhtumeid, kus kulg muutub ja omandab agressiivse difuusse vormi. Onkoloogidel on selline kriteerium nagu viieaastane elulemus. Seega näitab see haiguse kategooria, et 60–70 inimest sajast elavad selle viieaastase perioodi jooksul. 30–50% sellise diagnoosiga patsientidest suudavad ületada kümne aasta piiri. Sellel tüübil on sekundaarse folliikuli tunnused. Rakk hõlmab tsentrotsüüte ja tsentroblaste. Seda tüüpi patoloogia jaguneb rakulise koostise järgi kolmeks tsütoloogiliseks tüübiks. Rakulise koostise järgi eristatakse follikulaarse lümfoomi III tsütoloogilist tüüpi.
- Marginaalseid rakke mõjutavad B-rakulised lümfoomid – diagnoosimise protsent ei ole kõrge. Need ei ole agressiivsed ja neil on aeglane kasvukiirus. Varajases staadiumis avastatuna reageerivad nad ravile hästi.
- Mantelrakuline lümfoom - see patoloogia moodustab umbes 6% juhtudest. Haigus on üsna spetsiifiline. Ainult viiendik haigestunutest elab üle viie aasta.
- Väikerakuline lümfotsütaarne lümfoom ja krooniline lümfotsütaarne leukeemia – umbes 7% patsientidest on sellele haigusele vastuvõtlikud. Seda tüüpi patoloogia sarnaneb mitte-Hodgkini lümfoomiga. See ei ole eriti agressiivne, kuid on kasvajavastase ravi suhtes vähetundlik.
- B-rakuline mediastinaalne lümfoom – diagnoosimise sagedus on 2%. Enamasti diagnoositakse 30–40-aastastel naistel. Ainult pooled patsientidest on ravitavad.
- Burkitti lümfoom – esinemissagedus on umbes kaks protsenti. Haiguse kulg on agressiivne, kuid intensiivravi abil on võimalik saavutada täielik taastumine (50% patsientidest).
- Waldenströmi makroglobulineemia - ainult 1% juhtudest. See viib verevedeliku viskoossuse suurenemiseni, mis omakorda põhjustab tromboosi ja veresoonte terviklikkuse häireid. Sellise haigusega võib inimene elada nii 20 aastat kui ka vähem kui aasta.
- Karvrakuline leukeemia on üsna haruldane ja mõjutab vanemaid inimesi.
- Kesknärvisüsteemi lümfoom – kahjustuse allikaks on kesknärvisüsteem, mille järel hakkavad metastaasid mõjutama luu- ja ajurakke. Ainult 30% patsientidest elab viis aastat.
Follikulaarse lümfoomi 2. tüüpi tsütoloogiline uuring
Üks peamisi kriteeriume diagnoosi panemisel ja keemiaravi õigel määramisel on histoloogilise analüüsi tulemus. Praktikud on kinnitanud vajadust jagada kõnealune haigus tsütoloogilisteks tüüpideks (morfoloogilise põhimõtte järgi), olenevalt patsiendi kehas määratud suurte rakkude arvust.
Onkoloogid eristavad:
- 1 tsütoloogiline tüüp – väikeste lõhenenud rakkude olemasolu.
- Tsütoloogiliselt on follikulaarne lümfoom 2. tüüpi suurte ja väikeste rakkude kogum, mis on morfoloogiliselt üksteisega võrreldavad.
- 3 tsütoloogilist tüüpi - suured folliikulite rakud.
Korduva biopsia korral võib täheldada esimese tüübi muundumist teiseks, kuid mitte kunagi kolmandaks.
Tüübi diagnoosimisel tuginevad arstid tsütoloogilise uuringu tulemustele. Sellest lähtuvalt määravad onkoloogid tüübi (sõltuvalt mikroskoobi vaateväljas määratud tsentroblastide arvust):
- Tüüp 1 – nullist viieni.
- Tüüp 2 – 6 kuni 15.
- Tüüp 3 – rohkem kui 15. See tüüp jaguneb:
- Alatüübi 3-a puhul on tsentrotsüüte juba nägemisväljas täheldatud.
- Alatüübi 3-b korral moodustavad tsentroblastid ulatuslikke moodustisi ilma tsentrotsüütideta.
II tsütoloogilist tüüpi vähkkasvajad on progresseerumisel üsna agressiivsed ja vajavad radikaalsemaid keemiaravi meetmeid. Kuid kõigi tsütoloogiliste rühmade patsientide elulemus on üldiselt ligikaudu sama.
Follikulaarne lümfoom 3a tsütoloogiline tüüp
Kui patsiendil diagnoositakse tsütoloogilist tüüpi 3a follikulaarne lümfoom, on selle inimese prognoos väga ebasoodne. Selle patoloogiaga patsientidel, isegi pärast täielikku läbivaatust ja kvaliteetset piisavat ravi, täheldatakse haiguse ägenemise korduvaid märke palju sagedamini ja varem kui teistel (1. või 2. tüüpi follikulaarse lümfoomi korral).
Seda prognoosi saab mõnevõrra parandada, kui sellise patsiendi raviprotokolli lisada doksorubitsiinravi. Ja tsentrotsüütide olemasolu vaateväljas on onkoloogidele põhjuseks määrata patsiendile oluliselt agressiivne ravi. Tüüp 3a (tsütoloogiline klassifikatsioon) - see staadium määratakse siis, kui pahaloomulise protsessi levik mõjutab ühte või kahte kauget lümfisõlme.
Sellistel patsientidel, keda iseloomustab varajaste ägenemiste kõige tõenäolisem esinemine, on ka viieaastane elulemus suurem.
Diagnostika follikulaarne lümfoom
Isegi vähimagi onkoloogilise probleemi kahtluse korral suunab kohalik arst-terapeut oma patsiendi spetsialiseeritud onkoloogia dispanserisse, kus ta läbib vajaliku läbivaatuse. Follikulaarse lümfoomi diagnoosimise viib läbi kitsamalt spetsialiseeritud spetsialist - onkohematoloog.
Uuringu näidustused on mitmed kriteeriumid, mis määravad patoloogilise kliinilise pildi: ühe või mitme lümfisõlme mahu kasv, patsiendi kehas ilmsete joobeseisundi (süsteemse mürgistuse) tunnuste ilmnemine, ekstranodaalsed muutused.
Õige diagnoosi seadmiseks, mis viitab mitte-Hodgkini lümfoomile, peab onkoloog võtma uurimiseks kasvaja rakulise substraadi proovi. Selleks ja inimese tervisest täielikuma pildi saamiseks on ette nähtud nii instrumentaalsed meetodid kui ka laboratoorsed testid:
- Vastuvõetud patsiendi väline läbivaatus.
- Lümfisõlmede palpatsioon, mis võimaldab spetsialistil hinnata kasvaja mahtu ja tihedust. Kuid kõiki kasvajaid ei saa sel viisil uurida. Seetõttu on põhjalik uuring hädavajalik.
- Mõjutatud lümfisõlme biopsia tehakse.
- Laparoskoopia on kõhuõõne organite terapeutiline või diagnostiline uuring.
- Torakoskoopia on pleuraõõne endoskoopiline uurimine.
- Võetakse luuüdi punktsioon - see analüüs võimaldab meil välistada või kinnitada metastaaside olemasolu antud kehapiirkonnas.
Pärast ülalmainitud meetmete rakendamist saadetakse rakuline materjal edasiseks uurimiseks. Tehakse järgmised uuringud:
- Immunohistokeemia on meetod, mis võimaldab täpselt määrata konkreetse rakulise või koekomponendi (antigeeni) asukohta, sidudes selle märgistatud antikehadega.
- Tsütoloogiline uuring on rakkude struktuuriliste tunnuste, inimkeha organite, kudede ja vedelike rakulise koostise uuring mitmesuguste haiguste diagnoosimiseks suurendusseadmete abil.
- Tsütogeneetiline – inimese kromosoomide mikroskoopiline uurimine, meetodite kogum, mis seob pärilikke häireid rakkude struktuuriga (eriti rakutuuma struktuuriga).
- Muud uuringud.
Follikulaarse lümfoomi ravimeetmete protokolli määramise käigus määrab arst ka muid täiendavaid uuringuid kasvaja asukoha ja metastaaside ulatuse kindlakstegemiseks:
- Kahtlustatava kahjustatud piirkonna röntgenülesvõte.
- Lümfisõlmede, kilpnäärme ja piimanäärmete, maksa, põrna, munandikoti ja teiste organite ultraheliuuring.
- Kõhukelme ja rindkere kompuutertomograafia, mis võimaldab tuvastada isegi kõige väiksemaid struktuurilisi kõrvalekaldeid.
- Lümfoskintigraafia on meetod, mis võimaldab saada lümfisoonte pildi.
- Luude ja siseorganite stsintigraafia - metastaatiliste pahaloomuliste kasvajate diagnostika.
- Magnetresonantstomograafia (MRI) on meetod vähkkasvajate primaarsete ja metastaatiliste fookuste visuaalseks tuvastamiseks.
- Üldine ja biokeemiline vereanalüüs.
Kui uuringu käigus avastatakse peenelt hajutatud rakulisi ühekordseid struktuure, paneb onkoloog esimese või teise tüüpi patoloogia. Suurerakuline lümfoom näitab juba protsessi suuremat pahaloomulisust: 3a etapp - kahjustus on haaranud ühe või kaks lümfisõlme, mis asuvad peamise lokaliseerimise kohast eemal; 3b etapp - see on juba inimkeha ja täpsemalt selle lümfisüsteemi ulatuslikum kahjustus.
Üsna sageli tuvastab onkoloog lisaks mitte-Hodgkini lümfoomidele ka arvukalt kaasnevaid patoloogiaid, mis olukorda ainult halvendavad.
Kellega ühendust võtta?
Ravi follikulaarne lümfoom
Seoses onkoloogiliste haiguste halveneva olukorraga, mille osakaal aasta-aastalt suureneb, soovitavad onkoloogid mitte ignoreerida ennetavaid uuringuid. Mida varem haigus diagnoositakse, seda suurem on patsiendi võimalus mitte ainult jätkata kvaliteetset elu pärast kasvajavastast ravi, vaid ka päästa oma elu. Follikulaarse lümfoomi ravi määratakse igale patsiendile rangelt individuaalselt, kohandades seda ravikuuri jooksul. On juhtumeid, kus onkoloogid, andes patsiendile teatud soovitusi, on ooteseisundis, jälgides perioodiliselt patsiendi tervist ja kasvaja kasvukiirust. Kasvaja progresseerumise suhteliselt madala määra tõttu võib kuluda kümme aastat, enne kui see hakkab avalduma, seega ei kiirusta arstid radikaalsete meetmetega, sest ka kirurgilise sekkumise ja keemiaravi ravimite määramine ei jää inimkehale jäljetult.
See tähendab, et kui diagnoositakse patoloogia esimene või teine etapp aeglase arenguvormiga, siis võib sellist kliinilist pilti täheldada kümme aastat, perioodiliselt vaheldumisi remissiooni- ja ägenemisperioodidega, arst jälgib pidevalt ainult patsiendi seisundit, olles igal ajal valmis võtma piisavaid meetmeid.
Kuid me peaksime teid kohe kinnitama, et follikulaarne lümfoom, kui seda avastatakse õigeaegselt ja ravitakse piisavalt, muutub üksikjuhtudel patsiendi surma põhjuseks.
Kuid on võimalik täheldada ka vastupidist kliinilist pilti, kus kasvaja hakkab kiiresti progresseeruma, levitades metastaase igas suunas nagu kombitsad. Sellise kliinilise pildi korral hakkavad arstid kohe tegutsema, määrates laser- ja/või keemiaravi kuuri. Kui patsiendi metastaasid on mõjutanud luuüdi, võib onkoloog otsustada määrata selle siirdamiseks operatsiooni. Kohe tasub mainida, et sellise haiguspildi korral ei tohiks loota täielikule remissioonile. Isegi kui patoloogia fookus on täielikult eemaldatud, võib selline patsient elada maksimaalselt kolm kuni viis aastat.
Patoloogilise arengu hilisemates etappides, metastaaside ilmnemisel ja koldest kaugemates organites, määrab raviarst-onkoloog sellisele patsiendile laser- ja/või polükeemilise ravi.
Tänapäeval on kõige populaarsem raviskeem, mis annab häid terapeutilisi tulemusi, CHOP-meetod, mida esindab raviprotokoll, mis hõlmab selliseid ravimeid nagu vinkrestiin, tsüklofosfamiid, doksorubitsiin ja prednisoloon.
Taimsel alkaloidil vinkrestiinil on patsiendi organismile kasvajavastane toime. Seda ravimit manustatakse patsiendile suu kaudu intravenoosselt. Manustamisskeem on üks kord nädalas.
Raviarst määrab ravimi annuse rangelt individuaalselt. Täiskasvanud patsiendile manustatav ühekordne algannus on 0,4–1,4 mg, arvutatuna patsiendi kehapinna ruutmeetri kohta ja võttes seda üks kord nädalas. Väikeste patsientide algannus on 2 mg, arvutatuna kehapinna ruutmeetri kohta ja võttes seda üks kord nädalas.
Vajadusel võib arst määrata ravimi intrapleuraalse manustamise, st farmakoloogiline vedelik tarnitakse kopsumembraanide vahelisse õõnsusruumi. Selle manustamisviisiga tarnitakse patsiendi kehasse 1 mg ravimit, mis vahetult enne protseduuri lahjendati 10 ml soolalahusega.
Selle ravimi võtmise vastunäidustuste hulka kuuluvad kesk- või perifeerse närvisüsteemi haigused, patsiendi keha suurenenud tundlikkus ühe või mitme ravimi komponendi suhtes. See hõlmab ka rasedust või imetamist.
Samuti on olemas soovitused selle farmakoloogilise kategooria ravimite käitlemiseks.
- Seda ravimit tuleb manustada äärmise ettevaatusega, olles eelnevalt veendunud, et nõel on veenis. Nekroosi vältimiseks ei tohi farmakoloogilise vedeliku süstimist läbi viia veeni.
- Selle meditsiinilise protseduuri ajal peab õde oma silmi kaitsma ja kui ravim satub neisse, peab ta neid väga kiiresti ja põhjalikult puhta voolava veega loputama.
- Enne keemiaravi alustamist ravi ajal on vajalik perifeerse vere seisundi regulaarne jälgimine.
- Samuti on vajalik maksafunktsiooni biokeemiliste omaduste pidev jälgimine.
- Kui neutrofiilide tase langeb alla kriitilise taseme, ei määrata keemiaravi ravimi manustamise protseduuri, vaid see lükatakse edasi, kuni normaalsed parameetrid taastatakse.
- Hepatotoksilise toime tekke vältimiseks on keemiaravi keelatud võtta paralleelselt kiiritusraviga, mis mõjutab neerude ja maksa piirkonda.
Meditsiinipersonal, kes töötab nende keemiaravis kasutatavate ravimitega, peab järgima kõiki isikukaitsevahendite nõudeid, mis kehtivad mürgiste keemiliste ühenditega tihedas kokkupuutes.
Koos CHOP-iga näitab CVP-režiim, mis hõlmab selliseid ravimeid nagu vinkrestiin, tsüklofosfamiid ja prednisoloon, sama efektiivsust.
Alküülivate keemiliste ühendite hulka kuuluvat kasvajavastast ravimit tsüklofosfamiidi võib raviarst välja kirjutada patoloogilise pildi põhjal kas intramuskulaarselt, intravenoosselt, intraperitoneaalselt või intrapleuraalselt.
Vahetult enne asjakohast protseduuri lahjendatakse ravimit süsteveega, 10 ml lahjendiga ravimipudeli kohta annusega 0,2 g. Ravimi kvaliteedi kontrollnäitajaks on aeg, mis kulub ravimi lahustumiseks vees - see ei tohiks ületada nelja minutit.
Spetsialist valib ravimi manustamise skeemi iseseisvalt. Selliseid skeeme on mitu.
- Ühekordne annus arvutatakse 3 mg-na patsiendi kehakaalu kilogrammi kohta ehk umbes 200 mg-na, mida manustatakse üks kord päevas. Ravimi manustamisviis: intravenoosselt või intramuskulaarselt.
- Ühekordne annus arvutatakse 6 mg-na patsiendi kehakaalu kilogrammi kohta ehk umbes 400 mg, mida manustatakse üks kord kaks korda päevas. Ravimi manustamisviis: intravenoosselt või intramuskulaarselt.
- Ühekordne annus arvutatakse 15 mg-na patsiendi kehakaalu kilogrammi kohta ehk umbes 1 g, manustatuna intravenoosselt üks kord iga viie päeva tagant.
- Ühekordne annus arvutatakse 30–40 mg patsiendi kehakaalu kilogrammi kohta, umbes 2–3 g, mida manustatakse intravenoosselt üks kord iga kahe kuni kolme nädala järel.
Ühe ravikuuri jooksul kasutatava ravimi kogus on vahemikus 6 kuni 14 g. Pärast põhikuuri lõpetamist harjutatakse tavaliselt säilitusravi, mis hõlmab 0,1–0,2 g ravimi intravenoosset või intramuskulaarset manustamist kaks korda ühe nädala jooksul.
Seda ravimit kasutatakse ka immunosupressandina. Sellisel juhul määrab arst ravimi kvantitatiivse komponendi kiirusega 1,0–1,5 mg patsiendi kehakaalu kilogrammi kohta, mis vastab päevasele kogusele 50–100 mg. Kui organismil on ravimi taluvus suurenenud, võib arst määrata annuse 3–4 mg patsiendi kehakaalu kilogrammi kohta.
Intraperitoneaalseks või intrapleuraalseks manustamiseks võib ravimi annus olla vahemikus 0,4 kuni 1,0 g.
Vastunäidustused kõnealuse ravimi kasutamisele on patsiendi keha ülitundlikkus ravimi komponendi suhtes, samuti juhul, kui patsiendi haigusloos on raske neerufunktsiooni häire, leukopeenia (leukotsüütide tase veres alla 3,5 x 109/l), luuüdi hüpoplaasia, aneemia või kahheksia, trombotsütopeenia (trombotsüütide tase veres alla 120 x 109/l). See soovitus kehtib ka haiguse lõppstaadiumis, samuti juhul, kui naine on rase või toidab vastsündinut rinnaga.
Kuid meditsiini onkoloogiline suund pidevalt paraneb, teadlased ja farmakoloogid leiavad uusi ravimeid, meetodeid ja vorme. Tänapäeval praktiseerivad mõned onkoloogiakliinikud uuenduslikke ravimeetodeid, kasutades patsiendi tüvirakke. Kuigi isegi praeguse meditsiini taseme taustal pole sellist haigust nagu follikulaarne lümfoom veel täielikult uuritud ja see pole täielikult ravitav.
Onkoloogid arvestavad ebasoodsa tulemuse riski suurendavate teguritega:
- Patsientide vanuserühm üle 60 aasta.
- Patsiendi hemoglobiinisisaldus määratakse näitajate põhjal, mis on alla 120 g/l.
- Kui patsiendil diagnoositakse kolmas või neljas arengustaadium.
- Laktaatdehüdrogenaasi tõus.
- Kui arst täheldab, et patsiendil on vähk, mis mõjutab rohkem kui nelja lümfisõlmede rühma.
Pärast keemiaravi või laserteraapia kuuri on patsient kohustatud läbima säilitusravi, mille eesmärk on parandada tema immuunseisundit, mis on ravi tõttu oluliselt vähenenud.
Pärast keemiaravi ravimite saamist on patsiendi immuunsus oluliselt vähenenud ja sekundaarse infektsiooni vältimiseks, mis paljudel juhtudel on surma põhjuseks, peab selline patsient teatud aja jooksul viibima steriilses keskkonnas.
Kui patsiendil avastatakse sekundaarne leukeemia, mis tekib follikulaarse lümfoomi taustal ja mõjutab luuüdi piirkondi, on onkoloog sunnitud määrama patsiendile selle aine siirdamise ühelt tema lähimalt sugulaselt. Vastasel juhul on täieõigusliku doonori leidmine üsna keeruline. Aga kui operatsioon läks hästi, näitab see meetod kõrgeid terapeutilisi tulemusi.
Kõige tähtsam on mitte hetke maha magada ja pöörduda võimalikult kiiresti spetsialisti poole! Mõnikord sõltub ajast mitte ainult inimese edasine elukvaliteet, vaid ka tema elu!
Ärahoidmine
Selles artiklis käsitletud patoloogia ennetamise kohta on üsna raske nõu anda, kuid siiski tasub arutada mõningaid eluaspekte, mis aitavad vähendada mis tahes vähkkasvajate riski.
Seetõttu on follikulaarse lümfoomi ennetamiseks ette nähtud mitu soovitust:
- Tervisliku eluviisi säilitamine.
- Halbadest harjumustest loobumine.
- Tasakaalustatud ja ratsionaalne toitumine, mis on rikas mikroelementide ja vitamiinide poolest.
- Säilitage oma immuunsüsteem õigel tasemel.
- Haiguse (mis tahes laadi) korral tuleb leevendusravi läbi viia õigeaegselt ja kuni täieliku taastumiseni.
- Veenduge, et keha ei jahtuks ega kuumeneks pikka aega üle.
- Vältige liigset päevitamist, vanne, sauna ja solaariumi.
- Oma kodu jaoks koha valimisel on soovitatav eelistada puhta ökosüsteemiga piirkondi, eemal suurtest tööstuspiirkondadest.
- Hüpodünaamia kõrvaldamine. Liikumine on elu.
- Paljud eksperdid usuvad, et mõte on materiaalne, et mitte selle väljenduse negatiivset külge enda peal proovile panna – mõelge ainult positiivselt, lõõgastus ja meeldiv muusika on teretulnud.
- Inimese igapäevane rutiin peaks harmooniliselt ühendama töökoormuse ja puhkeperioodid.
- Regulaarselt, vähemalt kord aastas, läbige spetsialiseeritud meditsiiniasutuses põhjalik ennetav läbivaatus.
Prognoos
Mitte-Hodgkini lümfoomi diagnoosiga patsiendi patoloogia tagajärgede ühemõtteline hindamine on problemaatiline, kuna kasvajavastase ravi tulemus sõltub suuresti haiguse astmest.
Kui arstid diagnoosivad esimese või teise astme patoloogia, mis näitab sõlmelist progresseerumise kiirust, siis üheksal kümnest patsiendist on follikulaarse lümfoomi prognoos üsna soodne, mis põhineb õigel diagnoosil ja piisaval keemiaravi režiimil.
Mitte-Hodgkini lümfoomi korral, millel on üks kolmanda arenguetapi sortidest, on haiguse nodulaarse kulgemise prognoos vähem soodne. Selle kliinilise pildi ellujäämismäär on vaid viis inimest kümnest diagnoositud juhtumist.
Hea uudis on see, et haiguse neljanda staadiumi patoloogiline areng, kui metastaasid mõjutavad juba üsna kaugeid organeid, on väga haruldane. Selle haiguse kulgu prognoos on ebasoodne isegi vajalike terapeutiliste meetmete korral. Terapeutiline ravi võimaldab patsiendi eluiga vaid veidi pikendada (parimal juhul mitu aastat), kuid surmav tulemus on peaaegu vältimatu.
Üsna sageli ei teki sellise patsiendi surm otse vähkkasvajast, vaid surma põhjuseks on sekundaarne infektsioon, mis üsna kergesti satub haigusest nõrgenenud organismi.
Selliste patsientide ellujäämise jälgimine on üsna kurb: kahekümnest IV staadiumi follikulaarse lümfoomi diagnoosiga patsiendist jääb ellu kaks või kolm.
Saastunud keskkond, toit ja kiire elutempo ei anna tänapäeva inimesele tervist. Küpsetest B-lümfotsüütidest koosnev monoklonaalne kasvaja - follikulaarne lümfoom. Vähidiagnoos lööb inimese ja tema lähedased rajalt välja, pannes nad dilemma ette - mida teha? On ainult üks vastus - pöörduda viivitamatult nõu saamiseks spetsialiseeritud onkoloogiakeskusesse, läbida onkoloogi poolt täielik läbivaatus ja määrata võimalik ravi. Ainult õigeaegne ja kiire reageerimine probleemile ning piisav ravi võivad suurendada patsiendi võimalusi tema edasise elukvaliteedi või isegi ainult elu enda osas. Ennetavaid uuringuid ei tohiks eirata. "Hoolitse oma tervise eest juba noorelt" - see rahvatarkus sobib kõige paremini tänase artikli teemaga! Hoolitse enda eest ja ole terve!
 [ 23 ]
[ 23 ]

