Artikli meditsiiniline ekspert
Uued väljaanded
Mitte-tuberkuloossed mükobakterid
Last reviewed: 04.07.2025

Kõik iLive'i sisu vaadatakse meditsiiniliselt läbi või seda kontrollitakse, et tagada võimalikult suur faktiline täpsus.
Meil on ranged allhanke juhised ja link ainult mainekate meediakanalite, akadeemiliste teadusasutuste ja võimaluse korral meditsiiniliselt vastastikuste eksperthinnangutega. Pange tähele, et sulgudes ([1], [2] jne) olevad numbrid on nende uuringute linkideks.
Kui tunnete, et mõni meie sisu on ebatäpne, aegunud või muul viisil küsitav, valige see ja vajutage Ctrl + Enter.
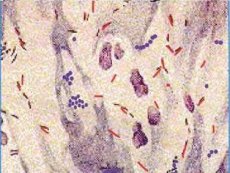
Mittetuberkuloosse mükobakterid on iseseisvad liigid, mis on keskkonnas saprofüütidena laialt levinud ja mõnel juhul võivad põhjustada raskeid haigusi - mükobakterioosi. Neid nimetatakse ka keskkonna mükobakteriteks, mükobakterioosi tekitajateks, oportunistlikeks ja atüüpilisteks mükobakteriteks. Oluline erinevus mittetuberkuloosse mükobakteri ja mükobakteri tuberkuloosi kompleksi vahel on see, et nad praktiliselt ei kandu inimeselt inimesele edasi.
Mittetuberkuloosse mükobakterid jagatakse nelja rühma, mis põhinevad piiratud arvul omadustel: kasvukiirus, pigmentide moodustumine, koloonia morfoloogia ja biokeemilised omadused.
1. rühm - aeglaselt kasvavad fotokromogeensed (M. kansasii jt.). Selle rühma esindajate peamine tunnus on pigmendi ilmumine valguse käes. Nad moodustavad S- kuni RS-vormis kolooniaid, sisaldavad karoteenikristalle, mis värvuvad kollaseks. Kasvukiirus on 7 kuni 20 päeva temperatuuridel 25, 37 ja 40 °C, katadaas-positiivsed.
M. kansasii on kollased batsillid, mis elavad vees ja pinnases ning mõjutavad kõige sagedamini kopse. Neid baktereid saab tuvastada nende suuruse ja ristikujulise paigutuse järgi. M. kansasii põhjustatud infektsioonide oluline ilming on dissemineerunud haiguse teke. Võimalikud on ka naha ja pehmete kudede kahjustused, tenosünoviidi, osteomüeliidi, lümfadeniidi, perikardiidi ja urogenitaaltrakti infektsioonide teke.
2. rühm - aeglaselt kasvavad skotokromogeensed (M. scrofulaceum, M. matmoense, M. gordonae jne). Mikroorganismid moodustavad pimedas kollaseid ja heledas oranže või punakaid kolooniaid, tavaliselt S-kujulised kolooniad, kasvavad temperatuuril 37 °C. See on arvukaim mittetuberkuloossetest mükobakteritest koosnev rühm. Neid eraldatakse saastunud veekogudest ja pinnasest ning neil on inimeste ja loomade jaoks madal patogeensus.
M. scrofulaceum (inglise keelest scrofula - scrofula) on üks peamisi emakakaela lümfadeniidi põhjustajaid alla 5-aastastel lastel. Raskete kaasuvate haiguste korral võivad need kahjustada kopse, luid ja pehmeid kudesid. Lisaks veele ja pinnasele on mikroobe eraldatud ka toorpiimast ja muudest piimatoodetest.
M. maimoense on mikroaerofiilid, mis moodustavad hallikasvalgeid, siledaid, läikivaid, läbipaistmatuid, kuplikujulisi ja ümaraid kolooniaid.
Primaarsed isolaadid kasvavad temperatuuril 22–37 °C väga aeglaselt. Valgusega kokkupuude ei põhjusta pigmendi tootmist. Vajadusel võib kokkupuudet jätkata kuni 12 nädalat. Inimestel põhjustavad nad kroonilist kopsuhaigust.
M. gordonae on kraanivee kõige levinumad saprofüüdid, skotokromogeenid ning põhjustavad mükobakterioosi äärmiselt harva. Lisaks veele (tuntud kui M. aquae) eraldatakse neid sageli pinnasest, maoloputusest, bronhide eritistest või muust patsientide materjalist, kuid enamasti ei ole nad inimestele patogeensed. Samal ajal on teateid meningiidi, peritoniidi ja nahakahjustuste juhtudest, mille on põhjustanud seda tüüpi mükobakterid.
3. rühm - aeglaselt kasvavad mittekromogeensed mükobakterid (M. avium kompleks, M. gaslri M. terrae kompleks jne). Nad moodustavad värvituid S- või SR- ja R-kolooniaid, millel võib olla helekollane ja kreemikas toon. Neid isoleeritakse haigetelt loomadelt, veest ja pinnasest.
M. avium - M. inlracellulare on ühendatud üheks M. avium kompleksiks, kuna nende liikidevaheline diferentseerumine tekitab teatud raskusi. Mikroorganismid kasvavad temperatuuril 25–45 °C, on patogeensed lindudele, vähem patogeensed veistele, sigadele, lammastele, koertele ja ei ole patogeensed merisigadele. Kõige sagedamini põhjustavad need mikroorganismid inimestel kopsukahjustusi. On kirjeldatud naha, lihaskoe ja skeleti kahjustusi, samuti haiguste dissemineerunud vorme. Need kuuluvad oportunistlike infektsioonide tekitajate hulka, mis raskendavad omandatud immuunpuudulikkuse sündroomi (AIDS). M. avium alamliik paratuberkuloos on veistel Jonesi tõve ja võimalik, et ka Crohni tõve (krooniline seedetrakti põletikuline haigus) põhjustaja inimestel. Mikroob esineb nakatunud lehmade lihas, piimas ja väljaheites ning seda leidub ka vees ja pinnases. Standardsed veepuhastusmeetodid seda mikroobi ei inaktiveeri.
M. xenopi põhjustab inimestel kopsukahjustusi ja AIDS-iga seotud dissemineerunud haigusvorme. Neid eraldatakse perekonna Xenopus konnadest. Bakterid moodustavad väikeseid, siledaid, läikivaid ja pigmenteerumata kolooniaid, mis hiljem muutuvad erekollaseks. Termofiilid ei kasva temperatuuril 22 °C ja kasvavad hästi temperatuuridel 37 ja 45 °C. Bakterioskoopia abil uurides näevad nad välja nagu väga õhukesed vardad, mis on ühest otsast kitsenevad ja paiknevad üksteisega paralleelselt (nagu piirdeaed). Neid eraldatakse sageli külmast ja kuumast kraaniveest, sealhulgas haiglate reservuaarides hoitavast joogiveest (nosokomiaalsed puhangud). Erinevalt teistest oportunistlikest mükobakteritest on nad tundlikud enamiku tuberkuloosivastaste ravimite suhtes.
M. ukerans on mükobakteriaalse naha N (Buruli haavand) etioloogiline tekitaja, kasvab ainult temperatuuril 30–33 °C, koloonia kasvu täheldatakse alles 7 nädala pärast. Patogeen vabaneb ka hiirte nakatumisel käpa talla pulpi. See haigus on levinud Austraalias ja Aafrikas. Nakkusallikaks on troopiline keskkond ja BCG vaktsineerimine selle mükobakterioosi vastu.
4. rühm - kiiresti kasvavad mükobakterid (M. fortuitum complex, M. phlei, M. xmegmatis jne). Nende kasvu täheldatakse R- või S-kujuliste kolooniate kujul 1-2 kuni 7 päeva jooksul. Neid leidub vees, pinnases, reovees ja nad on inimkeha normaalse mikrofloora esindajad. Selle rühma baktereid eraldatakse patsientide patoloogilisest materjalist harva, kuid mõnel neist on kliiniline tähtsus.
M. fortuitumi kompleksi kuuluvad M. fortuitum ja M. chcionae, mis koosnevad alamliikidest. Nad põhjustavad dissemineerunud protsesse, naha- ja postoperatiivseid infektsioone ning kopsuhaigusi. Selle kompleksi mikroobid on tuberkuloosivastaste ravimite suhtes väga resistentsed.
M. smegmatis on normaalse mikrofloora esindaja, mis on isoleeritud meeste smegmast. See kasvab hästi temperatuuril 45 °C. Inimeste haiguste tekitajana on see kiiresti kasvavate mükobakterite seas teisel kohal pärast M. fortuitumi kompleksi. See mõjutab nahka ja pehmeid kudesid. Tuberkuloosi patogeene tuleb uriini uurimisel M. smegmatis'est eristada.
Kõige sagedamini põhjustavad mükobakterioosi 3. ja 1. rühma esindajad.
Mükobakterioosi epidemioloogia
Mükobakterioosi tekitajad on looduses laialt levinud. Neid võib leida pinnases, tolmus, turbas, mudas, jõevees, tiikides ja basseinides. Neid leidub puukides ja kalades, nad põhjustavad lindude, mets- ja koduloomade haigusi ning on inimeste ülemiste hingamisteede ja urogenitaaltrakti limaskestade normaalse mikrofloora esindajad. Mittetuberkuloosse mükobakterisse nakatumine toimub keskkonnast õhus leviva tilga, nahakahjustusega kokkupuute, samuti toidu ja vee kaudu. Mikroorganismide ülekandumine inimeselt inimesele on haruldane. Need on oportunistlikud bakterid, seega on haiguse tekkes suur tähtsus makroorganismi resistentsuse vähenemisel ja selle geneetilisel eelsoodumusel. Kahjustatud piirkondades tekivad granulomatoossed rakud. Rasketel juhtudel on fagotsütoos mittetäielik, baktereemia on väljendunud ning organites avastatakse mittetuberkuloosse mükobakteriga täidetud ja leeprarakke meenutavaid makrofaage.
Mükobakterioosi sümptomid
Mükobakterioosi sümptomid on mitmekesised. Kõige sagedamini on mõjutatud hingamissüsteem. Kopsupatoloogia sümptomid on sarnased tuberkuloosi sümptomitega. Siiski esineb sageli protsessi ekstrapulmonaalset lokaliseerumist, mis hõlmab nahka ja nahaalust kude, haavapindu, lümfisõlmi, kuseteede organeid, luid ja liigeseid, samuti ajukelmeid. Elundite kahjustused võivad alata nii ägedalt kui ka latentselt, kuid peaaegu alati kulgevad raskelt.
Samuti on võimalik segainfektsiooni teke; mõnel juhul võivad need olla sekundaarse endogeense infektsiooni tekke põhjuseks.
Mükobakterioosi mikrobioloogiline diagnostika
Mükobakterioosi diagnoosimise peamine meetod on bakterioloogiline. Uuringu materjal võetakse haiguse patogeneesi ja kliiniliste ilmingute põhjal. Esialgu otsustatakse, kas eraldatud puhaskultuur kuulub tuberkuloosi tekitajate või mittetuberkuloossete mükobakterite hulka. Seejärel tehakse uuringute komplekt, et määrata mükobakterite tüüp, virulentsuse aste ja Runyoni rühm. Esmane identifitseerimine põhineb sellistel tunnustel nagu kasvukiirus, pigmendi moodustamise võime, koloonia morfoloogia ja võime kasvada erinevatel temperatuuridel. Nende tunnuste tuvastamiseks ei ole vaja täiendavaid seadmeid ega reagente, seega saab neid kasutada tuberkuloosi dispanserite põhilaborites. Lõplik identifitseerimine (võrdlusidentifitseerimine) keerukate biokeemiliste uuringute abil viiakse läbi teadusasutuste spetsialiseeritud moratooriumides. Enamasti eelistatakse nende identifitseerimist biokeemiliste faktide abil, näiteks tänapäevased molekulaargeneetilised meetodid on töömahukad, neil on palju ettevalmistavaid etappe, nad vajavad spetsiaalset varustust ja on kallid. Antibiootikumide suhtes tundlikkuse määramine on ravi seisukohalt väga oluline. Mükobakterioosi diagnoosimisel on määrava tähtsusega kriteerium kliiniliste, radioloogiliste ja laboratoorsete andmete samaaegse ilmnemise ning mittetuberkuloosse mükobakterite puhaskultuuri eraldamise ja mitmete dünaamika uuringute läbiviimise kohta.
Diagnostikas on teisejärgulise tähtsusega antiteeside määramine RNGA, RP, immunoelektroforeesi, RNIF ja ELISA abil, samuti nahaallergia testide tegemine sensitiinidega.
Mükobakterioosi ravi ja spetsiifiline ennetamine
Kõik mittetuberkuloosse mükobakteri tüübid, välja arvatud M. xenopi, on resistentsed isoniasiidi, streptomütsiini ja tiosemikarbasoonide suhtes. Mükobakterioosi ravi tuberkuloosivastaste ja antibakteriaalsete ravimitega peaks olema pikaajaline (12-13 kuud) ja kombineeritud. Tavaliselt on see ebaefektiivne MAC-infektsioonide ja kiiresti kasvavate mükobakterite põhjustatud haiguste korral. Mõnel juhul kasutatakse kirurgilist ravi. Mükobakterioosi spetsiifiliseks ennetamiseks mõeldud ravimeid ei ole välja töötatud.


 [
[