Artikli meditsiiniline ekspert
Uued väljaanded
hüpofüüsi
Viimati vaadatud: 04.07.2025

Kõik iLive'i sisu vaadatakse meditsiiniliselt läbi või seda kontrollitakse, et tagada võimalikult suur faktiline täpsus.
Meil on ranged allhanke juhised ja link ainult mainekate meediakanalite, akadeemiliste teadusasutuste ja võimaluse korral meditsiiniliselt vastastikuste eksperthinnangutega. Pange tähele, et sulgudes ([1], [2] jne) olevad numbrid on nende uuringute linkideks.
Kui tunnete, et mõni meie sisu on ebatäpne, aegunud või muul viisil küsitav, valige see ja vajutage Ctrl + Enter.
Hüpofüüs (hüpofüüs, s.glandula pituitaria) asub kiiluluu turjakõvera hüpofüüsi lohus ja eraldub koljuõõnest aju kõvakesta jätke abil, moodustades koljuõõne diafragma. Selle diafragma ava kaudu on hüpofüüs ühenduses vaheaju hüpotalamuse infundibulumiga. Hüpofüüsi ristisuunaline suurus on 10–17 mm, anteroposteriorne 5–15 mm, vertikaalne 5–10 mm. Hüpofüüsi mass meestel on umbes 0,5 g, naistel 0,6 g. Hüpofüüs on väljastpoolt kaetud kapsliga.
Vastavalt hüpofüüsi arengule kahest erinevast rudimendist eristub elundis kaks sagarat - eesmine ja tagumine. Adenohüpofüüs ehk eesmine lobe (adenohypophysis, s.lobus anterior) on suurem, moodustades 70-80% hüpofüüsi kogumassist. See on tihedam kui tagumine lobe. Eesmises lobis eristub distaalne osa (pars distalis), mis hõivab hüpofüüsi lohu eesmise osa, vahepealne osa (pars intermedia), mis asub tagumise loba piiril, ja muguljas osa (pars tuberalis), mis ulatub ülespoole ja ühendub hüpotalamuse infundibulumiga. Veresoonte rohkuse tõttu on eesmine lobe kahvatukollane värvus punaka varjundiga. Hüpofüüsi eesmise näärme parenhüümi esindavad mitut tüüpi näärmerakud, mille ahelate vahel paiknevad sinusoidaalsed verekapillaarid. Pooled (50%) adenohüpofüüsi rakkudest on kromofiilsed adenotsüüdid, mille tsütoplasmas on peeneteralised graanulid, mis värvuvad hästi kroomi sooladega. Need on atsidofiilsed adenotsüüdid (40% kõigist adenohüpofüüsi rakkudest) ja basofiilsed adenotsüüdid (10%). Basofiilsete adenotsüütide hulka kuuluvad gonadotroopsed, kortikotroopsed ja türeotroopsed endokrinotsüüdid. Kromofoobsed adenotsüüdid on väikesed, neil on suur tuum ja väike tsütoplasma maht. Neid rakke peetakse kromofiilsete adenotsüütide eelkäijateks. Ülejäänud 50% adenohüpofüüsi rakkudest on kromofoobsed adenotsüüdid.
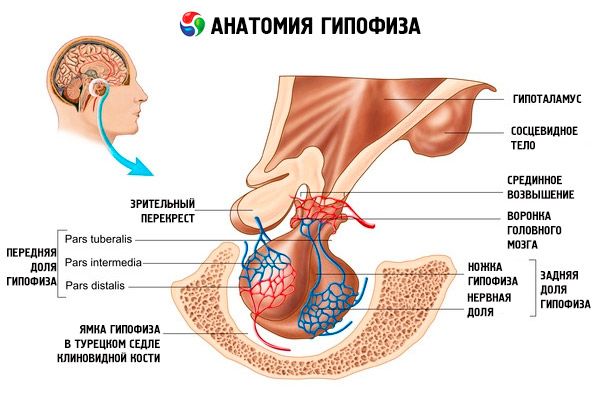
Neurohüpofüüs ehk tagumine lobe (neurohypophysis, s.lobus posterior) koosneb närvisagarast (lobus nervosus), mis asub hüpofüüsi lohu tagumises osas, ja lehtrikujulisest osast (infundibulum), mis asub adenohüpofüüsi mugulakujulise osa taga. Hüpofüüsi tagumise lobe moodustavad neurogliiarakud (hüpofüüsirakud), närvikiud, mis kulgevad hüpotalamuse neurosekretoorsetest tuumadest neurohüpofüüsi, ja neurosekretoorsed rakud.
Hüpofüüs on närvikiudude (radade) ja veresoonte kaudu funktsionaalselt seotud vaheaju hüpotalamusega, mis reguleerib hüpofüüsi aktiivsust. Hüpofüüsi ja hüpotalamust koos nende neuroendokriinsete, veresoonte ja närviühendustega peetakse tavaliselt hüpotaalamuse-hüpofüüsi süsteemiks.
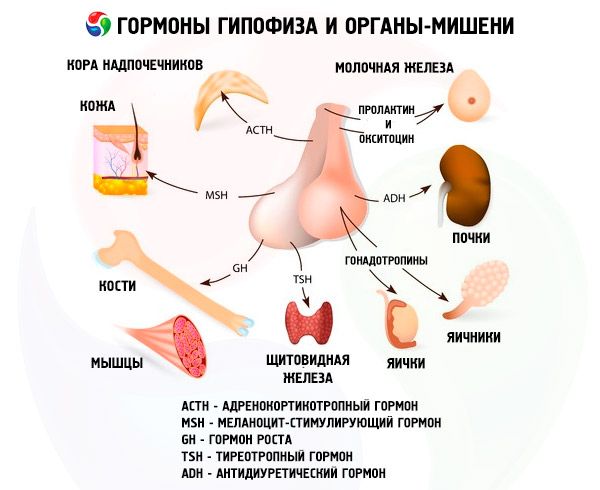
Hüpofüüsi eesmise ja tagumise osa hormoonid mõjutavad paljusid keha funktsioone, peamiselt teiste endokriinsete näärmete kaudu. Hüpofüüsi eesmises osas toodavad atsidofiilsed adenotsüüdid (alfa-rakud) somatotroopset hormooni (kasvuhormooni), mis osaleb noorte organismide kasvu- ja arenguprotsesside regulatsioonis. Kortikotroopsed endokrinotsüüdid eritavad adrenokortikotroopset hormooni (ACTH), mis stimuleerib neerupealiste poolt steroidhormoonide sekretsiooni. Türeotroopsed endokrinotsüüdid eritavad türeotroopset hormooni (TSH), mis mõjutab kilpnäärme arengut ja aktiveerib selle hormoonide tootmist. Gonadotroopsed hormoonid: folliikuleid stimuleeriv (FSH), luteiniseeriv (LH) ja prolaktiin - mõjutavad keha seksuaalset küpsemist, reguleerivad ja stimuleerivad folliikulite arengut munasarjas, ovulatsiooni, piimanäärmete kasvu ja piimatootmist naistel, spermatogeneesi protsessi meestel. Neid hormoone toodavad basofiilsed adenotsüüdid (beeta-rakud). Siin erituvad ka hüpofüüsi lipotroopsed faktorid, mis mõjutavad rasvade mobiliseerimist ja kasutamist organismis. Eesmise lobe vahepealses osas moodustub melanotsüüte stimuleeriv hormoon, mis kontrollib pigmentide – melaniinide – teket organismis.
Hüpotalamuse supraoptilise ja paraventrikulaarse tuuma neurosekretoorsed rakud toodavad vasopressiini ja oksütotsiini. Need hormoonid transporditakse hüpotaalamuse-hüpofüüsi trakti moodustavate aksonite kaudu hüpofüüsi tagumise osa rakkudesse. Hüpofüüsi tagumisest osast sisenevad need ained verre. Hormoon vasopressiinil on vasokonstriktiivne ja antidiureetiline toime, mille tõttu seda nimetatakse ka antidiureetiliseks hormooniks (ADH). Oksütotsiinil on stimuleeriv toime emaka lihaste kontraktiilsusele, see suurendab lakteeriva piimanäärme piimaeritust, pärsib kollaskeha arengut ja funktsiooni ning mõjutab seedetrakti silelihaste (mittevöötmeliste) toonuse muutusi.
Hüpofüüsi areng
Hüpofüüsi eesmine lobe areneb suuõõne seljaseina epiteelist rõngakujulise kasvajana (Rathke kott). See ektodermaalne eend kasvab tulevase kolmanda vatsakese põhja suunas. Selle suunas, teise ajupõiekese (tulevase kolmanda vatsakese põhja) alumisest pinnast, kasvab protsess, millest arenevad infundibulumi hall kühm ja hüpofüüsi tagumine lobe.
Hüpofüüsi veresooned ja närvid
Sisemistest unearteritest ja suuraju arteriaalse ringi veresoontest suunduvad ülemine ja alumine hüpofüüsiarter hüpofüüsi. Ülemised hüpofüüsiarterid suunduvad halli tuuma ja hüpotalamuse infundibulumi, anastomoosivad siin üksteisega ja moodustavad ajukoesse tungivaid kapillaare - primaarset hemokapillaarset võrgustikku. Selle võrgustiku pikkadest ja lühikestest silmustest moodustuvad portaalveenid, mis suunduvad hüpofüüsi eesmisse lobisse. Hüpofüüsi eesmise lobe parenhüümis lagunevad need veenid laiadeks sinusoidaalseteks kapillaarideks, moodustades sekundaarse hemokapillaarse võrgustiku. Hüpofüüsi tagumist lobe varustatakse verega peamiselt alumise hüpofüüsiarteri kaudu. Ülemise ja alumise hüpofüüsiarteri vahel on pikad arteriaalsed anastomoosid. Venoosse vere väljavool sekundaarsest hemokapillaarsest võrgustikust toimub veenide süsteemi kaudu, mis suubub aju kõvakesta kavernoossetesse ja interkavernoossetesse siinustesse.
Hüpofüüsi innervatsioonis osalevad sümpaatilised kiud, mis sisenevad elundisse koos arteritega. Postganglionaarsed sümpaatilised närvikiud väljuvad sisemise unearteri põimikult. Lisaks leidub hüpofüüsi tagumises lobas arvukalt hüpotalamuse tuumades paiknevate neurosekretoorsete rakkude jätkete otsi.
Hüpofüüsi vanusega seotud omadused
Hüpofüüsi keskmine kaal vastsündinutel ulatub 0,12 g-ni. Elundi kaal kahekordistub 10. eluaastaks ja kolmekordistub 15. eluaastaks. 20. eluaastaks saavutab hüpofüüsi kaal oma maksimumi (530–560 mg) ja jääb järgnevatel vanuseperioodidel peaaegu muutumatuks. 60 aasta pärast täheldatakse selle endokriinse näärme kaalu kerget vähenemist.
 [ 7 ], [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ]
[ 7 ], [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ]
Hüpofüüsi hormoonid
Närvilise ja hormonaalse regulatsiooni ühtsus kehas tagatakse hüpofüüsi ja hüpotalamuse tiheda anatoomilise ja funktsionaalse seose abil. See kompleks määrab kogu endokriinsüsteemi seisundi ja toimimise.
Peamine endokriinne nääre, mis toodab mitmeid peptiidhormoone, mis otseselt reguleerivad perifeersete näärmete funktsiooni, on hüpofüüs. See on punakashall oakujuline moodustis, mis on kaetud kiulise kapsliga, mis kaalub 0,5–0,6 g. See varieerub veidi sõltuvalt inimese soost ja vanusest. Hüpofüüsi üldtunnustatud jaotus kaheks sagaraks, mis erinevad arengu, struktuuri ja funktsiooni poolest, on säilinud: eesmine distaalne - adenohüpofüüs ja tagumine - neurohüpofüüs. Esimene moodustab umbes 70% näärme kogumassist ja jaguneb tavapäraselt distaalseks, infundibulaarseks ja vahepealseks osaks, teine - tagumiseks osaks ehk sagaraks ja hüpofüüsi varreks. Nääre asub kiiluluu turjakujulise ajuripatsi lohus ja on varre kaudu ühendatud ajuga. Eesmise sagara ülemist osa katavad nägemisnärvi kiasm ja nägemistraktid. Hüpofüüsi verevarustus on väga rikkalik ja seda teostavad sisemise unearteri harud (hüpofüüsi ülemine ja alumine arter), samuti suuraju arteriaalse ringi harud. Hüpofüüsi ülemised arterid osalevad adenohüpofüüsi verevarustuses ja alumised neurohüpofüüsi arterid, kontakteerudes hüpotalamuse suurte rakkude tuumade aksonite neurosekretoorsete otstega. Esimesed sisenevad hüpotalamuse keskmise eminentsi juurde, kus nad hajuvad kapillaaride võrgustikku (primaarne kapillaaride põimik). Need kapillaarid (millega kontakteeruvad mediobasaalse hüpotalamuse väikeste neurosekretoorsete rakkude aksonite otsad) kogunevad portaalveenidesse, mis laskuvad mööda hüpofüüsi vart adenohüpofüüsi parenhüümi, kus nad jagunevad taas sinusoidaalsete kapillaaride võrgustikuks (sekundaarne kapillaaride põimik). Seega siseneb veri, olles eelnevalt läbinud hüpotalamuse keskmise eminentsi, kus see rikastub hüpotaalamuse adenohüpofüsotroopsete hormoonidega (vabastavad hormoonid), adenohüpofüüsi.
Adenohüpofüüsihormoonidega küllastunud vere väljavool sekundaarse plexuse arvukatest kapillaaridest toimub veenide süsteemi kaudu, mis omakorda voolab dura mater'i venoossetesse siinustesse ja seejärel üldisesse vereringesse. Seega on hüpofüüsi portaalsüsteem, millel on hüpotalamusest laskuv verevoolu suund, adenohüpofüüsi troopiliste funktsioonide neurohumoraalse kontrolli keerulise mehhanismi morfofunktsionaalne komponent.
Hüpofüüsi innerveerivad sümpaatilised kiud, mis järgnevad hüpofüüsi arteritele. Need pärinevad postganglionaarsetest kiududest, mis läbivad sisemist karotiidpõimiku ja on ühendatud ülemiste kaelaganglionidega. Adenohüpofüüsi otsest innervatsiooni hüpotalamusest ei toimu. Tagumine sagar saab närvikiude hüpotalamuse neurosekretoorsetest tuumadest.
Adenohüpofüüsi histoloogiline struktuur on väga keeruline. Sellel on kahte tüüpi näärmerakke - kromofoobsed ja kromofiilsed. Viimased jagunevad omakorda atsidofiilseteks ja basofiilseteks (hüpofüüsi detailne histoloogiline kirjeldus on esitatud käsiraamatu vastavas osas). Siiski tuleb märkida, et adenohüpofüüsi parenhüümi moodustavate näärmerakkude poolt toodetavad hormoonid on viimaste mitmekesisuse tõttu oma keemilise olemuse poolest mõnevõrra erinevad ning sekreteerivate rakkude peenstruktuur peab vastama igaühe biosünteesi tunnustele. Kuid mõnikord võib adenohüpofüüsis täheldada näärmerakkude üleminekuvorme, mis on võimelised tootma mitut hormooni. On tõendeid, et adenohüpofüüsi näärmerakkude tüüp ei ole alati geneetiliselt määratud.
Turtskõrvase kelme diafragma all asub eesmise lobe lehtrikujuline osa. See haarab hüpofüüsi vart ja puutub kokku halli kühmuga. Seda adenohüpofüüsi osa iseloomustab epiteelirakkude olemasolu ja rikkalik verevarustus. See on ka hormonaalselt aktiivne.
Hüpofüüsi vahepealne (keskmine) osa koosneb mitmest suurte sekretoorselt aktiivsete basofiilsete rakkude kihist.
Hüpofüüs täidab oma hormoonide kaudu mitmesuguseid funktsioone. Selle eesmine lobe toodab adrenokortikotroopseid (ACTH), kilpnääret stimuleerivaid (TSH), folliikuleid stimuleerivaid (FSH), luteiniseerivaid (LH), lipotroopseid hormoone, samuti kasvuhormooni - somatotroopset (STO) ja prolaktiini. Vahesagaras sünteesitakse melanotsüüte stimuleerivat hormooni (MSH) ja tagumises lobis akumuleeruvad vasopressiin ja oksütotsiin.
AKTH
Hüpofüüsi hormoonid on valgu- ja peptiidhormoonide ning glükoproteiinide rühm. Hüpofüüsi eessagara hormoonidest on kõige paremini uuritud AKTH-d. Seda toodavad basofiilsed rakud. Selle peamine füsioloogiline funktsioon on stimuleerida neerupealise koore steroidhormoonide biosünteesi ja sekretsiooni. AKTH-l on ka melanotsüüte stimuleeriv ja lipotroopne toime. 1953. aastal eraldati see puhtal kujul. Hiljem määrati kindlaks selle keemiline struktuur, mis koosneb 39 aminohappejäägist inimestel ja paljudel imetajatel. AKTH-l puudub liigispetsiifilisus. Praegu on läbi viidud nii hormooni enda kui ka selle molekuli erinevate fragmentide keemiline süntees, mis on aktiivsemad kui looduslikud hormoonid. Hormooni struktuuril on kaks peptiidahela osa, millest üks tagab AKTH tuvastamise ja seondumise retseptoriga ning teine annab bioloogilise efekti. See seondub ilmselt AKTH retseptoriga hormooni ja retseptori elektrilaengute vastastikmõju kaudu. AKTH bioloogilise efektori rolli täidab 4-10 molekuli fragment (Met-Glu-His-Phen-Arg-Tri-Tri).
AKTH melanotsüüte stimuleeriv toime tuleneb molekulis olevast N-terminaalsest piirkonnast, mis koosneb 13 aminohappejäägist ja kordab alfa-melanotsüüte stimuleeriva hormooni struktuuri. See piirkond sisaldab ka heptapeptiidi, mida leidub ka teistes hüpofüüsi hormoonides ja millel on adrenokortikotroopne, melanotsüüte stimuleeriv ja lipotroopne toime.
AKTH toime võtmemomendiks peetakse ensüümi proteiinkinaasi aktiveerimist tsütoplasmas cAMP osalusel. Fosforüülitud proteiinkinaas aktiveerib ensüümi esteraasi, mis muundab kolesterooli estrid rasvapiiskades vabaks aineks. Ribosoomide fosforüülimise tulemusena tsütoplasmas sünteesitud valk stimuleerib vaba kolesterooli seondumist tsütokroom P-450-ga ja selle ülekandumist lipiidipiiskadest mitokondritesse, kus esinevad kõik ensüümid, mis tagavad kolesterooli muundumise kortikosteroidideks.
 [ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ], [ 21 ], [ 22 ]
[ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ], [ 21 ], [ 22 ]
Kilpnääret stimuleeriv hormoon
TSH - türeotropiin - kilpnäärme arengu ja toimimise, kilpnäärmehormoonide sünteesi ja sekretsiooni protsesside peamine regulaator. See keeruline valk - glükoproteiin - koosneb alfa- ja beeta-alamühikutest. Esimese alaühiku struktuur langeb kokku luteiniseeriva hormooni alfa-alamühikuga. Lisaks langeb see suures osas kokku erinevatel loomaliikidel. Inimese TSH beeta-alamühiku aminohappejääkide järjestus on dešifreeritud ja koosneb 119 aminohappejäägist. Võib märkida, et inimese ja veise TSH beeta-alamühikud on mitmes mõttes sarnased. Glükoproteiinihormoonide bioloogilised omadused ja bioloogilise aktiivsuse olemus määratakse beeta-alamühiku poolt. See tagab ka hormooni interaktsiooni retseptoritega erinevates sihtorganites. Enamikul loomadel ilmneb beeta-alamühik aga spetsiifilise aktiivsuse alles pärast ühendumist alfa-alamühikuga, mis toimib hormooni omamoodi aktivaatorina. Viimane indutseerib võrdse tõenäosusega luteiniseerivat, folliikuleid stimuleerivat ja türeotroopset aktiivsust, mis on määratud beeta-alamühiku omadustega. Leitud sarnasus võimaldab järeldada, et need hormoonid tekkisid evolutsiooni käigus ühest ühisest eelkäijast, beeta-alaühik määrab ka hormoonide immunoloogilised omadused. Eeldatakse, et alfa-alaühik kaitseb beeta-alaühikut proteolüütiliste ensüümide toime eest ja hõlbustab ka selle transportimist hüpofüüsist perifeersetesse sihtorganitesse.
Gonadotroopsed hormoonid
Gonadotropiinid esinevad organismis LH ja FSH kujul. Nende hormoonide funktsionaalne eesmärk piirdub üldiselt mõlema soo esindajate reproduktiivprotsesside tagamisega. Nagu TSH, on need keerulised valgud - glükoproteiinid. FSH indutseerib folliikulite küpsemist emastel munasarjades ja stimuleerib spermatogeneesi isastel. LH põhjustab emastel folliikulite rebenemist koos kollakeha moodustumisega ning stimuleerib östrogeenide ja progesterooni sekretsiooni. Meestel kiirendab sama hormoon interstitsiaalse koe arengut ja androgeenide sekretsiooni. Gonadotropiinide toimed on üksteisest sõltuvad ja esinevad sünkroonselt.
Gonadotropiinide sekretsiooni dünaamika naistel muutub menstruaaltsükli jooksul ja seda on piisavalt detailselt uuritud. Tsükli preovulatoorses (follikulaarses) faasis on LH sisaldus üsna madal, samas kui FSH on suurenenud. Folliikuli küpsedes suureneb östradiooli sekretsioon, mis soodustab hüpofüüsi poolt gonadotropiinide suurenenud tootmist ja nii LH kui ka FSH tsüklite toimumist ehk suguhormoonid stimuleerivad gonadotropiinide sekretsiooni.
Praeguseks on LH struktuur kindlaks määratud. Nagu TSH, koosneb see kahest allüksusest: a ja b. LH alfa-alaühiku struktuur erinevatel loomaliikidel on suures osas sarnane, see vastab TSH alfa-alaühiku struktuurile.
LH beeta-alaühiku struktuur erineb oluliselt TSH beeta-alaühiku struktuurist, kuigi sellel on neli identset peptiidahela osa, mis koosnevad 4-5 aminohappejäägist. TSH-s paiknevad need positsioonidel 27-31, 51-54, 65-68 ja 78-83. Kuna LH ja TSH beeta-alaühik määrab hormoonide spetsiifilise bioloogilise aktiivsuse, võib eeldada, et LH ja TSH struktuuri homoloogsed osad peaksid tagama beeta-alaühikute seose alfa-alaühikuga ning struktuurilt erinevad osad peaksid vastutama hormoonide bioloogilise aktiivsuse spetsiifilisuse eest.
Natiivne LH on proteolüütiliste ensüümide toime suhtes väga stabiilne, kuid beeta-alaühiku lõhustab kümotrüpsiin kiiresti ja α-alaühikut on ensüümil raske hüdrolüüsida, st see täidab kaitsvat rolli, takistades kümotrüpsiini ligipääsu peptiidsidemetele.
FSH keemilise struktuuri osas pole teadlased veel lõplikke tulemusi saanud. Nagu LH, koosneb ka FSH kahest allüksusest, kuid FSH beeta-allüksus erineb LH beeta-allüksusest.
Prolaktiin
Teine hormoon, prolaktiin (laktogeenne hormoon), mängib aktiivset rolli paljunemisprotsessides. Prolaktiini peamised füsioloogilised omadused imetajatel avalduvad piimanäärmete ja laktatsiooni arengu stimuleerimise, rasunäärmete ja siseorganite kasvu näol. See soodustab steroidide mõju avaldumist isasloomade sekundaarsetele sugutunnustele, stimuleerib hiirtel ja rottidel kollaskeha sekretoorset aktiivsust ning osaleb rasvade ainevahetuse reguleerimises. Viimastel aastatel on prolaktiinile pööratud palju tähelepanu kui ema käitumise regulaatorile; sellist polüfunktsionaalsust seletatakse selle evolutsioonilise arenguga. See on üks iidsetest hüpofüüsi hormoonidest ja seda leidub isegi kahepaiksetel. Praegu on prolaktiini struktuur mõnedel imetajaliikidel täielikult dešifreeritud. Kuid kuni viimase ajani väljendasid teadlased kahtlust sellise hormooni olemasolus inimestel. Paljud uskusid, et selle funktsiooni täidab kasvuhormoon. Nüüd on saadud veenvaid tõendeid prolaktiini olemasolu kohta inimestel ja selle struktuur on osaliselt dešifreeritud. Prolaktiini retseptorid seonduvad aktiivselt kasvuhormooni ja platsenta laktogeeniga, mis viitab kolme hormooni ühtsele toimemehhanismile.
Somatotropiin
Kasvuhormoonil somatotropiinil on veelgi laiem toimespekter kui prolaktiinil. Nagu prolaktiini, toodavad seda adenohüpofüüsi atsidofiilsed rakud. STH stimuleerib skeleti kasvu, aktiveerib valkude biosünteesi, omab rasvu mobiliseerivat toimet ja soodustab keha suuruse suurenemist. Lisaks koordineerib see ainevahetusprotsesse.
Hormooni osalemist viimases kinnitab asjaolu, et hüpofüüsi sekretsioon suureneb järsult, näiteks kui veresuhkru tase langeb.
Selle inimese hormooni keemiline struktuur on nüüdseks täielikult välja kujunenud – 191 aminohappejääki. Selle primaarstruktuur sarnaneb koorionse somatomammotropiini või platsenta laktogeeni omaga. Need andmed näitavad kahe hormooni olulist evolutsioonilist lähedust, kuigi neil on bioloogilises aktiivsuses erinevusi.
Vajalik on rõhutada kõnealuse hormooni kõrget liigispetsiifilisust – näiteks on loomset päritolu STH inimestel inaktiivne. Seda seletatakse nii inimeste ja loomade STH retseptorite vahelise reaktsiooniga kui ka hormooni enda struktuuriga. Praegu käivad uuringud STH keerulises struktuuris aktiivsete keskuste tuvastamiseks, millel on bioloogiline aktiivsus. Uuritakse molekuli üksikuid fragmente, millel on muud omadused. Näiteks pärast inimese STH hüdrolüüsi pepsiiniga eraldati peptiid, mis koosnes 14 aminohappejäägist ja vastas molekuli lõigule 31-44. Sellel ei olnud kasvuefekti, kuid see ületas oluliselt natiivset hormooni lipotroopse aktiivsuse poolest. Inimese kasvuhormoonil on erinevalt loomade sarnasest hormoonist märkimisväärne laktogeenne aktiivsus.
Adenohüpofüüs sünteesib paljusid peptiid- ja valguaineid, millel on rasva mobiliseeriv toime, ning hüpofüüsi troopilised hormoonid - AKTH, STH, TSH ja teised - omavad lipotroopset toimet. Viimastel aastatel on eriti rõhutatud beeta- ja γ-lipotroopseid hormoone (LPG). Kõige detailsemalt on uuritud beeta-LPG bioloogilisi omadusi; lisaks lipotroopsele aktiivsusele on sellel ka melanotsüüte stimuleeriv, kortikotropiini stimuleeriv ja hüpokaltseemiline toime ning see tekitab ka insuliinilaadse efekti.
Praeguseks on dešifreeritud lammaste LPG (90 aminohappejääki), sigade ja veiste lipotroopsete hormoonide, primaarstruktuur. Sellel hormoonil on liigispetsiifilisus, kuigi beeta-LPG keskse piirkonna struktuur on eri liikidel sama. See määrab hormooni bioloogilised omadused. Üks selle piirkonna fragmentidest leidub alfa-MSH, beeta-MSH, AKTH ja beeta-LPG struktuuris. On oletatud, et need hormoonid tekkisid evolutsiooniprotsessis samast eelkäijast. γ-LPG-l on nõrgem lipotroopne aktiivsus kui beeta-LPG-l.
Melanotsüüte stimuleeriv hormoon
See hüpofüüsi vahesagaras sünteesitud hormoon stimuleerib oma bioloogilises funktsioonis nahapigmendi melaniini biosünteesi, soodustab kahepaiksete naha pigmendirakkude melanotsüütide suuruse ja arvu suurenemist. Neid MSH omadusi kasutatakse hormooni bioloogilises testimises. Hormooni on kahte tüüpi: alfa- ja beeta-MSH. On näidatud, et alfa-MSH-l puudub liigispetsiifilisus ja sellel on kõigil imetajatel sama keemiline struktuur. Selle molekul on peptiidahel, mis koosneb 13 aminohappejäägist. Beeta-MSH-l seevastu on liigispetsiifilisus ja selle struktuur on erinevatel loomadel erinev. Enamikul imetajatel koosneb beeta-MSH molekul 18 aminohappejäägist ja ainult inimestel on see aminohappe otsast pikenenud nelja aminohappejäägi võrra. Tuleb märkida, et alfa-MSH-l on teatav adrenokortikotroopne toime ja selle mõju loomade ja inimeste käitumisele on nüüdseks tõestatud.
Oksütotsiin ja vasopressiin
Hüpotalamuses sünteesitavad vasopressiin ja oksütotsiin akumuleeruvad hüpofüüsi tagumisse sagarasse: vasopressiin supraoptilise tuuma neuronitesse ja oksütotsiin paraventrikulaarsesse tuuma. Seejärel kanduvad nad hüpofüüsi. Tuleb rõhutada, et vasopressiinhormooni eelkäija sünteesitakse kõigepealt hüpotalamuses. Samal ajal toodetakse seal valke neurofüsiini tüüpe 1 ja 2. Esimene seob oksütotsiini ja teine vasopressiini. Need kompleksid migreeruvad neurosekretoorsete graanulite kujul tsütoplasmas mööda aksonit ja jõuavad hüpofüüsi tagumisse sagarasse, kus närvikiud lõpevad veresoone seinas ja graanulite sisu siseneb verre. Vasopressiin ja oksütotsiin on esimesed hüpofüüsi hormoonid, millel on täielikult väljakujunenud aminohappejärjestus. Oma keemiliselt struktuurilt on nad nonapeptiidid ühe disulfiidsillaga.
Vaatlusalused hormoonid avaldavad mitmesuguseid bioloogilisi efekte: nad stimuleerivad vee ja soolade transporti läbi membraanide, omavad vasopressiivset efekti, suurendavad emaka silelihaste kokkutõmbumist sünnituse ajal ja suurendavad piimanäärmete sekretsiooni. Tuleb märkida, et vasopressiinil on suurem antidiureetiline toime kui oksütotsiinil, samas kui viimasel on tugevam mõju emakale ja piimanäärmetele. Vasopressiini sekretsiooni peamine regulaator on vee tarbimine; neerutuubulites seondub see tsütoplasmaatiliste membraanide retseptoritega, mille järel aktiveeritakse neis ensüüm adenülaattsüklaas. Molekuli erinevad osad vastutavad hormooni retseptoriga seondumise ja bioloogilise efekti eest.
Hüpofüüsi kaudu kogu närvisüsteemiga ühendatud nääre ühendab endokriinsüsteemi funktsionaalseks tervikuks, osaledes keha sisekeskkonna püsivuse tagamises (homeostaas). Endokriinsüsteemi sees toimub homöostaatiline regulatsioon hüpofüüsi eesmise lobe ja "sihtnäärmete" (kilpnääre, neerupealise koore, sugunäärmete) vahelise tagasiside põhimõttel. "Sihtnäärme" poolt toodetud hormooni liig pärsib ja selle puudus stimuleerib vastava troopilise hormooni sekretsiooni ja vabanemist. Hüpotalamus kuulub tagasisidesüsteemi. Just selles asuvad "sihtnäärmete" hormoonide suhtes tundlikud retseptoritsoonid. Spetsiifiliselt veres ringlevate hormoonidega seondudes ja hormoonide kontsentratsioonist sõltuvalt reaktsiooni muutes edastavad hüpotalamuse retseptorid oma toime vastavatesse hüpotalamuse keskustesse, mis koordineerivad adenohüpofüüsi tööd, vabastades hüpotalamuse adenohüpofüsiotroopseid hormoone. Seega tuleks hüpotalamust pidada neuroendokriinseks ajuks.

