Äge hematogeenne osteomüeliit
Viimati vaadatud: 07.06.2024

Kõik iLive'i sisu vaadatakse meditsiiniliselt läbi või seda kontrollitakse, et tagada võimalikult suur faktiline täpsus.
Meil on ranged allhanke juhised ja link ainult mainekate meediakanalite, akadeemiliste teadusasutuste ja võimaluse korral meditsiiniliselt vastastikuste eksperthinnangutega. Pange tähele, et sulgudes ([1], [2] jne) olevad numbrid on nende uuringute linkideks.
Kui tunnete, et mõni meie sisu on ebatäpne, aegunud või muul viisil küsitav, valige see ja vajutage Ctrl + Enter.
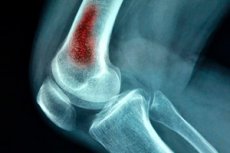
Üks kirurgilise infektsiooni eluohtlikumaid variante on äge hematogeenne osteomüeliit. See patoloogia ilmneb peamiselt lastel, ehkki täiskasvanud võivad haigestuda ka traumaatiliste vigastuste tagajärjel (püssist haavad, operatsioonijärgsed tüsistused jne). Patoloogia on mädane intraosseoosne protsess, mille põhjustab vereringesse sisenev nakkus. [1]
Epidemioloogia
Korpulentse hematogeense osteomüeliidi korral on luus mädane põletikuline protsess. See hõlmab medullaarseid struktuure, periosteumi ja kompaktset luukoe. Mõnikord muutub haigus mädase reaktsiooni leviku tagajärg luukoe suhtes lähedalasuvatest elunditest ja kudedest. Selline areng on iseloomulik odontogeensele osteomüeliidile, mis on põhjustatud hammaste kaarietest, ribide osteomüeliidi jaoks, mis on seotud pleura empüemaga, Panaricia põhjustatud phalangeaalse osteomüeliidi jaoks jne.
Enamikul juhtudest on põhjuslik aine Staphylococcus aureus või selle kombinatsioonid teiste patogeenidega - eriti Proteuse või Pseudomonas Bacillusega.
Ägeda hematogeenset osteomüeliiti peetakse valdavalt laste patoloogiaks. Patsientide peamine protsent (üle 95%) on koolieeliku ja algkooli vanuse lapsed. Selle selektiivsuse põhjus on lihtne ja on seotud luude troofilisuse ja struktuuri vanusega seotud anatoomiliste tunnustega, nimelt:
- Vere veresoonte võrgu tugev areng;
- Verevarustus epifüüsi, metafüüsi ja diafüüsi autonoomia;
- Suur hulk väikeseid veresoonte harukohti, mis kulgevad radiaalsel rajal läbi epifüüsi kõhre kuni luustude tuumani.
Metafüüsi vereringevõrk moodustub üle 2-aastastel lastel ja selle ajani on ülekaalus epifüüsi võrk. Need võrgud eksisteerivad üksteisest eraldi, kuid need on ühendatud anastomooside abil. Ühise veresoonte süsteemi moodustumine toimub siis, kui epifüüsi kasvupiirkond ossifitseerib. 2–3-aastastel patsientidel mõjutab metapifüüsi piirkondi, vanemas vanuses mõjutab probleem peamiselt diafüüsi.
Ägeda hematogeense osteomüeliidi diagnoositakse sagedamini 7–15-aastastel lastel, poistel - kolm korda sagedamini kui tüdrukutel. Ka täiskasvanu võib haigestuda, kuid see on palju vähem levinud.
Vastsündinute patoloogia areng on sageli seotud nabahaava nakatumisega. [2]
Põhjused äge hematogeenne osteomüeliit.
Sellise tõsise patoloogia nagu äge hematogeense osteomüeliidi moodustumine on patogeenide tungimine luuüdis, mis põhjustab mädase reaktsiooni tekkimist. Nakkuse fookused, millest patogeenid levisid läbi vereringe ja satuvad luu, võivad muutuda keskmise söötmeks, tonsilliitiks (mädaseks), furunculosis, suppuratiivseteks haavadeks. Ja patoloogia ei toimu kohe pärast esmast infektsiooni: kuud ja isegi aastad võivad mööduda.
Ägeda hematogeense osteomüeliidi peamine põhjuslik aine on Staphylococcus aureus: seda leidub umbes kaheksast kümnest patsiendist. Mõnel juhul on see kombineeritud infektsioon, sealhulgas Proteus ja Synegnaeus Bacillus.
Põletikulise protsessi intensiivsus on suuresti seotud luustruktuuri eripäradega. Põletikuline reaktsioon areneb medullaarses struktuuris, mida ümbritseb tihedama kortikaalsete seinte jäik keskkond. Sellistes tingimustes ei ole võimalust vähendada kudede rõhku põletikulist piirkonda laiendades, nii et reaktsioon levib vaskulaarse võrgu ja haversia kanalite kaudu piiramatult primaarse tsooni piiridest kaugemale.
Patoloogilise fookuse moodustumise hetkest võib osteomüeliiti pidada potentsiaalselt septiliseks protsessiks, mis hõlmab preemia ja sepsise etappe. [3]
Riskitegurid
Valdav enamus ägeda hematogeense osteomüeliidi juhtumeid esineb lastel ja noorukitel ning üldiselt nõrga immuunkaitsega patsientidel. Riskigrupid hõlmavad järgmisi kategooriaid:
- Koolieelikud ja põhikooli lapsed;
- Eakad isikud (üle kuuekümne aasta);
- Kaasasündinud või omandatud immuunpuudulikkuse tingimustega patsiendid;
- Septiliste seisunditega patsiendid;
- Vähihaiged;
- Patsiendid, kes kannatavad krooniliste nakkushaiguste patoloogiate all.
Kõik bakterite sissetungi sisemised allikad võib liigitada provotseerivateks teguriteks. See võib olla hambakaaries, tonsilliit (eriti mädane), põletiku kerimata fookused, aga ka mitmesugused eelsed tingimused. Olulist rolli mängib keha allergiline dispositsioon, immuunsuse langus mitmete profülaktiliste vaktsiinide, samuti trauma, hüpotermia ja stressirohkete olukordade samaaegse kasutuselevõtu tagajärjel. [4]
Pathogenesis
Ägeda hematogeense osteomüeliidi moodustumise patogeneetilist mehhanismi ei ole seni piisavalt uuritud. Eeldatavasti on patogeneesi peamised tegurid:
- Nakkusliku aine olemasolu kehas;
- Individuaalne luu anatoomia;
- Tugev immuunkompromiss.
Põletikulise vastuse tunnus ägeda hematogeense osteomüeliidi korral on selle kinnistamine luu kõva torus, mis hõlmab veresoonte võrgu tõsist kokkusurumist. Valusündroom muutub suurenenud rõhu tulemuseks medullaarses ruumis. Hüpertensiooni indikaator võib olla kuni 300–500 mm Hg (terve lapse norm on vahemikus 60–100 mm Hg).
Kui patoloogiat ei tuvastata luuüdi kanali põletikulise protsessi staadiumis, siis alates osteomüeliidi algusest alates neljandal või viiendal päeval hakkavad mädased massid levima Haversi ja Volkmanni süsteemi kaudu periosteumi, mille tulemusel see järk-järgult delaminiirub.
Kaheksandaks või kümnendaks päevaks jätkuvad mädased massid koos lagunemisproduktidega periosteumi delamineerudes, mille järel on mäda läbimurre pehmete kudede struktuuridesse. See viib intermuskulaarse ja nahaaluse flegmoni moodustumiseni. Väidetavalt on see olukord tähelepanuta jäetud haigus: hilise diagnoositud ägeda hematogeense osteomüeliidi ravi on keeruline ja pikk.
Valusündroom väheneb enamasti subperiosteaalse abstsessi spontaanse läbimurde taustal lähedalasuvatesse struktuuridesse, millega kaasneb medullaarses ruumis oleva rõhu järsk langus. [5]
Sümptomid äge hematogeenne osteomüeliit.
Sümptomatoloogia sõltub mingil määral patoloogilise protsessi vormist, mida saab lokaliseerida ja üldistada.
Lokaliseeritud kujul on valu raske, hajuv ja kontsentreeritud mõjutatud luu piirkonnas. Jäseme puudutamine või koputamine põhjustab äärmiselt ebameeldivaid aistinguid, motoorne aktiivsus on järsult piiratud, nahk põletiku piirkonnas on kuum, punakas, sageli turske.
Üldistatud kujul kombineeritakse kohalikud ilmingud üldisega. Jürgistamise märgid tõusevad, temperatuuri tõusevad, külmavärinad ja liigne higistamine toimub. Ürituste fookuste edasise leviku korral on olukord märkimisväärselt halvenenud. Võimalikud on mitu luukahjustust, mädase perikardiidi või mädase hävitava kopsupõletiku areng.
Ägeda hematogeense osteomüeliidi kohalikul käigus domineerivad kohalikud nähud, kuid need pole ainsad: joobeseisundi sümptomid esinevad igal juhul. Patsiendi küsitlemise käigus ilmnevad tingimata kaebused ebarahuldava üldhaiguse, külmavärinate, palaviku kohta. Väliselt juhitakse tähelepanu naha tursele, selle kahvatule või punetusele, nähtavale veresoonkonnale. Palpatoorselt tuvastatakse suurenev valulik piirkond, kui löökpillid üritades muutub valu eriti heledaks. [6]
Esimesed märgid
Äge hematogeenne osteomüeliit algab järsku, sageli - pärast traumat (isegi väikest) või mõnda muud provotseerivat tegurit (nt hüpotermia).
Peamine ja püsiv patoloogia märk on luuvalu, mis levib, valudest eriti intensiivseks. Valu takistab inimese magamist, muudab ta ärrituvaks, närviliseks. Reeglina levisid äärmiselt ebameeldivad aistingud kogu mõjutatud jäsemesse, kuid valu fookus saab sageli eksimatult tuvastada. Selline valusündroom on tingitud intraosseous rõhu suurenemisest luu kasvava põletikulise protsessi taustal. On tähelepanuväärne, et luuvalu iseloomustab püsivus.
Järgmine peamine märk ägeda osteomüeliidi korral on kõrge temperatuur. Esialgses patoloogilises staadiumis võivad näitajad olla vahemikus 37–38 ° C, kuid üldistatud osteomüeliidi tekkimisel tõuseb temperatuur järsult ja ühtlaselt 39–41 ° C-ni, millega mõnikord kaasneb palavik. Üldise hüpertermiaga samaaegselt on kahjustuse piirkonnas temperatuur kohalik tõus.
Haiguse kolmas esialgne märk on mõjutatud jäseme funktsionaalne häire. Patsient hakkab lonkama, motoorse aktiivsus on teravalt piiratud täieliku võimatuse punktiga. Isegi kahjustatud jäseme kerge liikumine põhjustab tugevat valu, mis sunnib inimest leidma sunnitud positsiooni maksimaalse võimaliku lihaste lõdvestumisega. Täpsemalt, kui puusa mõjutab, eelistab patsient jalga nii puusa- kui ka põlveliigestes: jäseme on pisut väljapoole pööratud. Kui see positsioon püsib pikka aega, võib tekkida paindumisliigese kontraktuur.
Seejärel paisusid tagajärjed umbes 48–96 tundi pärast ägeda osteomüeliidi algust. Aja jooksul levib ödeem teistesse kudedesse. Nahk patoloogilise fookuse kohal muutub pingeliseks, tihedaks. Mõjutab tõsiselt üldist heaolu. Raske patoloogia kulgemisega võib kaasneda haigusprotsessi levik teistesse luudesse.
Ägeda hematogeense osteomüeliidi kohalikud sümptomid
Äge hematogeenne osteomüeliit algab temperatuuri järsu tõusuga. Samal ajal ilmneb valu patoloogilise fookuse piirkonnas. Haige jäseme kaotab liikumisvõime, patsient üritab sellele sundpositsiooni anda. Piiratud pindala paisub, nahk omandab pastosity, palpeerimisel märgitakse kohalikku temperatuuri tõusu. Lühikese aja jooksul muutub paistes piirkond punaseks, märgitakse kõikumist.
Mikrosteoperforatsioon kinnitab intraosseous suurenenud rõhu olemasolu, mis võimaldab diagnoosi tuvastada isegi siis, kui luuüdi õõnsuses või periosteumi all puuduvad mädased massid. Mõnes olukorras on asjakohane teha diagnostiline luu punktsioon koos saadud materjali täiendava tsütoloogiaga.
Veretestid näitavad leukotsütoosi ja valemi vasakpoolset nihkumist, samuti toksilist neutrofiilide granulaarsust. Erütrotsüütide settekiirus suureneb märkimisväärselt ja see kasv on stabiilne. Samuti muutub vere valguspekter: seal on düsproteineemia, suurenenud globuliini fraktsioonid, hüpoalbumineemia. Pikaajalise osteomüeliidiga kaasneb tserebrospinaalse toksilise depressiooniga seotud aneemia.
Valu olemus ägeda hematogeense osteomüeliidi korral
Valu ägeda hematogeense osteomüeliidi korral:
- Tugev;
- Turvav;
- Intensiivistatud palpatsiooni ja koputades patoloogilisel alal;
- Mõne aja pärast muutub äärmiselt teravaks, väljakannatamatuks, vähimagi liikumise korral hetkelise süvenemisega.
Raske valu sündroomi tõttu võtab patsient sunniviisilise positsiooni, ta ei saa süüa ega magada, muutub ärrituvaks. Kui abi ei osuta, on olemas vaimne segadus, deliirium ja hallutsinatsioonid.
Klassifikatsioon
Sõltuvalt kursusest eristatakse ägedat ja kroonilist osteomüeliiti.
Patoloogia arengu mehhanism kajastub ka klassifikatsioonis:
- Endogeenne osteomüeliit (hematogeenne);
- Eksogeenne (trauma, kirurgilise sekkumise, püssilaskmise haava jne tagajärjel);
- Neurogeenne (kontaktkompressioon).
Sõltuvalt kliinilisest staadiumist eristuge:
- Äge osteomüeliit (kestab kuni 14–21 päeva);
- Alaäge (kuni 22-28 päeva);
- Krooniline (üle 28 päeva).
Haiguse ebatüüpilisi vorme esindab Brody abstsess, albumiinne osteomüeliit Ollier, skleroseeriv osteomüeliit Garre.
Kliinilise pildi kohaselt läbib äge hematogeenne osteomüeliit selliseid etappe:
- Patsiendi heaolu halveneb, isu kaotus, seletamatu apaatia.
- Seal on unetus, palavik, võimalikud düspepsia nähtused.
- Umbes 24 tunni pärast jõuab temperatuur kõrgele tasemele (umbes 39 ° C).
- Ristühendus suureneb, nahk muutub sinakaks kahvatuks. Valu hääldatakse, ägedad, aktiivsed liigutused puuduvad, passiivsed liigutused on tugevalt piiratud.
Kui patoloogiline fookus läbib, muutub nahk hüperoomiliseks, paraneb patsiendi seisund mõnevõrra. Võimalik on mitme luu fookuste moodustumine - umbes 1-2 nädalat pärast põhirõhku ilmumist.
Vormid
Ägeda mädase hematogeense osteomüeliidi patoloogilise fookuse lokaliseerimise piirkonna kohaselt on epifüüsi, metafüüsi, diafüüsi, käsnade, lamedate ja lühikeste luude kahjustustega. Patoloogilise protsessi teraapia sümptomatoloogia ja iseärasused sõltuvad nii patsiendi vanusest kui ka üldisest seisundist ning põletiku tsooni asukohast. Pikkade torukujuliste luude metafüüsi ja diafüüsi mõjutavad peamiselt koolieelsed ja nooremad kooliealised. Patoloogia pilt on mitmetahuline ja tihedalt seotud selliste teguritega nagu patogeense mikroorganismi immuunsuse ja virulentsus.
Ägeda hematogeense osteomüeliidi lokaalne vorm ei ole "puhas", kuna see ühendab nii kohalikud kui ka üldised ilmingud, ehkki kohalikud tunnused on mõnevõrra domineerivad. Luu piirkonnas on erksad valuvalud, juhib tähelepanu intensiivsele tursele (nahk on paistes, pinges). Koputamisel ilmneb patsiendil selge valuvastus. Kohalikul kujul võib mootori võimet mõnda aega säilitada.
Patoloogia mõjutab peamiselt pikki torukujulisi luid. Lamedad ja lühikesed luud mõjutavad palju harvemini. Enamikul juhtudel on luud mõjutatud:
- Reieluu (kuni 40% juhtudest);
- Sääreluu (umbes 30% juhtudest);
- Õlavarre (umbes 10%).
Palju harvemini leidub probleem jala, vaagna ja ülemises lõualuu luudes.
Pikkade torukujuliste luude ägeda hematogeense osteomüeliidiga on erinev jaotus. Seega saame rääkida järgmistest haiguse variantidest:
- Metadiafüüsi äge hematogeenne osteomüeliit - mõjutab metafüüsi ja enam kui 50% diafüüsist;
- Metapifüüsi äge hematogeenne osteomüeliit - mõjutab metafüüsi ja enamikku epifüüsist;
- Metafüüsi osteomüeliit - ulatub epifüüsi või diafüüsi servale;
- Kogu osteomüeliit - mõjutab diafüüsi ja mõlemat metafüüsi.
Ägeda hematogeense osteomüeliidi septikopieemiline vorm on haiguse eriti levinud variant, mis avaldub sepsise ägeda arengu abil. Mõnel patsiendil on märgitud väikest prodromaalset intervalli, mida iseloomustab väsimustunne, nõrkus, valu peas. Temperatuur tõuseb temperatuurini 39 ° C, märkimisväärsete igapäevaste kõikumistega 1,5–2 ° C. Valu kahjustuse piirkonnas ilmneb paar tundi pärast patoloogilise protsessi algust. Valusündroomil on rabelev iseloom, seda iseloomustab kõrge intensiivsus, patsient ei saa süüa ega magada, see on pidevalt sunnitud asendis, vältides igal võimalikul viisil mõjutatud jäseme puudutust. Üldine heaolu on äärmiselt kehv, rasked joobeseisundid on selged märgid. Kohalikke ilminguid tuvastatakse järk-järgult, valu lokaliseeritakse ainult teiseks päevaks, kuid puudutuse reaktsioon toimub peaaegu kohe. Turse ja kohalik pilt eristuvad ainult kolmandal või neljandal päeval. Kui arstiabi ei pöörata, täiendab turse piirkonda punetus ja kõikumine. Selle vormiga kaasneb sageli mädase-nakkusliku protsessi metastaasid, moodustudes mädaste fookuste (luustruktuurid, kopsud, neerud, maksa).
Ägeda hematogeense osteomüeliidi toksilist vormi (muud nimed - välk, adünaamika) iseloomustab kõige raskem kursus, domineerivate üldiste toksiliste ilmingutega. Patoloogia areneb kiiresti, hüpertermia on terav, ulatudes kiiresti kõrgete väärtusteni 40–41 ° C. on olemas eriline seisund, teadvuse võimaliku häirimise, pettuslik-hanlutsiineerivate episoodide raskusaste. Mõjutatud on südame aktiivsus: seal on tahhükardia, pulsi nõrk täidis, summutatud südametoonid. Sümptomatoloogia ebatüüpilisuse tõttu on seda vormi sageli keeruline diagnoosida. Patsiendi seisund on väga raske, mis teeb paljudel juhtudel võimatuks primaarse põletikulise fookuse.
Tüsistused ja tagajärjed
Ägeda hematogeense osteomüeliidi komplikatsioonid on kohalikud ja üldised.
Kohalike seas on kõige tavalisemad:
- Deformatsioonid, luudefektid;
- Patoloogilised luumurrud;
- Valeühenduste moodustumine;
- Anküloos;
- Mädane artriit, flegmonid;
- Osteomüelitsehaavandid;
- Fistuli seina pahaloomulisus.
Võimalikud tavalised tüsistused:
- Septilised tingimused;
- Neeru amüloidoos;
- Siseorganite düstroofia.
Kõige sagedasem komplikatsioon on sepsis: selle arengut märgitakse hilinenud või ebaõigete ravimeetmete korral.
Krolentse artriidi esinemine on tingitud nakkusliku aine levikust mõjutatud luust läbi lümfisüsteemi või mädase läbimurrega liigeseõõnsusesse.
Patoloogiline luumurd toimub mõjutatud luu hävitamise tõttu. Sel juhul moodustatakse mõnikord valeühendus - patoloogia, mida iseloomustab luu elemendi järjepidevuse ja liikuvuse stabiilne häirimine, mis pole konkreetse osakonna jaoks spetsiifiline.
Epifüüsi ja metafüüsi hematogeense patoloogia võib põhjustada luude häirimist ja luu raskeid moonutusi (lühenemist), mis on tingitud fookuse otsesest asukohast kasvutsooni lähedal. [7]
Diagnostika äge hematogeenne osteomüeliit.
Diagnostilised meetmed algavad kaebuste kogumisega ja anamnesise kogumisega.
Patsient kaebab palaviku, valu kahjustatud luu valu, halvenenud motoorse funktsiooni. Anamneesis võib esineda trauma, kirurgiliste sekkumiste ja muude nakkuslike fookuste esinemist kehas.
Füüsilise läbivaatuse käigus märkab patoloogilise fookuse projektsiooni piirkonnas valupesu ja löökpillide, temperatuuri, hüperemi ja turse valu suurenenud valu.
Testid näitavad põletikulise protsessi olemasolu kehas: veres on leukotsütoos, nihkumisega vasakule, samuti erütrotsüütide settekiiruse suurenemine. Uriinis esinevad valk, erütrotsüüdid ja silindrid.
Instrumentaalset diagnostikat esindavad järgmised uurimised:
- RADIOGRAAFIA - määratleb ägeda hematogeense osteomüeliidi tüüpilise pildi. See sisaldab: luu hägune pilt, luude risttalade virvendus ja seejärel luude hõrenemise ja paksenemise vahelduvad tsoonid, periosteaalne paksenemine. Ägeda hematogeense osteomüeliidi radioloogilisi tunnuseid tuvastatakse järk-järgult, 2-3 nädala jooksul pärast haiguse algust. Alguses tuvastatakse periosteumi irdumine periostiidi ilmingutega. Järgmisena moodustuvad metafüüsi tsoonis hõre kudede piirkonnad. 8-16 nädala pärast moodustuvad järjestused ja õõnsused.
- Ägeda hematogeense osteomüeliidi radioloogilist diagnoosimist saab fistulograafiaga täiendada kontrastiga. Tänu uuringule selgub luuõõnsuste täitmise aste ja ümbritsevad pehmete kudede struktuurid kontrastainega.
- Ultraheli aitab hinnata põletikulise reaktsiooni levikuastet pehmete kudede, tuvastada sekstraktsioone ja paraosseous mädane fookused.
- Angiograafiat kasutatakse avaskulaarsete luude segmentide tuvastamiseks ja flebotromboosi välistamiseks.
Põhjusava aine tuvastamiseks viiakse läbi eraldi bakterioloogiline uuring. Enamik patsiente on isoleeritud Staphylococcus aureusega, mõnevõrra harvemini Pseudomonas bacillus või proteusega, isegi harvemini enterobakterite või anaeroobidega. [8]
Diferentseeritud diagnoos
Diferentsiaaldiagnostika tehakse hematogeense ja posttraumaatilise osteomüeliidi vahel.
Hematogeenne põletik |
Traumajärgne põletik |
|
Nad haigestuvad sagedamini |
Laste- ja noorukieas patsiendid |
Enamasti täiskasvanud patsiendid |
Nakkuse tüüp |
Endogeenne-hematogeenne |
Eksogeenne |
Etioloogiline tegur |
Hematogeenne infektsioon |
Trauma koos nakkusega |
Domineeriv patogeen |
Staphylococcus aureus |
Cocci, Escherichia coli või pseudomonas, proteus, segainfektsioon |
Reaktiivne olek |
Keha reaktsioonivõime järsk suurenemine |
Keha normaalne reaktsioonivõime |
Morfoloogiline tegur |
Primaarne osteomüeliit |
Sekundaarne mädane ostiiit |
Sekvestreerimine |
Tõelised järjestused esinevad kogu patoloogilise protsessi vältel |
Pseudosekvestrid tekivad kõigepealt, tõesed hiljem |
Luumurd |
See on haruldane |
Kohal aluseks oleva patoloogiana |
Liigese nakatumine |
See on üsna tavaline nähtus |
Harva, ainult artikulaarse murdumise korral |
Septilised komplikatsioonid |
Sageli |
Harva |
Kellega ühendust võtta?
Ravi äge hematogeenne osteomüeliit.
Terapeutilised meetmed on kiireloomulised ja keerukad, need hõlmavad võimalikku mõju põhjustavale ainele, vältida septilisi komplikatsioone ja piiravad nakkuse lokaalset fookust. Oluline on leevendada joobeseisundit nii kiiresti kui võimalik, minimeerida elutähtsate elundite koormust, optimeerida patsiendi kaitsepotentsiaali ja valmistada ta ette eelseisvaks kirurgiliseks sekkumiseks. [9]
Esiteks on vaja kehatemperatuuri normaliseerida ja vältida tokseemia tekkimist, mis on lastel eriti oluline. Kasutage füüsikalisi jahutusmeetodeid, meditsiiniliselt laienege perifeerseid veresoone (drotaverine, papaveriin) ja vähendage temperatuuri (manustage 4% amidopüüriini 0,1 ml/kg koguses, 50% anaaliniini koguses 0,1 ml lapse eluaastas). Homöostaasi korrigeeritakse intravenoosse infusiooniga, et kõrvaldada hüpovoleemia ja stabiliseerida vee soola ja happe-aluse tasakaalu.
Infusioonravi alustatakse glükoosilahuse ning detoksikatsioonivõimega keskmise ja madala molekulmassiga polümeeride manustamisega (reopolüglukin, Hemodez jne), samuti valgulahuste (looduslik plasma, albumiin, veri). Vedelikumahtusid täiendatakse elektrolüütide lahustega. Actintiotilise oleku korrigeerimine toimub 4% naatriumvesinikkarbonaadi või trisamiini manustamisega. Düpepsia ja hüpokaleemiaga tõsise joobeseisundi korral manustatakse kaaliumkloriid. Kui on vaja kasutada spetsiaalseid tehnikaid, viiakse läbi hemosorptsioon - kehaväline vere puhastamine.
Kõige keerulisemad patsiendid võivad vahetada vereülekandes, asendades 1,5–2 mahtu ringlevat vere. Force Duuresis kasutatakse ka veekoormuse suurendamisel 5% glükoosilahusega, Ringer-Locke lahuse ning mannitooli ja Lasixi edasise manustamise korral.
Mõned patsiendid harjutavad edukalt plasmafereesi, kasutavad proteolüüsi inhibiitoreid (trasylol, kontseptsioon). Elistada hajutatud intravaskulaarne koagulatsiooni sündroom intravenoosselt hepariini manustada koguses 1-= 150 ühikut kg 6 tunni jooksul (mitte varem kui 12 tundi pärast operatsiooni). Kapillaaride läbilaskvuse vähendamiseks kasutatakse C-vitamiini, Rutini ja kaltsiumi sisaldavaid ravimeid.
Metabolismi aktiveerimiseks on ette nähtud pentoksool, metüüluratsiil, kaaliumorotaat. Immunoterapeutilised meetmed hõlmavad hüperimmuunse anti-stafülokoki plasma, stafülokoki vaktsiini ja hüperimmuunse anti-stafülokoki y-globuliini infusiooni.
Parenteraalset toitumist on kohustuslik, arvutamisel võttes arvesse soovitatud kalorite sisaldust ja valkude, rasvade, süsivesikute tasakaalu. Võimaluse korral kantakse patsient järk-järgult normaalse dieedi juurde.
Antibiootikumiravi viiakse läbi samaaegselt infusioonidega (intravenoosne, intramuskulaarne), samuti intraosseous (mõjutatud luu). Enne põhjustava aine tuvastamist manustatakse penitsilliini naatriumisoola intravenoosselt suurtes annustes. Intraosseus manustamine hõlmab antibiootikumide kasutamist laia aktiivsuse spektriga.
48 tundi pärast bakteriaalsete testide hindamist intraosseous süstimist, sõltuvalt resistentsusest: manustatakse tsefalosporiini ettevalmistusi, gentamütsiini, klaforan jne. Võimalik on täiendav süstimine 5 miljonit–10 miljonit penitsilliini ühikut 20 ml 0,25% nobokaiiniga reiearterisse.
Intraosseous süstimiseks mõeldud preparaadid jahutatakse temperatuurini +20 ° C.
Ägeda hematogeense osteomüeliidi lokaalne ravi
Kohaliku töötlemise peamine punkt on vähese intraosseous rõhu vähendamine ja patoloogilise protsessi edasise leviku ärahoidmine. Periostoomiat täiendavad spetsiifilised mikroskoopilised trepanatsioonid, mis võimaldavad õõnsust tühjendada ilma luustruktuuri häirimata.
Tehnika hõlmab järgmisi manipuleerimisi:
- Naha ja PJC lõikamine üle suurima valu;
- Lihaste eraldamine piki kiudu;
- Periosteum flegmoni avamine ja selle puudumisel - periosteumi dissektsioon;
- Perforatsiooniaukude täitmine spetsiaalsete jahvatuslõikurite abil, mille keskel on intraosseous antibiootikumravi keskus;
- Kipsi tükeldamine.
Kogu luukahjustusi tehakse ülaltoodud manipulatsioonid kahes metafüüsi piirkonnas. Operatsioonijärgses etapis on patsient riietatud ja uuritakse iga päev ning vajadusel viiakse läbi haavade redaktsioon. Kogu skeleti süsteemi uuritakse ka tõenäoliste sekundaarsete nakatunud fookuste õigeaegseks määramiseks. Kui selliseid fookuseid leitakse, viiakse läbi temperatuuri ja rõhu mõõtmistega luu punktsioon.
Füsioteraapiat saab rakendada, kui äge põletikuline protsess vaibub. On ette nähtud antibakteriaalsete ravimite elektroforeesis, UVA, ultrahigh-sagedusravi.
Umbes kuu aega hiljem viiakse läbi kontrollradiograaf ja hinnatakse ravi dünaamikat.
Ägeda hematogeense osteomüeliidi kirurgiline ravi
Kirurgiline sekkumine hematogeensesse osteomüeliidi on välja kirjutatud:
- Sekvestreerimine;
- Osteomüelitse luuõõnsus;
- Fistulid või haavandid;
- Muutused parenhmatoossetes elundites (osteomüeliidi tõttu);
- Lokaliseeritud pahaloomuline kasvaja.
Ägeda hematogeense osteomüeliidi operatsioon võib olla radikaalne, tavapäraselt radikaalne ja rekonstrueeriv.
Radikaalsed sekkumised hõlmavad neid:
- Mõjutatud luusegmendi marginaalne resektsioon;
- Pika luu osa lõppresektsioon keerulise traumaatilise osteomüeliidi korral;
- Pika luu osa segmentaalne resektsioon;
- Kahjustatud luuga segmendi disarticulation või eemaldamine.
Tingimuslikult radikaliseeritud sekkumised hõlmavad neid:
- Fistulosequestrectomia - hõlmab fistuli kanalite ekstsisiooni koos luude sekrestreerimisega;
- SequstRnecrektoomia - koosneb tihendatud kastist pärit sekstratsioonide resektsioonist pärast luude trepanatsiooni või luude õõnsuse eemaldamist navicular lamenemise kujul;
- FistulosequestRnecrektoomia (muu nimi: laiendatud nekrektoomia) - hõlmab nekroosi tüki, sekvestrumi, granuleerimise, fistuli või armkoe ekstsisiooni tervetes struktuurides;
- Pika torukujulise luu trepanatsioon sequstRnecrektoomiaga viiakse läbi, et pääseda luuüdi kanali tihendatud kastile, jätkates täiendavat selle avalikkust;
- Osteomüelitse fookuse eemaldamine, millele järgneb bilocal perkutaanne surve-destraction osteosünteesi, et asendada luudefekt.
Restaureerivad sekkumised hõlmavad hääldatud koedefektide asendamist ja need võivad olla järgmised:
- Pehmete kudede plast (klappülekanded);
- Plastist asendamine vaskulariseeritud koega;
- Kombineeritud tehnikad;
- Jääkõõne täitmine;
- Luuõõnsuste plastik verega toidetud kudedega (nt müoplastika);
- Asendusoperatsioon, kasutades Ilizarovi meetodit, aksiaalset osteosünteesi.
Ärahoidmine
Ennetamine seisneb varajases diagnoosimises, õigeaegse haiglaravi, täieliku terapeutilise ja kirurgilise ravi pakkumisel nakkushaigustega patsientidele. Vajadusel määrake antibiootikumiravi kursused, anti-stafülokoki plasma ja immuniseerimine stafülokoki anatoksiiniga, autovaktsia, retikulo-endoteeli süsteemi funktsioonide stimuleerimine. Provotseerivate tegurite agressiivse mõju, näiteks ümbritseva õhu temperatuuri (hüpotermia, ülekuumenemise), trauma jms võimaluse on kohustuslik välistada võimalus jne.
Vältige ägeda hematogeense osteomüeliidi tekkimist, vältides potentsiaalselt ebasoodsate tegurite mõju. Näiteks räägime omavahelistest nakkusprotsessidest, stressirohketest olukordadest, liigsest füüsilisest aktiivsusest, liigse külma või kuumuse teguritest.
Ühised terapeutilised sekkumised hõlmavad:
- Tervisliku eluviisi juhtimine;
- Täielik, mitmekesine ja kvaliteetne dieet;
- Stressirohkete olukordade vältimine;
- Regulaarne immuunsus;
- Nakkuslike fookuste õigeaegne kanalisatsioon;
- Õigeaegne otsimine vigastuste, traumade, haavade meditsiinilise abi otsimisel.
Oluline roll mängib ja vältida eneseravimist: patoloogiliste protsesside väljatöötamisel on kohustuslikud arstidega (nii suletud kui ka avatud) konsultatsioonid.
Prognoos
Kõik patsiendid, kes on läbinud ägeda hematogeense osteomüeliidi, on tingimata eraldatud rekordi. See on vajalik haiguse kordumise (ägenemise) õigeaegseks tuvastamiseks, ravi tulemuste hindamiseks, ennetav antibiootikumravi (näiteks kõige "ohtlikumatel" perioodidel - kevad ja langus). Haiguse kokkuleppe sõlminud inimene peaks külastama oma esmatasandi arst vähemalt kaks korda aastas.
Alates esimesest päevast pärast hematogeense osteomüeliidi kirurgilist sekkumist suurendab patsient järk-järgult motoorset aktiivsust:
- Lubage pöördeid voodi piirides;
- Teha hingamisharjutusi (staatilised ja dünaamilised harjutused);
- Soovitage torso tõsta, hoides samal ajal voodi kohal oleva vedrustuse seadme.
Taastusravi kiirendamiseks, troofiliste ja metaboolsete protsesside parandamiseks on ette nähtud füüsilised protseduurid - eriti magnetoteraapia ja UVB. Füsioteraapia terapeutiline kursus võib sisaldada viis kuni kümme protseduuri.
Üldiselt on ägeda hematogeense osteomüeliidi tingimuslik prognoos. Patsiendi võimalused taastuda ja lihas-skeleti mehhanismide funktsionaalsuse täielik taastamine sõltuvad patoloogilise protsessi astmest ja valitud ravi õnnestumisest, samuti kirurgilise ravi ajaliselt ja radikaalsusest.
Autoriteetsete raamatute ja uuringute loetelu ägeda hematogeense osteomüeliidi uurimisega
- "Luu- ja liigeseinfektsioonid: mikrobioloogiast diagnostika ja ravi" - autorid: W. Zimmerli, M. E. Corti (aasta: 2015)
- "Osteomüeliit: diagnoosimine, ravi ja prognoos" - autor Mahmut Nedim Doral (aasta: 2012)
- "Pediaatrilised osteoartikulaarsed infektsioonid" - autor: Pierre Lascombes, Antoine G. S. Lascombes (aasta: 2017)
- "Osteomüeliit: riskifaktorid, diagnoosimis- ja ravivõimalused" - autor Thore Zantop (aasta: 2016)
- "Osteomüeliit - meditsiiniline sõnaraamat, bibliograafia ja Interneti-viidete annoteeritud uurimisjuhend" - autor Icon Health Publications (Aasta: 2004)
- "Osteomüeliit: sümptomid, põhjused ja ravi" - autor Alton Carr (Aasta: 2012)
- "Osteomüeliidi uuringute edusammud" - autor Carlos A. Leonard (aasta: 2007)
- "Luu- ja liigeseinfektsioonid: bakterioloogiast diagnostika ja ravini" - autor Andreas F. Mavrogenis (aasta: 2018)
- "Kliinilise mikrobioloogiaprotseduuride käsiraamat, 1. kd" Autor: Amy L. Leber (aasta: 2016)
- "Osteomüeliit: Uued teadmised tervishoiuprofessionaalile: 2012. aasta väljaanne" - autor Q. Ashton Acton (aasta: 2012)
Kirjandus
Kotelnikov, G. P. Traumatoloogia / toimetanud Kotelnikov G. P., Mironov S. P. - Moskva: Geotar-Media, 2018.

