Artikli meditsiiniline ekspert
Uued väljaanded
A-hepatiidi viirus
Viimati vaadatud: 04.07.2025

Kõik iLive'i sisu vaadatakse meditsiiniliselt läbi või seda kontrollitakse, et tagada võimalikult suur faktiline täpsus.
Meil on ranged allhanke juhised ja link ainult mainekate meediakanalite, akadeemiliste teadusasutuste ja võimaluse korral meditsiiniliselt vastastikuste eksperthinnangutega. Pange tähele, et sulgudes ([1], [2] jne) olevad numbrid on nende uuringute linkideks.
Kui tunnete, et mõni meie sisu on ebatäpne, aegunud või muul viisil küsitav, valige see ja vajutage Ctrl + Enter.
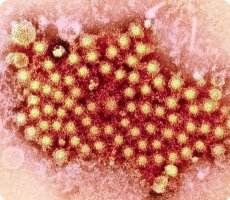
Viirushepatiit A on inimeste nakkushaigus, mida iseloomustab peamiselt maksakahjustus ning mis avaldub kliiniliselt joobe ja kollatõvena. A-hepatiidi viiruse avastasid 1973. aastal S. Feinstone (jt) immuun-elektronmikroskoopia meetodil, nakatades ahve - šimpanse ja marmosette. Immuun-elektronmikroskoopia meetodi olemus seisneb selles, et A-hepatiidiga patsiendi väljaheidete filtraadile lisatakse spetsiifilisi antikehi (paranemisseerumit) ja setteid uuritakse elektronmikroskoopia abil. Viiruste ja spetsiifiliste antikehade interaktsiooni tõttu toimub nende spetsiifiline agregatsioon. Sellisel juhul on neid lihtsam tuvastada ja antikehade mõjul toimuv agregatsioon kinnitab patogeeni spetsiifilisust. S. Feinstone'i avastust kinnitati vabatahtlikega tehtud katsetes.
A-hepatiidi viirus on kerakujuline, virioni läbimõõt on 27 nm. Genoomi esindab üheahelaline positiivne RNA, mille MD on 2,6 mm. Superkapsiidi ei ole. Sümmeetriatüüp on kuup-ikosaeeder. Kapsiidil on 32 kapsomeeri, see koosneb neljast polüpeptiidist (VP1-VP4). Oma omaduste järgi kuulub A-hepatiidi viirus perekonda Heparnovirus, sugukonda Picornaviridae. Antigeenide poolest on A-hepatiidi viirus (HAV - hepatiit A viirus) homogeenne. HAV paljuneb hästi šimpanside, paavianide, hamadrya paavianide ja marmoset-ahvide kehas. Pikka aega ei olnud viirust võimalik kultiveerida. Alles 1980. aastatel õnnestus saada rakukultuure, milles HAV paljuneb. Algselt kasutati nendel eesmärkidel reesusmakaagi embrüoneeru neeru pidevaid rakuliine (kultuur FRhK-4) ja nüüd kasutatakse rohelise ahvi neerurakkude pidevat rakuliini (kultuur 4647).
WHO ekspertide soovituste kohaselt on vastu võetud järgmine A-hepatiidi viiruse markerite nomenklatuur: A-hepatiidi viirus - A-hepatiidi viiruse vastased HAV-antikehad: anti-HAV IgM ja anti-HAV IgG.
HAV on väike osake läbimõõduga 27–30 nm, millel on ikosaeedriline sümmeetria ja homogeensus. Immuunagregatsiooni meetodil saadud elektronogramm näitab elektrontihedaid osakesi, millel on pinnal paiknevad sümmeetriliselt paigutatud kapsomeerid. Negatiivse kontrasti korral on preparaatides näha nii täis- kui ka tühje osakesi. HAV-i nukleokapsiidil, erinevalt gripiviirusest, puuduvad pinnaeemad ja membraan. Samuti on oluline, et HAV-virioonil ei oleks südamekujulist struktuuri.
Oma füüsikalis-keemiliste omaduste põhjal liigitatakse A-hepatiidi viirus pikornaviiruste perekonda, enteroviiruse perekonda seerianumbriga 72. See taksonoomia osutus aga liiga ebatavaliseks ja WHO pidas võimalikuks säilitada terminoloogia „A-hepatiidi viirus”.
Nagu kõik Picornaviridae perekonna viirused, sisaldab ka A-hepatiidi viirus ribonukleiinhapet. Mõned laborid on näidanud A-hepatiidi viiruse genoomi kloonimise võimalust, mis avab võimaluse vaktsiinide saamiseks.
A-hepatiidi viiruse resistentsus
Viirus on suhteliselt vastupidav kõrgetele temperatuuridele, hapetele, rasvalahustitele (lipiidid puuduvad), desinfitseerimisvahenditele ja talub hästi madalaid temperatuure. Kõik see aitab kaasa selle pikaajalisele säilimisele väliskeskkonnas. Toatemperatuuril säilib see mitu nädalat, 60 °C juures kaotab see osaliselt oma nakkavuse 4–12 tunni pärast ja täielikult mõne minuti pärast 85 °C juures. See on väga vastupidav kloorile, tänu millele suudab see tungida kraanivette läbi veepuhastusjaamade barjääride.
Kõiki andmeid kokku võttes saame A-hepatiidi viirust iseloomustada järgmiselt:
- loomulik peremeesorganism on inimene;
- katseloomad - marmosetid, šimpansid;
- nakkusallikas on väljaheited;
- haigus on epideemiline ja endeemiline;
- ülekandetee: feko-oraalne;
- inkubatsiooniperiood - 14-40 päeva;
- üleminek kroonilisele hepatiidile - ei täheldatud.
HAV-i immunoloogilised omadused on järgmised:
- Prototüüpsed tüved - Ms-1, CR-326, GВG. Kõik on immunoloogiliselt sarnased või identsed;
- Antikehad - IgM ja IgG - tekivad vastusena viiruse struktuurvalkude sissetoomisele ja on kaitsvad;
- I. Inimese seerumi gammaglobuliini kaitsev toime – ennetab või leevendab haigust, kui seda manustatakse enne nakatumist või inkubatsiooniperioodil.
NAU füüsikalis-keemilised omadused on järgmised:
- Morfoloogia: kooreta sfääriline kuubilise sümmeetriaga osake, kapsiid koosneb 32 kapsomeerist;
- Läbimõõt - 27-30 nm;
- Tihedus CsCl-is (g/cm3) - 1,38-1,46 (avatud osakesed), 1,33-1,34 (küps virion), 1,29-1,31 (ebaküpsed virionid, tühjad osakesed);
- Sedimentatsioonikoefitsient - 156-160 küpset virioni;
- Nukleiinhape on üheahelaline lineaarne RNA;
- Suhteline molekulmass - 2,25 × 106–2,8 × 106 KD;
- Nukleotiidide arv on 6500–8100.
HAV stabiilsus füüsikaliste ja keemiliste mõjude all on järgmine:
- Kloroform, eeter - stabiilne;
- Kloor, 0,5–1,5 mg/l, 5 °C, 15 min – osaline inaktiveerimine;
- Kloramiin, 1 g/l, 20 °C, 15 min – täielik inaktiveerimine;
- Formaliin, 1:4000, 35–37 °C, 72 tundi – täielik inaktiveerimine, 1:350, 20 °C, 60 minutit – osaline inaktiveerimine.
Temperatuur:
- 20–70 °C – stabiilne;
- 56 °C, 30 min - stabiilne;
- 60 °C, 12 tundi - osaline inaktiveerimine;
- 85 °C, 1 min - täielik inaktiveerimine;
- Autoklaavimine, 120 °C. 20 min - täielik inaktiveerimine;
- Kuivkuumutus, 180 °C, 1 tund - täielik inaktiveerimine;
- UFO, 1,1 W, 1 min - täielik inaktiveerimine.
Esitatud andmed näitavad, et oma füüsikalis-keemiliste omaduste poolest on A-hepatiidi viirus kõige lähedasem enteroviirustele. Nagu teisedki enteroviirused, on HAV resistentne paljude desinfitseerimislahuste suhtes ning inaktiveeritakse täielikult mõne minuti jooksul temperatuuril 85 °C ja autoklaavimisel.
On tõestatud, et A-hepatiidi viirus on võimeline paljunema nii inimese kui ka ahvi rakukultuuride primaarsetes ja pidevates monokihilistes liinides. A-hepatiidi viiruse eriti aktiivset paljunemist in vitro kultuurides täheldatakse haigete ahvide maksaekstraktide kasutamisel lähtematerjalina. Siiski tuleb märkida, et kõigis A-hepatiidi viiruse paljunemise katsetes in vitro kultuurides pööratakse tähelepanu pikale inkubatsiooniperioodile primaarsete passaažide ajal (kuni 4–10 nädalat), mille järel viiruse geneetilise materjali akumuleerumine suureneb, kuid absoluutväärtused jäävad väga ebaoluliseks, mis annab paljudele teadlastele alust rääkida A-hepatiidi viiruse mittetäielikust replikatsioonist koekultuurides.
Kokkuvõttes kirjanduse andmeid A-hepatiidi viiruse paljunemise kohta koevälistes kultuurides, võib öelda, et HAV-i pikaajaline ellujäämine in vitro on vaieldamatu. Viiruse stabiilse ja kõrge replikatsioonitaseme optimaalseid tingimusi pole lõplikult kindlaks tehtud ning see takistab selle bioloogiliste omaduste uurimist, diagnostikavahendite tootmiseks vajalike reagentide allika saamist ja vaktsiinide disainimist.
Samal ajal võib kirjandusest leida selle probleemi kohta optimistlikumaid hinnanguid. Kõigi A-hepatiidi viiruse kultiveerimisega seotud küsimuste lahendus on lähituleviku küsimus. Reesusmakaagi embrüonaalsete neerurakkude kultuuris HAV-i paljunemise optimaalsete tingimuste uurimisel tuvastati kaks faasi: nakkusliku viiruse tootmise faas (kuni 6-8 päeva 5. passaaži tasemel) ja viirusantigeeni intensiivse akumuleerumise faas. Samuti näidati, et viirusantigeeni kõige olulisem akumuleerumine toimub nn rullkultiveerimise tingimustes (pöörlevad kolvid). See meetod avab laialdased võimalused kultuurilise antigeeni saamiseks suurtes kogustes ja sellest tulenevalt tekib lähtematerjal diagnostiliste süsteemide valmistamiseks ja vaktsiinide tootmiseks.
A-hepatiidi epidemioloogia
A-hepatiidi viirus on inimestele väga patogeenne. WHO (1987) andmetel piisab haiguse tekitamiseks nakatumisest vaid ühe virioniga. Praktiline nakkusdoos on aga tõenäoliselt palju suurem. Ainus nakkusallikas on nakatunud inimene. Viirus eritub suurtes kogustes väljaheitega 12-14 päeva enne kollatõve algust ja ikterilise perioodi 3 nädala jooksul. Patogeeni eritumises A-hepatiidi ikterilise, anikterilise ja asümptomaatilise vormiga patsientidel ei ole leitud olulisi erinevusi. Nakatumistee on fekaal-oraalne, peamiselt vee, samuti olme- ja toidu kaudu. Nakatumistee on fekaal-oraalne, peamiselt vee, samuti olme- ja toidu kaudu. Viiruse peamine (esmane) edasikandumise tee on vee kaudu. Samuti on võimalik nakatuda õhus levivate piiskade kaudu. Elanikkonna vastuvõtlikkus on universaalne. Enamasti haigestuvad alla 14-aastased lapsed. Haigusel on väljendunud sügis-talvine hooajalisus.
 [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ]
[ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ]
A-hepatiidi sümptomid
Inkubatsiooniperiood varieerub 15 kuni 50 päeva, olenevalt viiruse nakkavast annusest, kuid keskmiselt on see 28-30 päeva. Organismis paljunedes paljuneb A-hepatiidi viirus piirkondlikes lümfisõlmedes, tungib verre ja seejärel maksarakkudesse ning põhjustab ägedat difuusset hepatiiti, millega kaasneb hepatotsüütide ja maksa retikuloendoteliaalsete elementide kahjustus ning selle detoksifitseerimis- ja barjäärifunktsioonide vähenemine. Hepatotsüütide kahjustus ei teki viiruse otsese toime, vaid immunopatoloogiliste mehhanismide tulemusena. A-hepatiidi kõige tüüpilisem pilt on äge ikteriline tsükliline vorm: inkubatsiooniperiood, prodromaalne (preikteriline), ikteriline periood ja paranemisperiood. Infektsioonikolletes avastatakse aga suur hulk anikteriliste ja asümptomaatiliste infektsioonivormidega patsiente, kelle arv domineerib oluliselt ikteriliste vormide ees ("jäämäe fenomen").
Infektsioonijärgne immuunsus on tugev ja pikaajaline, selle tekitavad viirust neutraliseerivad antikehad ja immuunmälurakud.
A-hepatiidi mikrobioloogiline diagnostika
A-hepatiidi diagnostika (välja arvatud loomade - šimpanside, marmosettide, paavianide - nakatumine, mida meil pole) põhineb erinevatel immunoloogilistel meetoditel: RSC, immunofluorestsentsmeetod, immuunadhesiooni hemaglutinatsioon (viirusantigeeni + antikeha kompleks komplemendi juuresolekul adsorbeerub erütrotsüütidele ja põhjustab nende kleepumist). Nende meetodite kasutusvõimalused on aga piiratud spetsiifiliste viirusantigeenide puudumise tõttu ning immunofluorestsentsreaktsioon nõuab maksa biopsiat, mis on ebasoovitav. Immuunelektronmikroskoopia meetod on usaldusväärne ja spetsiifiline, kuid väga töömahukas. Seetõttu on seni ainus vastuvõetav immunoloogiline reaktsioon tahke faasi immunosorbentanalüüsi meetod IFM-i või RIM-i kujul, eriti M-klassi immunoglobuliinide "püüdmise" modifikatsioonis. Meie riigis on selleks otstarbeks välja pakutud testsüsteem - "DIAGN-A-HEP". Selle testsüsteemi toimimise põhimõte on järgmine. Esmalt adsorbeeritakse polüstüreenist süvendite seintele M-klassi immunoglobuliinide (antiimmunoglobuliinid M) vastased antikehad, seejärel lisatakse testitav patsiendi seerum. Kui see sisaldab IgM-antikehi, seonduvad need M-klassi antikehadega, seejärel lisatakse spetsiifiline viirusantigeen (A-hepatiidi viirus), mis saadakse rakukultuuris kasvatamise teel. Süsteemi pestakse ja sellele lisatakse mädarõikaperoksidaasiga märgistatud viirusevastased antikehad. Kui kõik neli süsteemi komponenti omavahel interakteeruvad, moodustub neljakihiline "võileib":
- antiimmunoglobuliinid M,
- immunoglobuliinid M (A-hepatiidi viiruse vastu - uuritava patsiendi seerumis),
- viiruse antigeen,
- ensüümidega märgistatud viirusevastased antikehad.
Selle kompleksi tuvastamiseks lisatakse süvenditesse ensüümi substraat. Ensüümi mõjul see laguneb ja moodustub värviline produkt. Värvuse intensiivsust saab kvantitatiivselt mõõta spektrofotomeetri või fotokolorimeetri abil.
IgM "püüdmis" meetodi eeliseks on see, et selle immunoglobuliinide klassi antikehad ilmuvad primaarse immuunvastuse ajal ja näitavad nakkuse aktiivset staadiumi, kaovad pärast haiguse läbipõlemist. IgG klassi kuuluvad viirusevastased antikehad seevastu püsivad pikka aega pärast haiguse läbipõlemist, pakkudes omandatud immuunsust. A-hepatiidi viiruse tuvastamiseks on välja pakutud DNA-sondi meetod: sondina kasutatakse komplementaarset vRNA DNA-d.
A-hepatiidi spetsiifiline ennetamine
Varem laialdaselt kasutatud A-hepatiidi seroprofülaktika gammaglobuliiniga ei õigustanud ennast, seetõttu pandi põhirõhk vaktsineerimisprofülaktika läbiviimisele, viiakse läbi A-hepatiidi vastast vaktsineerimist. Sel eesmärgil töötatakse välja ja kasutatakse juba mitmesuguseid vaktsiine. Venemaal saadi efektiivne A-hepatiidi vaktsiin juba 1995. aastal ja seda kasutatakse nüüd edukalt.

