Artikli meditsiiniline ekspert
Uued väljaanded
Lõualuu ameloblastoom
Viimati vaadatud: 04.07.2025

Kõik iLive'i sisu vaadatakse meditsiiniliselt läbi või seda kontrollitakse, et tagada võimalikult suur faktiline täpsus.
Meil on ranged allhanke juhised ja link ainult mainekate meediakanalite, akadeemiliste teadusasutuste ja võimaluse korral meditsiiniliselt vastastikuste eksperthinnangutega. Pange tähele, et sulgudes ([1], [2] jne) olevad numbrid on nende uuringute linkideks.
Kui tunnete, et mõni meie sisu on ebatäpne, aegunud või muul viisil küsitav, valige see ja vajutage Ctrl + Enter.
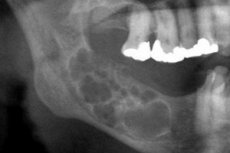
Hambakoe kasvaja – ameloblastoom – on epiteliaalse iseloomuga ja kaldub agressiivselt kasvama. Kasvaja ei ole pahaloomuline, kuid võib põhjustada luukoe hävimist ja harvadel juhtudel metastaseeruda. Ravi on kirurgiline: operatsiooni ulatus sõltub peamiselt patoloogia staadiumist. [ 1 ]
Epidemioloogia
Ameloblastoomi esineb nii meestel kui naistel ligikaudu võrdse sagedusega. See moodustab umbes 1% kõigist suuõõne kasvajatest ja umbes 9–11% odontogeensetest kasvajatest. Tavaliselt on see aeglaselt kasvav, kuid lokaalselt invasiivne kasvaja. [ 2 ] Patsientide keskmine vanus on kakskümmend kuni viiskümmend aastat. Kasvaja ilmnemine on võimalik ka lapsepõlves ja noorukieas, kuigi see juhtub palju harvemini – ainult 6,5%-l patsientidest, kellel on lõualuu healoomulised kasvajad.
Enamikul juhtudel mõjutab ameloblastoom alumist lõualuu (80–85%) ja palju harvemini ülemist lõualuu (15–20%):
- kõige sagedasem kahjustus on alalõua nurk ja haru;
- 20% juhtudest on keha mõjutatud suurte molaaride küljelt;
- 10% juhtudest on mõjutatud lõua piirkond.
Naistel on sagedasem siinus-nina süsteemi ameloblastoom, mis moodustub prolifereeruvast odontogeensest epiteelist. Patoloogia võib olla polütsüstiline ja monotsüstiline, mis nõuab tsüstidega kõige täpsemat diferentsiaaldiagnostikat.
Hambaid põhjustavate kasvajate esinemissagedus on kõigist näo-lõualuu piirkonda mõjutavatest kasvajaprotsessidest vahemikus 0,8–3,7%. Nende hulgas on domineerivad odontoomid (üle 34%), ameloblastoomid (umbes 24%) ja müksoomid (umbes 18%). [ 3 ]
Ameloblastoom on peaaegu 96–99% juhtudest healoomuline. Pahaloomulist kasvajat täheldatakse vaid 1,5–4% patsientidest. [ 4 ]
Ameloblastoomi teised nimetused on adamantblastoom, adamantinoom (sõnast email – substantia adamantina).
Põhjused ameloblastoomid
Spetsialistide seas puudub ameloblastoomi tekke põhjuste osas üksmeel. Mõned teadlased seostavad patoloogiat hambaidu moodustumise häirega, teised aga odontogeensete epiteelijäänustega. Kasvajaprotsessi päritolu küsimusele pole aga selget vastust ning riskifaktorid on teadmata.
Kasvaja nimetus tuleneb inglise ja kreeka sõnade kombinatsioonist: "amel" – email ja "blastos" – rudiment. Patoloogia areneb hambaplaadi epiteelist, seda iseloomustab lokaalne agressiivne kasv ja suur kordumise oht. [ 5 ]
Kasvajat kirjeldas esmakordselt dr Cusack 1827. aastal. Peaaegu 60 aastat hiljem kirjeldas teine teadlane Malassez haigust, millele ta pani nimeks adamanthinoma. Tänapäeval kasutatakse seda terminit haruldase primaarse pahaloomulise luukasvaja kirjeldamiseks. Kuid nimetus ameloblastoom võeti meditsiinilises kasutuses esmakordselt kasutusele alles 1930. aastal ja seda kasutatakse tänapäevalgi.
Ameloblastoom on tõeline healoomuline kahjustus, mis koosneb prolifereeruvast odontogeensest epiteelist, mis on kinnistunud kiulise strooma sisse.
Pathogenesis
Ameloblastoomi arengu etioloogiat ei ole täielikult mõistetud. Eksperdid usuvad, et neoplasmi kasv algab suuõõne rakustruktuuridest või Malasset'i epiteeli saartest, üleliigsete hammaste algetest või hambaplaadi ja hambakottide hajutatud rakukompleksidest.
Lõikel on ameloblastoomil iseloomulik roosakas-hallikas toon ja käsnjas struktuur. Põhistruktuuri esindab kiuline sidekude, mis on rikastatud spindlikujuliste rakkude ja odontogeensete epiteeli ahelate harudega. Iga ahela lähedal paiknevad silindrilised epiteelirakud ja siseküljel külgnevad nendega hulknurksed struktuurid, mis muutuvad tähtkujulisteks.
Lisaks märgitakse ebakorrapäraselt konfigureeritud rakulisi struktuure: need on peamine erinevus ameloblastoomi ja emailitud organi vahel. Tsüstilised intratumoraalsed moodustised kahjustavad epiteelirakke, seega mikroskoopilisel uurimisel on täheldatud ainult silindrilisi perifeerseid rakke.
Ameloblastoomi destruktiivsete tsoonide suurus ulatub kolmest millimeetrist kuni mitme sentimeetrini. Rasketel juhtudel levib kasvaja kogu lõualuusse. [ 6 ]
Praegu räägivad eksperdid ameloblastoomi ilmnemise mitmest patogeneetilisest teooriast. Neist ainult kahel on suurim põhjendus:
- A. Abrikosovi teooria kohaselt algab kasvajalise protsessi areng hamba moodustumise perioodil emaili staadiumis. Tavaliselt toimub pärast hamba lõikumist emaili pöördvõrdeline areng. Kuid häirete korral see säilib ja vohab: see põhjustab ameloblastoomi teket.
- V. Braitsevi ja N. Astahovi teooria viitab epiteelkoe jäänuste kaasatusele luus ja parodondis (Malyasse saared). See oletus on usutav esiteks seetõttu, et ameloblastoomi iseloomustab suur histoloogiline mitmekesisus. Lisaks leiti diagnostika käigus paljude patsientide kasvajates sarnaseid emaili struktuure.
On ka teisi teooriaid, mida pole hetkel piisavalt uuritud. Näiteks kaalutakse sidekoe metaplaasia hüpoteesi ja ülalõuaurke epiteeli proliferatsiooni oletust.
Sümptomid ameloblastoomid
Ameloblastoomi peamine sümptom, millega patsiendid pöörduvad arsti poole, on lõualuu kuju asümmeetria ja moonutus, mille ilmingud esinevad erineva raskusastmega. Kõige sagedamini ilmub lõualuu piirkonda omapärane eend või turse. Kui kasvaja paikneb piki alalõua keha ja haru, täheldatakse kogu näo alumise külgmise osa deformatsiooni.
Kasvaja palpeerimine võimaldab tuvastada sileda või konarliku pinnaga tihenemist. Hilisemates staadiumides, luukoe hõrenemise taustal, on sõrmedega vajutamisel täheldatud selle painutamist. Ameloblastoomi kohal olev nahk on normaalse välimusega, värvus ja tihedus ei muutu, moodustavad kergesti voldi ja liiguvad. Suuõõne uurimine võimaldab märgata alveolaarprotsessi konfiguratsiooni rikkumist. [ 7 ]
Kui tegemist on ülalõua ameloblastoomiga, siis võib välimus vaid veidi kannatada, kuna kasvaja kasvab siinusesse. Siiski täheldatakse kõva suulae deformatsiooni ja on ka märkimisväärne tõenäosus protsessi levikuks silmakoopa ja ninaõõnde. [ 8 ]
Üldiselt võib kliinilist pilti iseloomustada järgmiste sümptomitega:
- valu, mis suureneb luukoe kahjustuse tekkimisega;
- lõualuu liikuvuse halvenemine;
- hambad lahti, hammaste ebaühtlus;
- neelamisraskused, närimine, haigutamine;
- ebameeldivad helid alalõualuu liikumise ajal, mis on põhjustatud kortikaalse plaadi hõrenemisest;
- haavandumine, limaskestade verejooks neoplasmi piirkonnas;
- submandibulaarsetest lümfisõlmedest ei ole vastust.
Kui tüsistusena tekib mädane põletikuline reaktsioon, siis täheldatakse flegmoni või ägeda osteomüeliidi iseloomulikke tunnuseid. [ 9 ]
Ameloblastoomi tekke algstaadiumis ei tunne inimene tavaliselt midagi ebameeldivat. Kasvaja progresseerub üsna aeglaselt, kuna selle kasv on suunatud ülalõuaurke õõnsusse. Umbes kuue kuu pärast sellist järkjärgulist arengut on juba võimalik tuvastada lõualuu konfiguratsiooni häireid. Välimus on häiritud ja funktsioon kannatab. Ameloblastoomi lokaliseerimise piirkonnas on täheldatud silutud või muguljat spindlikujulist eendu, mis põhjustab alveolaarprotsessi kuju muutust ja sellele järgnevat närimishammaste lõdvenemist.
Patoloogiliste protsesside tagajärjel tunneb patsient valu ja ebameeldivat klõpsatust alalõualuu liigutamisel oimusluu piirkonnas. See põhjustab probleeme närimise ja toidu neelamisega. [ 10 ]
Kasvaja moodustumise edasise kasvuga tekib mädane põletikuline reaktsioon, millega võib kaasneda suuõõnde viiva fistuli teke. Kui selleks ajaks pole patsient saanud kvalifitseeritud kirurgilist abi, suureneb haigusprotsessi edasise leviku oht silmakoopa ja ninaõõnde.
Mõnel juhul võivad suuõõne limaskestadele ilmuda mädase sisuga fistulid. Pärast hamba väljatõmbamist tekkinud haavad paranevad raskesti. Kasvajakolde punkteerimisel leitakse hele, hägune kolloidne aine või kollakas aine, mis võib sisaldada kolesterooli kristalle.
Ameloblastoom kipub nakatuma, seega peaksite võimalikult kiiresti arsti poole pöörduma. [ 11 ]
Ameloblastoom lastel
Lapsepõlves esineb ameloblastoom 6-7% kõigist healoomulistest lõualuu kasvajatest. Patoloogiat diagnoositakse kõige sagedamini 7-16-aastaselt, kusjuures valdav lokaliseerumine on alalõua haru ja nurga piirkonnas. Neoplasmi põhjused jäävad uurimata.
Arengu algstaadiumis laps kaebusi ei esita. Harvemini esineb valusid, mida hinnatakse hambavaludeks. Hilisemates staadiumides ilmnevad raskused ninahingamisel, nägemishäired, pisaravool ja muutused kasvaja küljel oleva naha tundlikkuses. Arsti poole pöördumine on vajalik peamiselt pärast näo ja lõualuude deformatsioonide avastamist.
Lastel täheldatakse ameloblastoomi pahaloomulisust äärmiselt harvadel juhtudel – näiteks pikaajalise ebaõige ravi korral. Ravi on ainult kirurgiline: kasvaja eemaldatakse tervete kudede sees (10–15 mm kaugusel kasvajast). [ 12 ]
Vormid
Eksperdid jagavad ameloblastoomi järgmistesse tüüpidesse:
- Tahke ameloblastoom.
- Tsüstiline ameloblastoom:
- unitsüstiline;
- polütsüstiline.
Alumise lõualuu ameloblastoomi esindab kõige sagedamini kasvaja polütsüstiline variant, mis kasvab odontogeense epiteeli osakestest.
Makroskoopiliselt uurides on tahke kasvaja lahtise roosakas-hallika moodustisega, mõnes kohas pruunika varjundiga. Mikroskoopilisel uurimisel on võimalik tuvastada tsüste. [ 13 ]
Tsüstilise ameloblastoomi puhul on üks või mitu omavahel ühendatud õõnsust - sileda seinaga või kergelt konarlikud, mis on eraldatud pehmete kudede kihtidega, mis on täidetud helepruuni või kolloidse sisuga. Histoloogilise uuringu käigus leitakse enamasti tsoonid, mis on paigutatud analoogselt tahke kasvajaga.
Seega võib ameloblastoomi struktuuris leida nii tihedaid kui ka tsüstilisi tsoone. Mõned spetsialistid usuvad, et haiguse erinevad tüübid on lihtsalt kasvaja moodustumise erinevad staadiumid. [ 14 ]
Tsüstiline variant sisaldab rohkem parenhüümialasid ja vähem stroomat. Esineb mitmeid erineva suuruse ja konfiguratsiooniga tsüstilisi õõnsusi, samuti luuvaheseinu. Tsüstide sees leidub viskoosset vedelikku, mis mõnikord sisaldab kolesterooli kristalle.
Patoloogia tahket vormi esindavad stroom ja parenhüüm, millel on kapsel. Stroom on sidekude koos veresoonte ja rakkudega. Parenhüüm koosneb epiteelkoe kiududest, mis on altid proliferatsioonile. [ 15 ]
Ülalõualuu ameloblastoom on üsna haruldane ja peaaegu kunagi ei avaldu lõualuu seina defektina, mis on seotud kasvaja kasvuga ülalõualuu siinuse õõnsusse. Kui aga kasv toimub ninaõõnes või silmakoobas, siis täheldatakse kõva suulae ja alveolaarjätke konfiguratsiooni rikkumist ning silmamuna nihkumist.
Sõltuvalt mikroskoopilistest omadustest jaguneb mandibulaarne ameloblastoom järgmisteks alatüüpideks:
- follikulaarne ameloblastoom - sisaldab stroomas omapäraseid folliikuleid ehk epiteeli saarekesi;
- pleomorfne – sisaldab epiteelikiudude võrgustikku;
- akantomatoosne - iseloomustab keratiini moodustumine kasvajarakkude piirkonnas;
- basaalrakuline - omab basaalrakulise kartsinoomi iseloomulikke tunnuseid;
- granuleeritud rakk - sisaldab epiteelis atsofiilseid graanuleid.
Praktikas avastatakse kõige sagedamini kahte esimest tüüpi neoplasmi: follikulaarne ja pleomorfne vorm. Paljudel patsientidel on ühes kasvajas kombinatsioon mitmest histoloogilisest variandist.
Tüsistused ja tagajärjed
Ameloblastoom on altid korduma isegi mitu aastat pärast selle eemaldamist. Ligikaudu 1,5–4% juhtudest on võimalik pahaloomulisus, mis avaldub moodustise kiirenenud kasvus ja idanemises lähedalasuvatesse kudedesse.
Kohesteks postoperatiivseteks tagajärgedeks on valu ja turse, mis kaovad iseenesest mõne päeva jooksul. Valu võib levida lõualuudesse, hammastesse, pähe ja kaela. Kui ebamugavustunne ei kao nädala jooksul, vaid süveneb, peaksite kindlasti pöörduma arsti poole. [ 16 ]
Muud võimalikud postoperatiivsed tüsistused:
- põletikulised protsessid;
- neuriit;
- paresteesia (tuimus, põskede, keele, lõualuude tundlikkuse kaotus);
- hematoomid, pehmete kudede abstsessid.
Põletikulised protsessid võivad areneda ebapiisavate antiseptikumide või ebaõige operatsioonijärgse hoolduse tõttu (näiteks kui toit satub haava).
Te peaksite viivitamatult pöörduma arsti poole, kui:
- mõne päeva jooksul turse ei kao, vaid suureneb;
- valu muutub intensiivsemaks ja valuvaigistid muutuvad ebaefektiivseks;
- kehatemperatuur tõuseb mitme päeva jooksul;
- isukaotuse taustal ilmneb üldine nõrkus ja iiveldus.
Kasvu käigus moonutab kasvaja hambarida ja lõualuu. Juhtub, et ameloblastoom mädaneb, tekib pehmete kudede turse, mida võib komplitseerida fistulite teke. [ 17 ]
Ameloblastoomi korduvat arengut retsidiivi vormis täheldatakse 60% juhtudest pärast konservatiivset kuretaaži, 5% juhtudest pärast radikaalset kirurgilist eemaldamist.
Preoperatiivsed tüsistused |
|
Varajased postoperatiivsed tüsistused |
|
Hilinenud tüsistused |
|
Diagnostika ameloblastoomid
Ameloblastoomi diagnoositakse hambaarsti läbivaatuse ja röntgenograafia abil, mille käigus ilmnevad iseloomulikud muutused luustruktuuris. Diagnoosi kinnitamiseks on ette nähtud tsütoloogiline uuring. [ 18 ]
Testid on mittespetsiifilised ja neid saab määrata üldise kliinilise diagnoosi osana:
- üldine vereanalüüs võetakse kolm korda (enne operatsiooni, pärast operatsiooni ja enne väljakirjutamist);
- uriinianalüüsi tehakse ka kolm korda;
- kogu raviperioodi jooksul võetakse biokeemiline vereanalüüs üks kord iga 14 päeva järel (koguvalgu, kolesterooli, uurea, bilirubiini, kreatiniini, ALAT, ASAT tase);
- koagulogramm;
- SCC kasvaja markerid;
- Vereanalüüs glükoositaseme määramiseks.
Lisaks tehakse kasvaja pinnalt võetud määrdumise tsütoloogiline uuring.
Ameloblastoomi tuvastamiseks kasutatakse järgmisi instrumentaalseid diagnostikameetodeid:
- radiograafia (annab teavet kasvaja suuruse, selle piiride ja struktuuri kohta);
- KT, kompuutertomograafia (meetod, mis on täpsem ja detailsem kui radiograafia);
- MRI, lõualuude magnetresonantstomograafia;
- biopsia (kui lõpliku diagnoosi tegemisel on raskusi);
- tsütoloogia, histoloogia (neoplasma koostise uurimiseks, diagnoosi kinnitamiseks).
Histoloogiline uuring näitab, et ameloblastoomil on emailorganiga sarnane struktuur. Epiteelikasvude perifeerias paiknevad kõrged sammas- või kuubikujulised rakud, mis sisaldavad suuri hüperkromaatilisi tuumasid, üleminekuga mitmetahulistele ja kuubikujulistele ning edasi keskosa suunas tähekujulistele rakustruktuuridele. Lõdvalt jaotunud rakkude vahel on erineva suurusega tsüstid, mis on täidetud granuleeritud või homogeense sisuga. [ 19 ]
Tsüstilised õõnsused võivad olla sisemiselt kaetud mitmekihilise lameepiteeli koega. Sellistel juhtudel määrab arst kogu neoplasmi kudede uurimiseks ekstsisioonilise biopsia.
Kasvaja parenhüüm võib koosneda peamiselt lamedate epiteelirakkude kombinatsioonidest või ahelmoodustistest või polüeedriliste ja sammasrakkude kasvudest. Mõnikord sisaldab struktuur nii basaalseid epiteelirakke kui ka sammasepiteeliga kaetud näärmekude. Harvadel juhtudel on täheldatud kasvaja angiomatoosset struktuuri. Kasvaja stroom on hästi arenenud, võib esineda hüalinosis koos fokaalse kaltsifikatsiooniga.
Ameloblastoomi radiograafiline pilt on üsna spetsiifiline. Eristavaks radiograafiliseks kriteeriumiks on õõnsuste varjude erinev läbipaistvuse aste. Õõnsustel võib olla erinev läbipaistvuse tase: madalast kõrgeni. Tsüsti keskosa on alati väga läbipaistev. Ameloblastoomi tsüstilise variandi korral on tuvastatav üks suur tsüst, mis lokaliseerub alalõua nurga ja haru piirkonnas ehk polütsüstoom. Suurt tsüsti iseloomustavad radiograafiliselt selged moodustise piirid, sageli homogeenne luuhõrenemine. Mõnel juhul projitseeritakse tsüstilisele õõnsusele impakteeritud hammas, kuid selle kroon asub väljaspool, erineva hambapaigutusega. Polütsüstoomi röntgenülesvõte näitab mitme erineva läbimõõduga tsüsti olemasolu, mis asuvad üksteise kõrval (nagu "seebimullid"). Moodustistel on selge ümar konfiguratsioon, mõnikord ebaühtlaste kontuuridega. Need võivad sisaldada impakteeritud hammast. [ 20 ]
Radiograafil tuvastatakse tahke ameloblastoom ebaühtlase ja suhteliselt selgete piiridega luu hõrenemise järgi. Mõnedel patsientidel leitakse hõrenemise taustal vaevumärgatavaid tsüstilisi õõnsusi, mis sageli viitavad kasvaja üleminekuperioodile tahkest ameloblastoomist tsüstiliseks.
Diferentseeritud diagnoos
Ameloblastoomi tuleks eristada järgmistest patoloogiatest:
- osteoblastoklastoom;
- odontogeensed tsüstid;
- kiuline osteodüsplaasia;
- sarkoom;
- krooniline osteomüeliit (koos mädase kasvajaga).
Kui kasvaja asub alalõua nurgas, tuleks seda lisaks eristada odontoomist, hemangioomist, kolesteatoomist, fibroomist ja eosinofiilsest granuloomis.
Kellega ühendust võtta?
Ravi ameloblastoomid
Ameloblastoomi saab ravida ainult kirurgiliselt, nimelt eemaldades kasvaja poolt kahjustatud lõualuu koe. Sekkumise ulatuse määrab patoloogilise protsessi asukoht ja staadium. Mida varem operatsioon tehakse, seda vähem struktuure tuleb eemaldada. Kui kasvaja on saavutanud suure suuruse ja levinud luu valdavasse ossa, võib olla vajalik eemaldada osa lõualuust või isegi kogu hambarida. Kuna operatsioon tehakse näo piirkonnas, kus esteetiline tegur on eriti oluline, lõpetatakse sekkumine eemaldatud kudede ja organite rekonstruktiivse korrektsiooniga – see tähendab nähtava kosmeetilise defekti kõrvaldamisega. [ 21 ]
Pärast kasvaja fookuse resektsiooni alustatakse ravimteraapiat, mille eesmärk on vältida operatsioonijärgseid tüsistusi ja patoloogia kordumist.
Antibiootikumid pärast operatsiooni määrab kirurg. Amoksiklav on sageli valitud ravim selle efektiivsuse, minimaalsete vastunäidustuste ja kõrvaltoimete tõttu. Ravimeid võetakse rangelt vastavalt arsti kirjeldatud skeemile.
Valu ilmnemisel võtke valuvaigisteid ja põletikuvastaseid ravimeid (näiteks nimesuliidi), samuti immuunsüsteemi toetamiseks vitamiinilisandeid.
Suu loputamiseks kasutatakse tavaliselt kloorheksidiini, furatsiliini lahust ja Miramistini.
Taastusravi ajal on oluline järgida spetsiaalset dieeti. Toit peaks olema pehme (optimaalselt vedel) ja mugava temperatuuriga. Teie toidust tuleks välja jätta vürtsid, sool ja suhkur, limonaad, alkohoolsed joogid ja toores taimne toit. [ 22 ]
Ravimid
Ravimite valimisel on vaja arvestada vastunäidustusi, ravimite toksilisuse astet, võimalikke kõrvaltoimeid, pehmetesse kudedesse tungimise kiirust ja organismist eritumise perioodi. [ 23 ] Võib välja kirjutada järgmisi ravimeid:
- Ibuprofeen - võtke üks tablett kolm korda päevas kolme päeva jooksul. Pikem kasutamine võib negatiivselt mõjutada seedesüsteemi.
- Ketanov - võetakse suu kaudu üks kord või korduvalt, olenevalt valu tugevusest, 10 mg annuse kohta, kuni 3-4 korda päevas.Ravi kestus ei ole pikem kui viis päeva, mis aitab vältida seedetrakti erosioonilisi ja haavandilisi kahjustusi.
- Solpadeiin - kasutatakse tugeva valu leevendamiseks, 1-2 tabletti kolm korda päevas, hoides annuste vahel vähemalt 4-tunnise intervalli. Ravimit ei tohi võtta kauem kui viis päeva. Pikaajalisel kasutamisel on võimalik kõhuvalu, aneemia, unehäired, tahhükardia.
- Cetrin - turse leevendamiseks võtke 1 tablett päevas koos veega. Ravim on tavaliselt hästi talutav, ainult mõnikord võib see põhjustada seedehäireid, peavalu, unisust, suukuivust.
- Amoksiklav - postoperatiivsel perioodil määratakse 500 mg 2-3 korda päevas kuni 10 päeva jooksul. Võimalikud kõrvaltoimed: düspepsia, peavalu, krambid, allergilised reaktsioonid.
- Tsifran (tsiprofloksatsiin) – määratakse antibiootikumravi osana individuaalsetes annustes. Võimalike kõrvaltoimete hulka kuuluvad iiveldus, kõhulahtisus ja allergilised reaktsioonid.
- Linkomütsiin on linkosamiidantibiootikum, mida võetakse 500 mg kolm korda päevas. Raviga võivad kaasneda iiveldus, kõhuvalu, pöörduv leukopeenia ja tinnitus. Sellised kõrvaltoimed kaovad pärast ravikuuri iseenesest.
Füsioteraapia
Pärast ameloblastoomi kirurgilist resektsiooni saab kudede taastumise kiirendamiseks kasutada füsioteraapiat. Head tulemused on saavutatavad järgmiselt:
- ülikõrgete sageduste elektriline toime oligotermilises või atermilises annuses, kestusega 10 minutit, kuus protseduuri ravikuuri kohta;
- 10 minutit kestev kõikumine kuue protseduuri ulatuses (kolm korda päevas ja ülejäänud kord iga kahe päeva tagant);
- infrapunalaser ravi kestusega 15-20 minutit, iga päev, 4 protseduuri ulatuses;
- Magnetlaserravi lainepikkusega 0,88 µm, koguvõimsusega 10 mW, magnetinduktsiooniga 25–40 mT, toimeajaga 4 minutit ja kaheksast seansist koosneva kuuriga.
Kui operatsioonipiirkonnas esinevad tihendeid ja armide muutusi, on näidustatud ultraheliravi pidevas režiimis, seansi kestusega kuni 8 minutit ja pea pindalaga 1 cm². Ravikuur koosneb 8-10 seansist.
Taimne ravi
Kuidas saavad ravimtaimed ameloblastoomi korral aidata? Mõned taimed võivad leevendada valu ja stimuleerida immuunsüsteemi, kiirendades seeläbi kudede taastumist. Teada on ka teisi ravimtaimede eeliseid:
- ravimtaimedel võib olla kasvajavastane toime;
- paljud taimed säilitavad happe-aluse tasakaalu;
- taimsed preparaadid imenduvad hästi isegi nõrgenenud organismi poolt patoloogia mis tahes staadiumis;
- Ürdid parandavad organismi kohanemist uute elutingimustega ja hõlbustavad operatsioonijärgse perioodi kulgu.
Ravimtaimi saab kasutada nii kuivatatult kui ka värskelt korjatuna. Neid kasutatakse leotiste ja keediste valmistamiseks. Ameloblastoomi puhul on olulised järgmised ravimtaimed:
- Karanthus on poolpõõsas, millel on kasvajavastane toime. Tinktuuri valmistamiseks võtke 2 spl taime oksi ja lehti, valage peale 250 ml viina, hoidke pimedas kohas 10 päeva, filtreerige. Võtke 5 tilka pool tundi enne sööki, suurendades annust iga päev, viies selle 10 tilgani päevas. Ravi kestus on 3 kuud. Ettevaatust: taim on mürgine!
- Harilik vahukomm on tuntud rögalahtistav ja põletikuvastane taim, mis pole vähem efektiivne mitmesuguste kasvajaliste protsesside korral. Üks supilusikatäis purustatud risoomi valatakse termosesse 200 ml keeva veega, hoitakse 15 minutit, valatakse tassi ja jahutatakse toatemperatuuril 45 minutit, seejärel filtreeritakse. Võtke suu kaudu kolm korda päevas pärast sööki, 50-100 ml, 2-3 nädala jooksul.
- Harilik lõvilõug – selle taime risoom sisaldab terpenoidi, millel on valuvaigistav ja taastav toime. Valmistage leotis 1 spl purustatud juurt 200 ml keeva vee kohta. Võtke 50 ml päevas (jagage kaheks annuseks).
- Kuderpuu - sisaldab alkaloidi, mida kasutatakse edukalt isegi pahaloomuliste kasvajate raviks. Kuderpuu juured ja noored võrsed (20 g) valatakse 400 ml keeva veega, keedetakse 15 minutit ja lastakse seejärel tõmmata umbes 3-4 tundi. Kurnatakse ja keeva veega täidetakse maht 500 ml-ni. Joo 50 ml 4 korda päevas.
- Harilik immortelle – suurepärane spasmide leevendamiseks ja operatsioonijärgse valu leevendamiseks. Keetmise valmistamiseks võtke 3 spl purustatud taime, valage peale 200 ml keeva vett, laske 40 minutit tõmmata, kurnake. Lisage keedetud vett, et maht suureneks 200 ml-ni. Võtke 50 ml kolm korda päevas pool tundi enne sööki kuu aja jooksul.
- Takjajuur – kasvajavastase toimega. Võetakse suu kaudu keedisena (10 g 200 ml vee kohta), 100 ml kaks korda päevas, kuu aega.
- Sedum – selle ürdi keetmine ja leotis parandab ainevahetust, toniseerib, kõrvaldab valu ja peatab põletikulise protsessi. Valmistage leotis 200 ml keevast veest ja 50 g taime kuivadest purustatud lehtedest. Jooge 50–60 ml päevas.
- Ohakas - ennetab kasvaja taastekke. Keedunõu valmistatakse kiirusega 1 spl lehti 200 ml keeva vee kohta. Võtke 100 ml 3 korda päevas.
- Saialill - soodustab patoloogiliste fookuste resorptsiooni, vere puhastamist ja haavade paranemist. Võtke apteegitinktuuri 20 tilka 15 minutit enne sööki (veega) kolm korda päevas kuu aja jooksul.
Ravimtaimede kasutamise peab heaks kiitma raviarst. Neid ei tohiks kunagi kasutada traditsioonilise ravi asendajana. [ 24 ]
Kirurgiline ravi
Ravi seisneb ameloblastoomi kirurgilises eemaldamises. Mädase põletikulise protsessi korral teostab kirurg suuõõne desinfitseerimise. Kasvaja eemaldatakse, seinad pestakse fenooliga: see on vajalik kasvajaelementides nekrootiliste protsesside käivitamiseks ja nende arengu aeglustamiseks. Kui operatsioon tehakse mandibulaarpiirkonnas, siis tehakse lisaks luusiirdamine ja hambaproteesimine koos ortopeedilise seadme pideva kandmisega. Pärast operatsiooni õõnsust ei õmmelda, et vähendada kasvaja kordumise riski. Õmbluse asemel kasutatakse tamponaadi, mis soodustab õõnsuse seinte epiteeliseerumist. [ 25 ]
Komplekssete krooniliste juhtude korral tehakse lõualuu osaline disartikulatsioon (lõualuu kirurgiline keeramine mööda liigesepilu piiri, mis ei vaja luu saagimist). Eemaldatud lõualuu osa asemele implanteeritakse spetsiaalse ortopeedilise seadme abil luuplaat.
Kui ameloblastoomi eemaldamine on mingil põhjusel võimatu või kui kasvaja muutub pahaloomuliseks, määratakse kiiritusravi. [ 26 ]
Pärast operatsiooni määratakse patsientidele antibiootikumikuur ja neile antakse postoperatiivse toitumise põhitõed. Mitu nädalat ei tohiks patsient süüa kõva ega jämedat toitu ning pärast iga söögikorda tuleb suud loputada spetsiaalse lahusega. [ 27 ]
Ameloblastoomi eemaldamine toimub järgmiselt:
- Kui neoplasm lokaliseerub luumassis, tehakse osaline mandibulaarne resektsioon.
- Kui ameloblastoom on suur ja ulatub alalõualuu servani, tehakse läbiv mandibulaarne resektsioon. Kui harul on tugev kahjustus ja kondülaarprotsess on mõjutatud, on see näidustus alalõualuu ja kasvaja eksartikuleerimiseks tervete kudede piiridesse.
- Kasvaja kordumise vältimiseks peab kirurg mõistma ja järgima ablastika ja antiblastika põhimõtteid.
Patsienti ravitakse haiglas umbes 2 nädalat, mille järel ta viiakse ambulatoorsele vaatlusele kohustusliku arstivisiidiga:
- esimesel aastal pärast operatsiooni – iga kolme kuu tagant;
- järgmise kolme aasta jooksul – üks kord kuue kuu jooksul;
- seejärel igal aastal.
Ärahoidmine
Põletikuliste protsesside, patoloogiliste luumurdude ja pahaloomuliste kasvajate vormis tüsistuste vältimiseks preoperatiivses staadiumis on vaja ameloblastoomi võimalikult varakult avastada. Kõigile patsientidele ilma eranditeta on soovitatav kompleksne ravi sümptomaatiliste ravimite ja antibiootikumravi abil.
Verejooksu vältimiseks operatsioonijärgsel taastumisperioodil on vaja jälgida vere hüübimise kvaliteeti ja vererõhu näitajaid.
Hilinenud kõrvaltoimete ennetamine on tihedalt seotud kvalifitseeritud diagnostika, esialgse stereolitograafilise modelleerimisega. Optimaalseks peetakse radikaalset sekkumist koos järgneva luuplastikaga, endoproteeside ja innukate implantaatide paigaldamisega, kontuurplastikaga ning siirdamise mikrovaskulaarsete meetmetega.
Prognoos
Ameloblastoomi diagnoositakse sageli kasvu hilisemates staadiumides, mis on tingitud haiguse ebapiisavalt väljendunud sümptomitest ja selle väikesest levikust. Kasvaja peamine ravivõimalus on selle kohene eemaldamine koos järgneva rekonstrueerimisega (võimaluse korral).
Soodsa prognoosi peamiseks teguriks on haiguse varajane diagnoosimine ja õigeaegne kvalifitseeritud ravi, mis hõlmab kirurgilist eemaldamist, keemilist või elektrilist koagulatsiooni, kiiritusravi või kirurgia ja kiirituse kombinatsiooni.
Operatsioonijärgse taastumise edasine tulemus sõltub teostatud ravi, sealhulgas kirurgilise sekkumise mahust ja iseloomust. Näiteks alalõualuu radikaalne eemaldamine toob kaasa märkimisväärsete kosmeetiliste defektide ilmnemise, samuti kõne- ja närimisfunktsiooni kahjustuse. [ 28 ]
Radikaalse sekkumise läbinud patsientide rehabilitatsiooni peamiseks eesmärgiks peetakse lõualuu funktsiooni korrigeerimist. Selleks tehakse primaarne ehk edasilükatud luuplastika koos järgneva hambaproteesiga. Sellise operatsiooni ulatuse määrab näo-lõualuu kirurg.
Praegu ei ole ameloblastoomi eemaldamise järgselt patsiendilt individuaalse hambaproteesimise meetodid piisavalt arenenud, hoolimata asjaolust, et näo konfiguratsiooni ja lõualuu funktsionaalsuse taastamine on sotsiaalse ja meditsiinilise rehabilitatsiooni oluline punkt.

