Artikli meditsiiniline ekspert
Uued väljaanded
Eesnäärmevähi staadiumide diagnoosimine
Viimati vaadatud: 04.07.2025

Kõik iLive'i sisu vaadatakse meditsiiniliselt läbi või seda kontrollitakse, et tagada võimalikult suur faktiline täpsus.
Meil on ranged allhanke juhised ja link ainult mainekate meediakanalite, akadeemiliste teadusasutuste ja võimaluse korral meditsiiniliselt vastastikuste eksperthinnangutega. Pange tähele, et sulgudes ([1], [2] jne) olevad numbrid on nende uuringute linkideks.
Kui tunnete, et mõni meie sisu on ebatäpne, aegunud või muul viisil küsitav, valige see ja vajutage Ctrl + Enter.
Kliiniliselt eristatakse lokaliseeritud (T1-2 , N0 , M0 ), lokaalselt levinud (T3-4 , N0-1 , M0 ) ja generaliseerunud vähki (T1-4 , N0-1 , M1 ).
Kliiniliselt lokaliseeritud ja lokaalselt kaugelearenenud staadiumiga patsiendid liigitatakse riskiastme järgi (D'Amico A V. jt, 2003):
- madal: staadium T1a -c; PSA tase alla 10 ig/ml: Gleasoni skaala - 2-5; biopsia korral - ühepoolne kahjustus alla 50%:
- mõõdukas: staadium T2a ; PSA tase alla 10 ng/ml; Gleasoni skoor - 3 + 4 = 7; biopsias - kahepoolne kahjustus alla 50%;
- kõrge staadium T2b , T3a -b; PSA tase - 10-20 ng/ml; Gleasoni skaala - üle 4 + 3 - 7; biopsia korral - kahjustus üle 50%, perineuraalne invasioon;
- väga kõrge: staadium T4 ; PSA tase üle 20 ng/ml; Gleasoni skoor üle 8; biopsia näitab lümfovaskulaarset invasiooni.
Pärast diagnoosi selgitamist ja protsessi ulatuse (lokaliseeritud, lokaalselt levinud või generaliseerunud) kindlakstegemist seisavad arst ja patsient ravimeetodi valiku ees. Tänapäeva ühiskonnas omistatakse suurt tähtsust patsientide elukvaliteedile pärast ravi alustamist. Elukvaliteet ilma ravita vastab põhihaiguse kulule ja sõltub onkoloogilise protsessi progresseerumisest. Elukvaliteedi muutused toimuvad peamiselt pärast ravi alustamist ja ühe terapeutilise või kirurgilise meetodi kasutamist. Protsessi staadiumi selge kindlakstegemine võimaldab mitte ainult valida optimaalse ravimeetodi, vaid ka ennustada haiguse edasist kulgu.
PSA taseme määramine koos eesnäärmevähi kliinilise pildi ja kasvaja gradatsiooniga Gleasoni skaala järgi suurendab oluliselt iga loetletud näitaja infosisu vähi patoloogilise staadiumi kindlakstegemisel. AV Partin jt (1997) pakkusid välja prognostilised tabelid, mis võimaldavad ennustada kasvaja edasist levikut, ravimeetodi valikut, radikaalsuse astet ja ravi efektiivsuse prognoosi.
Kasvaja leviku hindamiseks on kõige sagedamini kasutatavad meetodid DRE, TRUS, PSA taseme määramine ja luu stsintigraafia. Vajadusel määratakse kompuutertomograafia (KT) või magnetresonantstomograafia (MRI) ja rindkere röntgenülesvõte.
Kõik pildiuuringud on mõeldud staadiumi määramiseks ja ravi efektiivsuse hindamiseks. Pärast diagnoosi kinnitamist peab uroloog selgitama primaarse kasvaja mahtu, selle piire, kasvaja invasiivset või metastaatilist potentsiaali. Kõik need näitajad on haiguse prognoosi ja ravimeetodi valiku seisukohalt väga olulised.
Primaarne kasvaja (T)
Kõigepealt on vaja kindlaks teha, kas kasvaja piirdub eesnäärmega (T 1-2 ) või ulatub kapslist väljapoole (T 3-4 ). Digitaalne uuring ei võimalda sageli hinnata kasvaja levikut. Mõnede andmete kohaselt vastavad DRE tulemused histoloogilise uuringu tulemustele vähem kui 50% patsientidest. Täpsem uuring on siiski näidustatud alles radikaalse ravi otsustamisel.
PSA tase võib küll peegeldada kasvaja ulatust, kuid ei võimalda täpselt määrata morfoloogilist staadiumi. PSA taseme, Gleasoni indeksi ja palpatsiooniandmete kombinatsioon võimaldab morfoloogilist staadiumi paremini ennustada kui iga parameetri eraldi hindamine. Vaba PSA väärtus on vastuoluline: ühes uuringus aitas vaba PSA sisalduse määramine selgitada staadiumi lokaliseeritud kasvajate puhul, kuid teised uuringud seda ei kinnitanud. Ainult põhjalikud uuringud aitavad seda küsimust lahendada.
Transrektaalset ultraheli kasutatakse eesnäärme seisundi uurimiseks kõige sagedamini. See meetod suudab tuvastada ainult 60% kasvajatest ja ei näita alati kapsli invasiooni. Ligi 60% patsientidest, kellel on T3 staadium . Ultraheli näitab harvemat protsessi. Kapsli invasiooni ultraheli tunnusteks on näärme kontuuri kumerus, ebatasasus ja rebend. Kasvajarakkude invasioon seemnepõiekestesse on halb prognostiline märk, kuid selle kohta käiv teave on ravimeetodi valimisel äärmiselt oluline. TRUS-i tegemisel tuleb pöörata tähelepanu vesiikulite ehhostruktuurile (hüperehhogeensus), nende asümmeetriale, deformatsioonile ja laienemisele. Samuti viitab seemnepõiekeste kahjustusele ümaruse kadumine ja tihendus näärme alusel. Need tunnused on üsna subjektiivsed, seega on ultraheliandmetele täielikult lootma jäämine kohatu. Seemnepõiekeste invasioon näitab suurt lokaalse retsidiivi ja metastaaside riski ning nende biopsia on selgitamiseks näidustatud (enne operatsiooni). Uuringut ei tohiks selle protseduuriga alustada, kuid kui invasiooni oht on suur ja ravi valik sõltub biopsia tulemusest, on selle rakendamine õigustatud. Negatiivne tulemus ei välista mikroskoopilist invasiooni. Seemnepõiekeste biopsia tehakse reeglina kliinilises staadiumis T2b ja kõrgemas ning PSA sisaldus on üle 10 ng/ml. Tulemust peetakse positiivseks, kui vähemalt üks eesnäärme baasi biopsia sisaldab kasvajarakke. Lisaks täiendavatele uuringutele ja primaarse biopsia tulemuste põhjalikule analüüsile saab staadiumi kliinilise määramise täpsust suurendada (rolli mängivad kasvajakollete arv ja ulatus, kapsli invasioon). Oluline on ka diferentseerumisaste: Gleasoni indeksiga alla 6 lokaliseerub kasvaja 70% juhtudest.
Vähi korral on verevool eesnäärmes suurem kui normaalses eesnäärmes või selle hüperplaasia korral. Pärast kastreerimist väheneb verevoolu intensiivsus näärmes. Ehhodopplerograafia kaartide väljatöötamine eesnäärmevähi diagnoosimiseks ja jälgimiseks on paljulubav, kuid praegu puuduvad usaldusväärsed andmed ehhodopplerograafia kasutamise kohta lokaalse protsessi staadiumi määramisel. Selle meetodi abil on võimalik saada täiendavat materjali sihipärase biopsia ajal patoloogilise vaskularisatsiooni fookustest.
Eesnäärmevähi visualiseerimise tulemused sõltuvad otseselt kliiniku tehnilisest varustusest ja spetsialisti kogemusest. Seetõttu mängivad kõik kaasaegsed visualiseerimismeetodid mitte määravat, vaid selgitavat rolli ning ravimeetodi valik põhineb kliinilise läbivaatuse andmete ja instrumentaalsete uuringute kombinatsioonil.
MRI-l on parimad võimalused eesnäärme struktuuri visualiseerimiseks. Kaasaegne standard vaagnaelundite uurimiseks MRI-meetodil on endorektaalse anduri kasutamine, mis võimaldab saada pildi võimalikult suure ruumilise lahutusvõimega 0,5–1 mm. Õhu surumine endorektaalsesse andurisse tagab eesnäärme kapsli, eesnäärme nurkade ja Denonvilliers'i eesnäärme frontaalfastsia selge visualiseerimise. Endorektaalse anduri kasutamine MRI-s ei piira piirkondlike lümfisõlmede (kuni kõhuaordi hargnemiskoha tasemeni) visualiseerimist. Eesnäärmevähki iseloomustab madal signaali intensiivsus T-kaalutud piltidel näärme muutumatust perifeersest tsoonist tuleva kõrge intensiivsusega signaali taustal. Ebakorrapärane kuju, hajus levik massiefektiga, hägused ja ebaühtlased kontuurid on eesnäärme perifeerses tsoonis asuvate madala signaali intensiivsusega fookuste morfoloogilised tunnused, mis viitavad kahjustuse neoplastilisele olemusele. Dünaamilise kontrasteerimise teostamisel akumuleerivad vähikolded kontrastaine kiiresti arteriaalses faasis ja eemaldavad selle kiiresti, mis peegeldab angiogeneesi astet ja vastavalt ka kasvaja pahaloomulisuse astet. Madal signaali intensiivsus on iseloomulik ka biopsiajärgsete hemorraagiate fookustele, prostatiidile, näärme neutraalse tsooni stromaalsele healoomulisele hüperplaasiale, fibroossetele-katariaalsetele muutustele, fibromuskulaarsele hüperplaasiale, hormonaalse või kiiritusravi tagajärgedele. MRI ilma dünaamilise kontrasteerimiseta ei võimalda enamiku loetletud muutuste ja haiguste usaldusväärset diferentseerimist.
Nagu eespool märgitud, on eesnäärmevähi kuvamismeetodi üks peamisi ülesandeid määrata näärmekahjustuse maht ja kasvaja levik kapslist väljapoole. Kasvaja mahu määramine on prognoosi seisukohalt oluline. Kasvaja maht alla 4 cm3 näitab kaugete metastaaside esinemist ja 12 cm3 näitab metastaaside äärmiselt suurt tõenäosust. Uuringute kohaselt on MRI täpsus eesnäärme neoplastiliste kahjustuste fookuste tuvastamisel vahemikus 50–90%. MRI tundlikkus eesnäärmevähi lokaliseerimise määramisel on umbes 70–80%, samas kui vähi mikroskoopilisi fookuseid (koldeid) MRI abil tuvastada ei saa.
Endorektaalse MRI kõige olulisem eelis on võime lokaliseerida neoplastilisi kahjustusi piirkondades, mis on teistele diagnostilistele meetoditele ligipääsmatud, ning selgitada kasvaja kasvu olemust ja suunda. Näiteks võimaldab MRI tuvastada neoplastilisi kahjustusi eesnäärme perifeerse tsooni eesmistes osades, mis on transrektaalse biopsiaga ligipääsmatud. Üldiselt täiendab MRI oluliselt DRE ja TRUS andmeid kasvaja lokaliseerimise kohta.
Endorektaalne magnetresonantstomograafia (MRT) võimaldab visualiseerida näärmekapslit, veresoonte-närvi kimpe, seemnepõiekesi, näärmetippu, eesnäärme ümbruse venoosset põimiku ja määrata näärmekasvaja lokaalset levimust. Tuleb rõhutada, et kapsli penetratsiooni peetakse mikroskoopiliseks tunnuseks ja isegi tänapäevased MRT-seadmed (endorektaalne spiraal) ei suuda sellist teavet anda. Andmeid on võimalik saada ainult näärmekapslist kaugemal asuva kasvu kohta.
Ekstrakapsulaarse venituse diagnostilised kriteeriumid MRI abil:
- ekstrakapsulaarse kasvaja olemasolu;
- näärme ebaühtlane kontuur (deformatsioon, nurk);
- neurovaskulaarsete kimpude asümmeetria;
- eesnäärme nurkade hääbumine;
- kasvaja lai kokkupuude kapsliga.
MRI tulemuste kõrgeim spetsiifilisus (kuni 95-98%) ja täpsus saavutatakse keskmise või kõrge ekstrakapsulaarse invasiooni riskiga patsientide uurimisel. Arvatakse, et ekstrakapsulaarne invasioon (MRI andmetel) näitab kirurgilise ravi sobimatust ja haiguse ebasoodsat prognoosi. Hormonaalne või kiiritusravi ei mõjuta eesnäärme kasvaja ekstrakapsulaarse leviku avastamise täpsust. Vähikollete ja kasvaja ekstrakapsulaarse leviku avastamise peamine raskus on tomogrammide tõlgendamise suur varieeruvus erinevate spetsialistide poolt. Kiiritusdiagnostika spetsialisti peamine ülesanne on saavutada kõrge diagnostiline spetsiifilisus (isegi tundlikkuse arvelt), et mitte võtta opereeritavatelt patsientidelt võimalust radikaalseks raviks.
Vähi-, hüperplastilise ja normaalse eesnäärmekoe tiheduse sarnasus kompuutertomograafias muudab selle meetodi kasvaja lokaalse leviku hindamisel vähekasulikuks. Seemnepõiekeste invasioon on olulisem kui kapslite invasioon, kuid isegi sel juhul annab kompuutertomograafia teavet ainult kaugelearenenud juhtudel. Seda meetodit kasutatakse aga aktiivselt löögipiirkonna märgistamiseks enne kiiritusravi.
Kiiritusdiagnostika aeglane areng meie riigis on toonud kaasa eesnäärmevähi hilise diagnoosimise ja sellest tulenevalt eesnäärmevähi radikaalsete ravimeetodite (näiteks prostatektoomia) ebapiisava levimuse, kaasaegsete tomograafide vähese kättesaadavuse ning kiiritusdiagnostika spetsialistide ja uroloogide asjakohaste koolitusprogrammide puudumise. Vaatamata asjaolule, et kompuutertomograafia ja magnetresonantstomograafia on nüüdseks laialt levinud, on kabinettide varustustase ja kiiritusdiagnostika spetsialistide haridus ebapiisav, et saadud teave saaks eesnäärmevähiga patsientide ravimeetodi valikul otsustavaks.
Regionaalsed lümfisõlmed (N)
Regionaalseid lümfisõlmi tuleks hinnata ainult siis, kui see otseselt mõjutab ravistrateegiat (tavaliselt radikaalse ravi planeerimisel). Kõrge PSA tase, T2c -T3a kasvajad, halb diferentseerumine ja perineuraalne invasioon on seotud lümfisõlmede metastaaside suure riskiga. Lümfisõlmede seisundi hindamist PSA taseme põhjal peetakse ebapiisavaks.
Ainult lümfadenektoomia (avatud või laparoskoopiline) annab vajaliku teabe. Hiljutised laiendatud lümfadenektoomia uuringud on näidanud, et eesnäärmevähk ei mõjuta alati obturaatori lümfisõlmi. Asümptomaatiliste kasvajate ja PSA taseme alla 20 kg/ml korral kinnitab kompuutertomograafia (KT) suurenenud lümfisõlmi ainult 1% juhtudest. MRI või KT kasutamine on õigustatud kõrge metastaaside riski korral, kuna nende meetodite spetsiifilisus ulatub 93–96%-ni. Kuid isegi positiivne tulemus nende kasutamisel võib olla vale ja ainult kahtlase lümfisõlme punktsioon võimaldab lümfadenektoomiast keelduda. Retrospektiivse analüüsi kohaselt ei näita lümfisõlme suurus alati metastaaside olemasolu selles; mõjutatud lümfisõlmede asümmeetriat peetakse informatiivsemaks märgiks. Praegu diagnoositakse postoperatiivse histoloogilise uuringu põhjal lümfisõlmede metastaasid vaid 2–3%-l patsientidest, kellel on lokaliseeritud eesnäärmevähi tõttu tehtud radikaalne prostatektoomia.
Lümfisõlmede metastaaside tuvastamise meetoditena on soovitatav positronemissioontomograafia (PET) ja märgistatud antikehadega stsintigraafia, kuid nende kasutamine on ebapiisava tundlikkuse tõttu endiselt piiratud.
Partini nomogramme (2001) saab kasutada regionaalsete lümfisõlmede haaratuse riski hindamiseks. Nomogrammid on matemaatilised algoritmid, mida kasutatakse konkreetse patsiendi või patsientide rühma puhul. Need tabelid võimaldavad kliinilise staadiumi, PSA taseme ja Gleasoni indeksi põhjal määrata lokaalse kasvaja leviku tõenäosust (kapslisse, seemnepõiekestesse) ja lümfisõlmede haaratust. Eelkõige võimaldavad need tuvastada patsientide rühma, kellel on lümfisõlmede metastaaside tekkimise tõenäosus madal (alla 10%) (PSA tase üle 20 ng/md, staadium T1-2a ja Gleasoni indeks 2-6); selles rühmas ei pruugi lümfisõlmede seisundit enne radikaalset ravi täpsustada. Lümfisõlmede metastaaside riski saab hinnata ka väljendunud anaplaasiaga (4-5 punkti) kasvajapiirkondade tuvastamise teel: kui selliseid piirkondi leitakse neljas või enamas biopsias või need domineerivad vähemalt ühes biopsias, ulatub risk 20-45%-ni. Teistel patsientidel ei ületa see 2,5%-ni. Sellistel juhtudel ei ole täiendavat uuringut vaja.
Kaugemetastaasid (M)
85%-l eesnäärmevähki surevatest patsientidest avastatakse aksiaalse skeleti kahjustused. Luumetastaasid tekivad vähirakkude tungimise tõttu luuüdisse vereringega, mis viib kasvaja kasvu ja luustruktuuride lüüsini. Luumetastaaside levimus mõjutab prognoosi ja nende varajane avastamine hoiatab arsti võimalike tüsistuste eest. 70% juhtudest kaasneb metastaasidega luu isoensüümi aluselise fosfataasi (ALP) aktiivsuse suurenemine. ALP aktiivsuse ja PSA taseme määramine võimaldab enamikul juhtudest tuvastada luumetastaase. Mitmemõõtmelise analüüsi kohaselt mõjutab neid näitajaid ainult luumetastaaside arv. On oluline, et luu isoensüümi ALP aktiivsus peegeldaks luukahjustuse astet täpsemalt kui PSA tase.
Stsintigraafiat peetakse luumetastaaside avastamisel kõige tundlikumaks meetodiks (see on parem kui radiograafia ning aluselise ja happelise fosfataasi aktiivsuse määramine). Tehneetsiumdifosfonaate on parem kasutada radiofarmatseutilise ravimina, kuna nende akumuleerumine luudes on palju aktiivsem kui pehmetes kudedes. On näidatud korrelatsiooni luukahjustuse poolkvantitatiivse hindamise ja elulemuse vahel. Kaugemetastaaside avastamine on võimalik igas organis. Kõige sagedamini esinevad need mitteregionaalsetes lümfisõlmedes, kopsudes, maksas, ajus ja nahas. Vastavate kaebuste ja sümptomite korral kasutatakse nende avastamiseks rindkere röntgenograafiat, ultraheli, kompuutertomograafiat ja magnetresonantstomograafiat. Kahtlustatava luumetastaasi taktika on esitatud diagrammil.
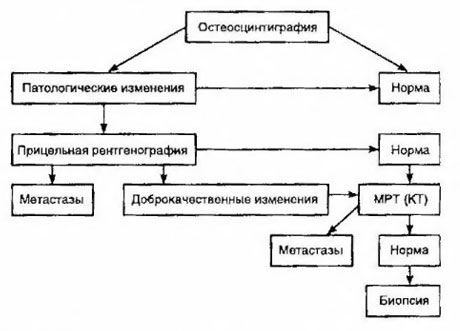
Kõige usaldusväärsem laboratoorne indikaator, mis aitab määrata metastaaside astet, on PSA tase. On näidatud, et selle tõus üle 100 ng/ml on ainus parameeter, mis usaldusväärselt viitab kaugetele metastaasidele. PSA taseme määramine vähendab luustsintigraafiat vajavate patsientide arvu. Luumetastaaside avastamise tõenäosus PSA taseme languse korral on väga väike. Kaebuste puudumisel ja algse PSA sisalduse korral alla 20 ng/ml saab kõrgelt ja mõõdukalt diferentseerunud kasvajate avastamist vältida. Samal ajal on stsintigraafia näidustatud halvasti diferentseerunud kasvajate ja kapsli invasiooni korral (sõltumata PSA tasemest).


 [
[