Artikli meditsiiniline ekspert
Uued väljaanded
Tsüstiline fibroos
Viimati vaadatud: 04.07.2025

Kõik iLive'i sisu vaadatakse meditsiiniliselt läbi või seda kontrollitakse, et tagada võimalikult suur faktiline täpsus.
Meil on ranged allhanke juhised ja link ainult mainekate meediakanalite, akadeemiliste teadusasutuste ja võimaluse korral meditsiiniliselt vastastikuste eksperthinnangutega. Pange tähele, et sulgudes ([1], [2] jne) olevad numbrid on nende uuringute linkideks.
Kui tunnete, et mõni meie sisu on ebatäpne, aegunud või muul viisil küsitav, valige see ja vajutage Ctrl + Enter.
Tsüstiline fibroos on geneetiline autosomaalselt retsessiivne monogeenne haigus, mida iseloomustab elutähtsate organite eksokriinsete näärmete sekretsioonihäire, mis kahjustab peamiselt hingamis- ja seedesüsteemi, rasket kulgu ja ebasoodsat prognoosi.
 [ 1 ]
[ 1 ]
Epidemioloogia
Tsüstilise fibroosi esinemissagedus kõigub vahemikus 1:2500 kuni 1:4600 vastsündinu kohta. Igal aastal sünnib maailmas umbes 45 000 tsüstilise fibroosiga inimest. Tsüstilise fibroosi geeni kandjate esinemissagedus on 3-4%, kusjuures kogu maailmas on selle geeni kandjaid umbes 275 miljonit inimest, kellest umbes 5 miljonit elab Venemaal ja umbes 12,5 miljonit SRÜ riikides.
Põhjused tsüstiline fibroos
Tsüstiline fibroos kandub edasi autosomaalselt retsessiivselt. Tsüstilise fibroosi geen asub autosoomis 7, sisaldab 27 eksonit ja koosneb 250 000 nukleotiidipaarist.
Ühel geenil võib olla palju mutatsioone, millest igaüks on spetsiifiline kindlale populatsioonile või geograafilisele piirkonnale. On kirjeldatud üle 520 mutatsiooni, millest kõige levinum on delta-P-508 ehk aminohappe fenüülalaniini asendus positsioonil 508.
Pathogenesis
Tsüstilise fibroosi geeni mutatsioonid häirivad CFTR-i (tsüstilise fibroosi transmembraanne regulaator) valgu struktuuri ja funktsiooni. See valk toimib kloriidikanalina, osaledes bronhopulmonaalsüsteemi, seedetrakti, kõhunäärme, maksa ja reproduktiivsüsteemi epiteelirakkude vee-elektrolüütide vahetuses. CFTR-valgu funktsiooni ja struktuuri häire tagajärjel kogunevad rakus kloriidioonid Cl⁻ . See viib eritusjuhade valendikus elektrilise potentsiaali muutumiseni, mis hõlbustab suures koguses naatriumioonide (Na⁺) voolamist juha valendikusest rakku ja veelgi suurenenud vee imendumist peritsellulaarsest ruumist.
Nende muutuste tagajärjel pakseneb enamiku eksokriinsete näärmete sekretsioon, selle evakueerimine on häiritud, mis põhjustab organites ja süsteemides väljendunud sekundaarseid häireid, mis on kõige ilmekamad bronhopulmonaalses ja seedesüsteemis.
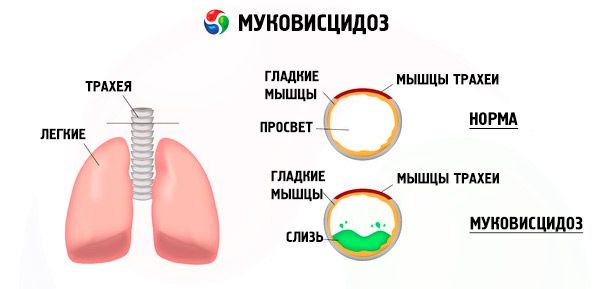
Bronhides tekib erineva intensiivsusega krooniline põletikuline protsess, ripsmelise epiteeli funktsioon on järsult häiritud, röga muutub väga viskoosseks, paksuks, väga raskesti eemaldatavaks, täheldatakse selle stagnatsiooni, tekivad bronhiolo- ja bronhoektaasiad, mis aja jooksul muutuvad sagedasemaks. Need muutused põhjustavad hüpoksia suurenemist ja kroonilise kopsuhaiguse teket.
Tsüstilise fibroosiga patsientidel on äärmiselt suur eelsoodumus kroonilise põletiku tekkeks bronhopulmonaalsüsteemis. See on tingitud lokaalse bronhopulmonaalkaitsesüsteemi väljendunud häiretest (IgA, interferooni, alveolaarsete makrofaagide ja leukotsüütide fagotsüütilise funktsiooni vähenemine).
Alveolaarsed makrofaagid mängivad olulist rolli kroonilise põletiku tekkes bronhopulmonaalsüsteemis. Nad toodavad suures koguses IL-8-d, mis suurendab dramaatiliselt neutrofiilide kemotaksist bronhide puus. Neutrofiilid kogunevad suurtes kogustes bronhidesse ja koos epiteelirakkudega eritavad paljusid põletikku soodustavaid tsütokiine, sealhulgas IL-1, 8, 6, tuumorinekroosifaktorit ja leukotrieene.
Bronhopulmonaalsüsteemi kahjustuste patogeneesis mängib olulist rolli ka ensüümi elastaasi kõrge aktiivsus. Eristatakse eksogeenset ja endogeenset elastaasi. Esimest toodavad bakteriaalne floora (eriti Pseudomonas aeruginosa), teist neutrofiilsed leukotsüüdid. Elastaas hävitab bronhide epiteeli ja teisi struktuurielemente, mis aitab kaasa mukotsiliaarse transpordi edasisele häirdumisele ja bronhoektaasia kiirele tekkele.
Neutrofiilsed leukotsüüdid sekreteerivad ka teisi proteolüütilisi ensüüme. Alfa-1-antipürsiin ja leukoproteaaside sekretoorne inhibiitor neutraliseerivad proteolüütiliste ensüümide mõju ja kaitsevad seeläbi bronhopulmonaalsüsteemi nende kahjuliku mõju eest. Kahjuks aga pärsib tsüstilise fibroosiga patsientidel neid kaitsvaid faktoreid märkimisväärne hulk neutrofiilset proteaasi.
Kõik need asjaolud aitavad kaasa infektsiooni sattumisele bronhopulmonaalsüsteemi ja kroonilise mädase bronhiidi tekkele. Lisaks tuleb arvestada, et tsüstilise fibroosi geeni poolt kodeeritud defektne valk muudab bronhide epiteeli funktsionaalset seisundit, mis soodustab bakterite, eelkõige Pseudomonas aeruginosa, adhesiooni bronhide epiteelile.
Lisaks bronhopulmonaalsüsteemi patoloogiale põhjustab tsüstiline fibroos ka kõhunäärme, mao, jäme- ja peensoole ning maksa tõsist kahjustust.
Sümptomid tsüstiline fibroos
Tsüstiline fibroos avaldub mitmesuguste kliiniliste sümptomitega. Vastsündinutel võib haigus avalduda mekooniumi iileusena. Trüpsiini puudumise või isegi täieliku puudumise tõttu muutub mekoonium väga tihedaks, viskoosseks ja koguneb ileotsekaalsesse piirkonda. Lisaks tekib soolesulgus, mis avaldub intensiivse sapise oksendamise, kõhupuhituse, mekooniumi eritumise puudumise, peritoniidi sümptomite tekke ja raske joobeseisundi kliiniliste ilmingute kiire süvenemise näol. Kui kiiret kirurgilist sekkumist ei tehta, võib laps surra esimestel elupäevadel.
Kergematel juhtudel on tsüstilise fibroosi iseloomulikuks tunnuseks rikkalik, sagedane, õline, suure rasvasisaldusega ja väga ebameeldiva lõhnaga väljaheide. 1/3 patsientidest täheldatakse pärasoole prolapsi.
Seejärel jätkavad patsiendid soole talitlushäireid, malabsorptsioonisündroomi, raskeid füüsilise arengu häireid ja rasket hüpovitaminoosi.
Esimesel või teisel eluaastal ilmnevad bronhopulmonaalsüsteemi kahjustuse sümptomid (haiguse kerge vorm), mis avaldub köhana, mis võib olla äärmiselt väljendunud ja meenutada läkaköhaga köha. Köhaga kaasneb tsüanoos, õhupuudus ja paksu röga eritumine, mis on esialgu limase ja seejärel mädase iseloomuga. Järk-järgult kujuneb välja kroonilise obstruktiivse bronhiidi ja bronhektaasia, kopsuemfüseemi ja hingamispuudulikkuse kliiniline pilt. Lapsed on äärmiselt vastuvõtlikud ägedatele respiratoorsetele viirus- ja bakteriaalsetele infektsioonidele, mis aitab kaasa bronhopulmonaalpatoloogia ägenemisele ja progresseerumisele. Võimalik on infektsioonist sõltuva bronhiaalastma teke.
Kooliealistel lastel võib tsüstiline fibroos avalduda "soolekoolikutena". Patsiendid kurdavad tugevat paroksüsmaalset kõhuvalu, puhitust ja korduvat oksendamist. Kõhu palpeerimisel määratakse tihedad moodustised, mis paiknevad jämesoole projektsioonis - väljaheited, mis on segatud paksu, tiheda limaga. Lapsed on väga altid hüpokloreemilise alkaloosi tekkele, mis on tingitud soola liigsest eritumisest higiga kuuma ilmaga, samal ajal kui lapse nahale ilmub "soolakülm".
Bronhopulmonaalsüsteemi häired täiskasvanutel
Tsüstilise fibroosiga (haiguse kopsuvorm) patsientidel esinevat bronhopulmonaalsüsteemi kahjustust iseloomustab kroonilise mädase obstruktiivse bronhiidi, bronhiektaasia, kroonilise kopsupõletiku, kopsuemfüseemi, hingamispuudulikkuse ja kopsu-südamehaiguse teke. Mõnedel patsientidel tekib pneumotooraks ja muud tsüstilise fibroosi tüsistused: atelektaas, kopsuabstsessid, hemoptüüs, kopsuverejooks ja infektsioonist sõltuv bronhiaalastma.
Patsiendid kurdavad valulikku paroksüsmaalset köha koos väga viskoosse, raskesti eraldatava limase ja mädase rögaga, mõnikord vere lisandiga. Lisaks on äärmiselt iseloomulik õhupuudus, mis esineb esmalt füüsilise koormuse ajal ja seejärel puhkeolekus. Õhupuuduse põhjuseks on bronhide obstruktsioon. Paljud patsiendid kurdavad polüpoosist ja sinusiidist tingitud kroonilist nohu. Iseloomulikud on ka märkimisväärne nõrkus, progresseeruv sooritusvõime langus ja sagedased ägedad hingamisteede viirushaigused. Uurimisel ilmneb kahvatu nahk, näo turse, nähtavate limaskestade tsüanoos ja tugev õhupuudus. Dekompenseeritud kopsuarteri haiguse tekkega ilmneb jalgade turse. Võib täheldada sõrmede otsmiste falangide paksenemist trummipulkade kujul ja küünte paksenemist kellaklaaside kujul. Rindkere omandab tünnikujulise kuju (kopsuemfüseemi tekke tõttu).
Kopsude löökpillidel on näha emfüseemi tunnuseid – kastikujuline heli, kopsuserva liikuvuse järsk piiramine ja kopsude alumise ääre langemine. Kopsude auskultatsioonil on näha rasket hingamist pika väljahingamisega, hajutatud kuiva vilistavat hingamist ning niisket keskmist ja peent mullitavat vilistavat hingamist. Raske kopsuemfüseemi korral on hingamine järsult nõrgenenud.
Tsüstilise fibroosi ekstrapulmonaalsed ilmingud
Tsüstilise fibroosi ekstrapulmonaalsed ilmingud võivad olla üsna väljendunud ja esineda sageli.
Pankrease kahjustus
85%-l tsüstilise fibroosiga patsientidest esineb erineva raskusastmega kõhunäärme eksokriinse funktsiooni puudulikkust. Kõhunäärme väiksemate kahjustuste korral maldigestiooni ja malabsorptsiooni sündroomid puuduvad, eksokriinse puudulikkuse laboratoorsed ilmingud on vaid laboratoorsed (trüpsiini ja lipaasi madal tase veres ja kaksteistsõrmiksoole sisus; sageli raske steatorröa). On teada, et maldigestiooni sündroomi ennetamiseks piisab vaid 1–2% lipaasi koguhulga sekretsioonist. Kliiniliselt avalduvad ainult olulised eksokriinse funktsiooni häired.
Normaalsetes tingimustes toodavad kõhunäärme atsinused ensüümiderikast vedelat sekreeti. Kui sekreet liigub mööda eritusjuhat, rikastub see vee ja anioonidega ning muutub veelgi vedelamaks. Tsüstilise fibroosi korral ei saa kõhunäärme sekreet transmembraanse regulaatori (kloriidikanali) struktuuri ja funktsiooni häire tõttu piisavalt vedelikku, see muutub viskoosseks ja selle liikumise kiirus mööda eritusjuhat aeglustub järsult. Sekreedi valgud ladestuvad väikeste eritusjuhade seintele, mille tulemuseks on nende ummistumine. Haiguse progresseerumisel areneb lõpuks atsinuste hävimine ja atroofia - tekib krooniline pankreatiit koos eksokriinse pankrease puudulikkusega. See kajastub kliiniliselt seedimise ja imendumishäirete sündroomide tekkes. Kõhunäärme puudulikkus on tsüstilise fibroosi korral rasvade imendumishäire peamine põhjus, kuid seda täheldatakse tavaliselt märkimisväärse lipaasidefitsiidi korral. Forsher ja Durie (1991) näitavad, et pankrease lipaasi täielikul puudumisel lagundatakse ja imendub rasv 50–60% ulatuses, mis on tingitud mao- ja süljeerituse (keelealuste) lipaaside olemasolust, mille aktiivsus on normi alumise piiri lähedal. Koos rasvade lagunemise ja imendumise häirega häirub ka valkude lagunemine ja reabsorptsioon. Umbes 50% toiduga saadud valgust läheb roojaga kaotsi. Süsivesikute imendumine on α-amülaasi puudulikkusest hoolimata vähemal määral mõjutatud, kuid süsivesikute ainevahetus võib olla oluliselt häiritud.
Kõhunäärme kahjustus väljendub seedimise ja imendumishäire sündroomi tekkes, millega kaasneb märkimisväärne kaalulangus ja rikkalik rasvane väljaheide.
Seedimise ja imendumishäirete sündroomide teket soodustab ka soole näärmete raske düsfunktsioon, soolemahla sekretsiooni häire ja sooleensüümide sisalduse vähenemine selles.
Maldigitsiooni ja malabsorptsiooni sündroome nimetatakse ka tsüstilise fibroosi soolevormiks.
Tsüstilise fibroosiga patsientidel haiguse hilisemas staadiumis (2% lastest ja 15% täiskasvanutest) on täheldatud kõhunäärme endokriinse funktsiooni häiret (diabetes mellitus).
 [ 16 ], [ 17 ], [ 18 ], [ 19 ]
[ 16 ], [ 17 ], [ 18 ], [ 19 ]
Maksa ja sapiteede kahjustused
13%-l tsüstilise fibroosi sega- ja soolevormiga patsientidest tekib maksatsirroos. Kõige tüüpilisem on see mutatsioonide W128X, delta-P508 ja X1303K korral. 5–10%-l patsientidest avastatakse biliaarne maksatsirroos koos portaalhüpertensiooniga. Welchi ja Smithi (1995) andmetel avastatakse maksakahjustuse kliinilisi, morfoloogilisi, laboratoorseid ja instrumentaalseid tunnuseid 86%-l tsüstilise fibroosiga patsientidest.
Paljudel tsüstilise fibroosiga patsientidel tekib ka krooniline koletsüstiit, sageli kalkulaarne.
Suguelundite talitlushäired
Tsüstilise fibroosiga patsientidel võib esineda azoospermiat, mis on viljatuse põhjus. Viljakuse vähenemine on naistele samuti tüüpiline.
Etapid
Kopsu tsüstilise fibroosi raskusaste on kolm.
Kerget tsüstilise fibroosi vormi iseloomustavad haruldased ägenemised (mitte rohkem kui üks kord aastas); remissiooniperioodidel kliinilised ilmingud praktiliselt puuduvad ja patsiendid on töövõimelised.
Mõõdukas raskusaste - ägenemisi täheldatakse 2-3 korda aastas ja need kestavad umbes 2 kuud või kauem. Ägenemise faasis esineb intensiivne köha raskesti eraldatava rögaga, õhupuudus isegi väikese füüsilise koormuse korral, subfebriilne kehatemperatuur, üldine nõrkus, higistamine. Samal ajal on häiritud kõhunäärme eksokriinne funktsioon. Remissioonifaasis ei ole töövõime täielikult taastunud, õhupuudus füüsilise koormuse ajal püsib.
Rasket kulgu iseloomustavad haiguse väga sagedased ägenemised. Remissioonid praktiliselt puuduvad. Kliinilises pildis tulevad esile raske hingamispuudulikkus, kroonilise kopsuhaiguse sümptomid, sageli dekompenseeritud, tüüpiline on hemoptüüs. Täheldatakse märkimisväärset kaalulangust, patsiendid on täielikult puudega. Reeglina kaasneb raske bronhopulmonaalse patoloogiaga kõhunäärme järsult väljendunud düsfunktsioon.
Vormid
- Bronhopulmonaalsed kahjustused
- Korduv ja korduv kopsupõletik pikaajalise kuluga.
- Abstsesseeruv kopsupõletik, eriti imikutel.
- Krooniline kopsupõletik, eriti kahepoolne.
- Bronhiaalastma, mis ei allu traditsioonilisele ravile.
- Korduv bronhiit, bronhioliit, eriti Pseudomonas aeruginosa kultuuri korral.
- Muutused seedetraktis
- Mekooniumi iileus ja selle ekvivalendid.
- Tundmatu päritoluga soolestiku imendumishäire sündroom.
- Obstruktiivne kollatõbi vastsündinutel pikaajalise kuluga.
- Maksatsirroos.
- Suhkurtõbi.
- Gastroösofageaalne refluks.
- Sapikivitõbi.
- Pärasoole prolaps.
- Muutused teistes organites ja süsteemides
- Kasvu- ja arenguhäired.
- Hilinenud seksuaalne areng.
- Meeste viljatus.
- Nina polüübid.
- Tsüstilise fibroosiga peredest pärit õed-vennad.
 [ 24 ]
[ 24 ]
Tüsistused ja tagajärjed
Seedetrakti tüsistused hõlmavad järgmist:
- Suhkurtõbi tekib 8–12%-l üle 25-aastastest patsientidest.
- Fibroosne kolonopaatia.
- Mekooniumi iileus vastsündinu perioodil (12%-l tsüstilise fibroosiga vastsündinutest), distaalne soole obstruktsiooni sündroom, pärasoole prolaps, peptiline haavandtõbi ja gastroösofageaalne reflukshaigus.
Maksa tüsistused:
- Rasvmaks (30–60% patsientidest),
- Fokaalne biliaarne tsirroos, multinodulaarne biliaarne tsirroos ja sellega kaasnev portaalhüpertensioon.
Portaalhüpertensioon põhjustab mõnikord söögitoru veenilaiendite tõttu surma.
Koletsüstiidi ja sapikivide levimus on tsüstilise fibroosiga patsientidel suurem kui teistel inimestel.
Hilinenud puberteet ja vähenenud viljakus ning muud tüsistused. Enamikul meestel esineb azoospermiat ja seemnejuhade vähearenenud arengut.
Diagnostika tsüstiline fibroos
Üldine vereanalüüs - tüüpiline on erineva raskusastmega aneemia, tavaliselt normo- või hüpokroomne. Aneemial on polüfaktoriaalne genees (raua ja B12-vitamiini imendumise vähenemine soolestikus malabsorptsioonisündroomi tekke tõttu). Võimalik on leukopeenia, millega kaasneb mädase bronhiidi ja kopsupõletiku teke - leukotsütoos, suurenenud erütrotsüütide settimine (ESR).
Üldine uriinianalüüs - olulisi muutusi pole, harvadel juhtudel täheldatakse kerget proteinuuriat.
Koproloogiline uuring - täheldatakse steatorröad ja kreatorröad. Becker (1987) soovitab mõõta kümotrüpsiini ja rasvhapete sisaldust väljaheites. Enne kümotrüpsiini määramist väljaheites on vaja seedeensüümide võtmine lõpetada vähemalt 3 päeva enne uuringut. Tsüstilise fibroosi korral on kümotrüpsiini hulk väljaheites vähenenud ja rasvhapete hulk suurenenud (rasvhapete normaalne eritumine on alla 20 mmol/päevas). On vaja arvestada, et rasvhapete suurenenud eritumist väljaheitega täheldatakse ka järgmistel juhtudel:
- konjugeeritud rasvhapete puudus peensooles maksapuudulikkuse, sapijuhade obstruktsiooni, peensoole olulise bakteriaalse koloniseerimise tõttu (sel juhul toimub sapphapete intensiivne hüdrolüüs);
- ileiit;
- tsöliaakia (koos malabsorptsioonisündroomi tekkega);
- enteriit;
- soolelümfoomid;
- Whipple'i tõbi;
- toiduallergiad;
- Toidumasside kiirenenud transiit erineva päritoluga kõhulahtisuse, kartsinoidsündroomi, türeotoksikoosi korral.
Biokeemiline vereanalüüs - üldvalgu ja albumiini taseme langus, alfa2- ja gammaglobuliinide, bilirubiini ja aminotransferaaside taseme tõus (maksakahjustuse korral), amülaasi, lipaasi, trüpsiini ning raua- ja kaltsiumitaseme langus (malidigestiooni sündroomi, malabsorptsiooni tekke korral).
Röga analüüs - suure hulga neutrofiilsete leukotsüütide ja mikroorganismide olemasolu (röga bakterioskoopia ajal).
Peensoole imendumisfunktsiooni ja kõhunäärme eksokriinse funktsiooni uuring näitab olulisi häireid.
Kopsude röntgenuuring - näitab muutusi, mille raskusaste sõltub haiguse raskusastmest ja faasist. Kõige iseloomulikumad muutused on:
- suurenenud kopsude mustrid peribronhiaalsete interstitsiaalsete muutuste tõttu;
- kopsude juurte laienemine;
- pilt kopsude lobulaarsest, subsegmentaalsest või isegi segmentaalsest atelektaasist;
- kopsuväljade suurenenud läbipaistvus, peamiselt ülemistes sektsioonides, diafragma madal asend ja ebapiisav liikuvus, retrosternaalse ruumi laienemine (kopsuemfüseemi ilming);
- kopsukoe segmentaalne või polüsegmentaalne infiltratsioon (kopsupõletiku tekkes).
Bronhograafia paljastab viskoosse röga poolt bronhide ummistumisest tingitud muutused (kontrastaine bronhide täidise killustumine, ebaühtlased kontuurid, bronhide rebenemise nähtus, külgmiste harude arvu oluline vähenemine), samuti bronhoekgaasid (silindrilised, segatud), mis lokaliseeruvad peamiselt kopsude alumistes osades.
Bronhoskoopia abil avastatakse difuusne mädane bronhiit koos rohke paksu, viskoosse röga ja fibriinsete kilega.
Spiromeetria - juba haiguse algstaadiumis näitab obstruktiivset tüüpi hingamispuudulikkust (vähenenud FVC, FEV1, Tiffno indeks), piiravat (vähenenud FVC) või enamasti obstruktiivselt piiravat (vähenenud FVC, FVC, FEV1, Tiffno indeks).
Gibsoni ja Cooki higitest (higi elektrolüütide test) hõlmab higistamise stimuleerimist pilokarpiini elektroforeesi abil, millele järgneb kloriidide määramine higis. Doerehuk (1987) kirjeldab testi järgmiselt. Pilokarpiini elektroforees viiakse läbi käsivarrel, elektrivool on 3 mA. Pärast naha puhastamist destilleeritud veega kogutakse higi stimuleeritud piirkonnale asetatud filterpaberi abil, mis on kaetud marliga, et vältida aurustumist. 30–60 minuti pärast eemaldatakse filterpaber ja elueeritakse destilleeritud veega. Mõõdetakse kogutud higi kogus. Usaldusväärsete tulemuste saamiseks on vaja koguda vähemalt 50 mg (eelistatavalt 100 mg) higi.
Kui kloriidi kontsentratsioon on üle 60 mmol/l, peetakse tsüstilise fibroosi diagnoosi tõenäoliseks; kui kloriidi kontsentratsioon on üle 100 mmol/l, on see usaldusväärne; sel juhul ei tohiks kloori ja naatriumi kontsentratsiooni erinevus ületada 8-10 mmol/l. Hadson (1983) soovitab, et kui higi naatriumi ja kloriidi sisaldus on piiripealne, tuleks teha prednisolooni test (5 mg suu kaudu 2 päeva jooksul, millele järgneb higi elektrolüütide määramine). Isikutel, kes ei põe tsüstilist fibroosi, langeb higi naatriumisisaldus normi alumise piirini; tsüstilise fibroosi korral see ei muutu. Higitesti on soovitatav teha igale kroonilise köhaga lapsele.
Tsüstilise fibroosi geeni peamiste mutatsioonide tuvastamine vereproovidest või DNA-proovidest on kõige tundlikum ja spetsiifilisem diagnostiline test. See meetod sobib aga ainult riikidele, kus delta-P508 mutatsioonimäär on üle 80%. Lisaks on tehnika väga kallis ja tehniliselt keeruline.
Tsüstilise fibroosi sünnieelne diagnoosimine toimub lootevees leeliselise fosfataasi isoensüümide määramise teel. See meetod on võimalik alates 18.-20. rasedusnädalast.
Tsüstilise fibroosi diagnoosimise peamised kriteeriumid on järgmised:
- näidustused lapsepõlves hilinenud füüsilise arengu anamneesis, korduvad kroonilised hingamisteede haigused, düspeptilised häired ja kõhulahtisus, tsüstilise fibroosi esinemine lähisugulastel;
- krooniline obstruktiivne bronhiit, sageli korduv, koos bronhektaasia ja kopsuemfüseemi tekkega, sageli korduv kopsupõletik;
- krooniline korduv pankreatiit koos eksokriinse funktsiooni märgatava vähenemisega, malabsorptsioonisündroom;
- suurenenud kloorisisaldus patsiendi higis;
- viljatus säilinud seksuaalfunktsiooniga.
Tsüstilise fibroosi eduka diagnoosimise ja diferentsiaaldiagnoosimise hõlbustab riskirühmade kindlakstegemine.
Tsüstilise fibroosi sõeluuringu programm
- Vere, uriini, röga üldanalüüs.
- Röga bakterioloogiline analüüs.
- Koproloogiline analüüs.
- Biokeemiline vereanalüüs: kogu valgu ja valgufraktsioonide, glükoosi, bilirubiini, aminotransferaaside, aluselise fosfataasi, gamma-glutamüültranspeptidaaside, kaaliumi, kaltsiumi, raua, lipaasi, amülaasi, trüpsiini määramine.
- Kõhunäärme eksokriinse funktsiooni ja soolestiku imendumisfunktsiooni uurimine.
- Kopsude fluoroskoopia ja radiograafia, kopsude kompuutertomograafia.
- EKG.
- Ehhokardiograafia.
- Bronhoskoopia ja bronhograafia.
- Spiromeetria.
- Higiproov.
- Konsultatsioon geneetikuga.
- Vereproovide või DNA-proovide analüüs tsüstilise fibroosi geeni peamiste mutatsioonide suhtes.
Millised testid on vajalikud?
Kellega ühendust võtta?
Ravi tsüstiline fibroos
Tsüstilise fibroosi sümptomite tüüp ja raskusaste võivad olla väga erinevad, seega puudub tüüpiline raviplaan; see on iga inimese jaoks individuaalne.
Teraapia koosneb järgmistest terapeutilistest meetmetest:
- Hingamisharjutused ja posturaalne drenaaž aitavad vabaneda kopsudesse kogunevast paksust limast. Mõned hingamisteede puhastamise tehnikad vajavad pereliikmete, sõprade või pulmonoloogi abi. Paljud inimesed kasutavad täispuhutavat rinnavesti, mis vibreerib kõrgel sagedusel.

- Inhaleeritavad ravimid, millel on bronhodilateeriv, drenaaž (mukolüütikumid) ja antibakteriaalne toime (näiteks fluorokinoloonid).
- Pankrease ensüüme sisaldavad preparaadid seedimise parandamiseks. Neid preparaate võetakse söögi ajal.
- Multivitamiinid (sh rasvlahustuvad vitamiinid).
2015. aastal kiitis FDA heaks teise ravimi tsüstilise fibroosi raviks, mis on suunatud defektsele valgule, mida tuntakse CFTR-ina. Esimene ravim, nn CFTR-modulaator, kiideti heaks 2012. aastal. CFTR-modulaatoritelt oodatakse mõnede tsüstilise fibroosiga inimeste eluea pikendamist aastakümnete võrra.
Järgmiste hingamisteede tüsistuste raviks võib olla vajalik operatsioon:
- Pneumotooraks, massiline korduv või püsiv hemoptüüs, ninapolüübid, püsiv ja krooniline sinusiit.
- Mekooniumi iileus, soolesulgus, pärasoole prolaps.
Kopsu siirdamine viiakse läbi haiguse lõppstaadiumis.
Prognoos
Tsüstilise fibroosiga patsientide keskmine elulemus on 35–40 aastat. Meeste keskmine elulemus on kõrgem kui naistel.
Tänapäevaste ravistrateegiate abil jõuab täiskasvanuikka 80% patsientidest. Tsüstiline fibroos piirab aga oluliselt patsiendi funktsionaalseid võimeid. Sellele haigusele pole siiani ravi.

