Artikli meditsiiniline ekspert
Uued väljaanded
Tsütomegaloviiruse hepatiit
Last reviewed: 05.07.2025

Kõik iLive'i sisu vaadatakse meditsiiniliselt läbi või seda kontrollitakse, et tagada võimalikult suur faktiline täpsus.
Meil on ranged allhanke juhised ja link ainult mainekate meediakanalite, akadeemiliste teadusasutuste ja võimaluse korral meditsiiniliselt vastastikuste eksperthinnangutega. Pange tähele, et sulgudes ([1], [2] jne) olevad numbrid on nende uuringute linkideks.
Kui tunnete, et mõni meie sisu on ebatäpne, aegunud või muul viisil küsitav, valige see ja vajutage Ctrl + Enter.
Epidemioloogia
CMV-nakkus on laialt levinud. 70–80%-l täiskasvanutest on veres viirust neutraliseerivad antikehad. Viirus eritub uriiniga 4–5%-l rasedatest, emakakaela kraapimisel avastatakse seda 10%-l naistest ja piimas 5–15%-l imetavatest emadest. Erinevatel põhjustel surnud vastsündinute seas avastatakse generaliseerunud CMV-infektsiooni tunnuseid 5–15%-l. Tsütomegaloviirushepatiit moodustab 1% viirusliku etioloogiaga ägeda ikterilise hepatiidi etioloogilisest struktuurist. Tsütomegaloviirushepatiidi levimust tervikuna pole aga seni uuritud.
CMV-nakkuse allikaks on ainult inimene, haige inimene või viiruse kandja. Edastamine toimub kontakti teel, harvemini õhus levivate piiskade ja enteraalselt. Lisaks võib infektsioon toimuda parenteraalselt, sealhulgas vereülekannete ajal. See edastustee on ilmselt sagedasem, kui üldiselt arvatakse, mida kinnitab tsütomegaloviiruse sagedane tuvastamine doonoritel (kuni 60%). Transplatsentaarne infektsioonitee on usaldusväärselt tõestatud. Loote nakatumine toimub emalt - viiruse kandjalt. Nakkus kandub edasi otse platsenta kaudu või sünnituse ajal lapse läbimisel sünnituskanalist. Vastsündinud võivad nakatuda emapiima kaudu.
Tsütomegaloviiruse hepatiidi korral on domineerivad nakkusteed ilmselt parenteraalsed ja perinataalsed, kui tsütomegaloviirus siseneb otse verre, möödudes patsiendi lümfoidsest aparaadist.
Põhjused tsütomegaloviiruse hepatiit
Tsütomegaloviirus, mis kuulub Herpesviridae perekonda, eraldati 1956. aastal M. Smithi poolt. Kaasaegse klassifikatsiooni kohaselt nimetatakse seda inimese herpesviiruse tüübiks 5 (HHV5). Praegu on teada kaks tsütomegaloviiruse serotüüpi. Morfoloogiliselt sarnaneb see herpes simplex viirusega. Virion sisaldab DNA-d, selle läbimõõt on 120–140 nm ning see kultiveerub hästi inimese embrüo fibroblastide kultuuris. Viirus säilib hästi toatemperatuuril, on tundlik eetri ja desinfitseerimisvahendite suhtes. Sellel on nõrk interferonogeenne toime. Tsütomegaloviirus põhjustab haigusi ainult inimestel. Loode ja vastsündinud on viiruse suhtes eriti tundlikud.
Pathogens
Pathogenesis
Tsütomegaloviirushepatiidi patogenees on siiani ebaselge. Traditsiooniliselt arvatakse, et CMV mõjutab kolestaatilise hepatiidi tekkega peamiselt sapiteid. Siiski on lubatud CMV otsene tsütopaatiline toime otse maksa parenhüümile. Mõned peavad tsütomegaloviirust vaieldamatuks hepatotroopseks agensiks. Sellisel juhul võib maksakahjustusi täheldada nii kaasasündinud kui ka omandatud CMV-infektsiooni korral.
Tsütomegaloviiruse hepatiidi korral hepatotsüütide isoleeritud kahjustuste tekkimisel võib olulist rolli mängida patogeeni otsene sisenemine verre (parenteraalne nakkusmehhanism). Sellisel juhul ei sisene viirus lümfisüsteemi ja seega ka piirkondlikesse lümfisõlmedesse ning veelgi vähem ei paljune neis. Patogeen ilmub koheselt üldisesse vereringesse, kust see siseneb maksa parenhüümi. Seda patogeneetilise ahela faasi võib tavapäraselt nimetada parenhüümseks difusiooniks. Sellisel juhul võib viirus kohe tungida hepatotsüütidesse, kus see leiab tingimused paljunemiseks.
Isoleeritud tsütomegaloviiruse hepatiidi patogeneesis ei saa välistada erinevate tsütomegaloviiruse genotüüpide rolli, samuti vastuvõtliku indiviidi 6. kromosoomi peamise histosobivuskompleksi (HLA-süsteemi) kandidaatgeenide polümorfismi.
Patomorfoloogia
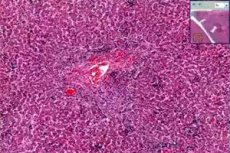
Tervetel täiskasvanutel esineva ägeda tsütomegaloviiruse hepatiidi morfoloogilisi muutusi iseloomustab intralobulaarsete granuloomide kombinatsioon mononukleaarsete rakkude sinusoidaalse infiltratsiooniga, samuti periportaalne põletik. Hepatotsüütide nekroos võib olla kerge.
Neerusiirdamise läbinud immuunpuudulikkusega täiskasvanutel, kellel on krooniline tsütomegaloviiruse hepatiit, täheldatakse periportaalset ja perisinusoidaalset fibroosi, segarakkude infiltratsiooni, hepatotsüütide paisumist ja kolestaasi tunnuseid. Haiguse varases staadiumis tuvastatakse tsütomegaloviiruse antigeene maksas sinusoidaalsetes rakkudes viiruse hematogeense leviku tagajärjel. Täheldatakse hepatotsüütides nekrootilisi, düstroofseid muutusi, lümfotsüütilist infiltratsiooni ja Kupfferi rakkude aktivatsiooni, samas kui spetsiifiline rakkude transformatsioon on haruldane. Tsütomegaloviirushepatiidiga kaasneb neil patsientidel kolestaatiline sündroom ja sapijuhade kadumise sündroom. Sellisel juhul tuvastatakse hepatotsüütides pp65 antigeneemia ja CMV DNA ning võivad ilmneda maksatsirroosi tunnused.
Lisaks viirushepatiidile iseloomulikele klassikalistele muutustele võivad tsütomegaloviiruse põhjustatud maksakahjustusega patsientidel esineda väikesed neutrofiilsete polümorfonukleaarsete leukotsüütide agregaadid, mis sageli paiknevad nakatunud hepatotsüüdi ümber koos tuumasiseste CMV inklusioonidega. Immunohistokeemilised meetodid on näidanud, et klassikaliste tuumasiseste CMV inklusioonideta rakkudes on tsütoplasma basofiilne granulaarsus põhjustatud tsütomegaloviiruse materjali olemasolust. Seega on CMV hepatiidi iseloomulikuks tunnuseks mitte ainult viiruse tuumasisene inklusioon, vaid ka tsütoplasma basofiilne granulaarsus.
Üldiselt on immuunpuudulikkusega patsientidel CMV-nakkusel tugevam tsütopatogeenne toime ja see põhjustab hepatotsüütide ulatuslikumat lüüsi kui immuunkompetentsetel CMV-hepatiidiga patsientidel.
Kaasasündinud CMV-hepatiidiga laste maksakoe morfoloogilisi muutusi iseloomustab hepatotsüütide hiiglaslik rakutransformatsioon, kolestaas, portaalfibroos, sapijuha epiteeli proliferatsioon ja fulminantsete vormide korral massiivne maksanekroos.
Sümptomid tsütomegaloviiruse hepatiit
Tsütomegaloviiruse hepatiit võib esineda nii ägedas kui ka kroonilises vormis.
 [ 23 ]
[ 23 ]
Äge omandatud tsütomegaloviiruse hepatiit
Omandatud ägedat CMV-hepatiiti lastel, noorukitel ja noortel täiskasvanutel saab diagnoosida infektsioosse mononukleoosi sümptomite kompleksi osana. Mõnel juhul täheldatakse siiski isoleeritud maksakahjustust. Sellisel juhul esineb haigus anikterilise, kerge, mõõduka või raske vormina. Üksikjuhtudel võib tekkida fulminantne hepatiit.
CMV-hepatiidi inkubatsiooniperioodi pole täpselt kindlaks määratud. See on arvatavasti 2-3 kuud.
Preikteriline periood. Ägeda CMV-hepatiidi kliinilised ilmingud ja laboratoorsed parameetrid ei erine põhimõtteliselt teiste etioloogiatega viirushepatiidi omadest. Haigus algab järk-järgult. Patsientidel esineb isutus, nõrkus, peavalu, kõhuvalu. Mõnel juhul tõuseb kehatemperatuur 38 °C-ni.
Ägeda CMV-hepatiidi A preikterilise perioodi kestus on tavaliselt 3 kuni 7 päeva.
Preikteriaalse perioodi kliinilised ilmingud võivad puududa. Sellistel juhtudel debüteerib tsütomegaloviiruse hepatiidi manifestne esialgne vorm kollatõve ilmnemisega.
Kollatõbi. Patsientidel pärast kollatõve algust püsivad või isegi süvenevad eelkollatõve perioodil täheldatud joobeseisundi sümptomid.
Ägeda tsütomegaloviiruse hepatiidi kliinilised ja laboratoorsed ilmingud ei erine põhimõtteliselt teiste etioloogiate viirushepatiidi ilmingutest.
Ägeda tsütomegaloviiruse hepatiidi korral kestab ikteriline periood 13 kuni 28 päeva.
Haiguse postikterilist perioodi iseloomustab patsiendi heaolu normaliseerumine, maksa ja põrna suuruse vähenemine ning ensüümi aktiivsuse märkimisväärne langus.
Krooniline tsütomegaloviiruse hepatiit
Krooniline tsütomegaloviiruse hepatiit tekib kõige sagedamini immuunpuudulikkusega patsientidel (HIV-nakkusega, immunosupressiivset ravi saavatel, maksasiirdamise läbinud patsientidel jne). Seega täheldatakse tsütomegaloviiruse siiriku kahjustusi 11–28,5%-l patsientidest, kellele on erinevatel põhjustel (autoimmuunsed maksahaigused, viirushepatiit jne) tehtud maksasiirdamine. CMV DNA-d tuvastatakse hepatotsüütides 20%-l maksasiirdamise läbinud patsientidest, kellel on hepatiidi kliiniline, biokeemiline ja histoloogiline pilt.
Kroonilise tsütomegaloviiruse hepatiidi teke on aga võimalik ka immuunkompetentsetel lastel ja täiskasvanutel. Sellisel juhul võib krooniline hepatiit areneda primaarse kroonilise protsessina või esialgse manifesteerunud tsütomegaloviiruse hepatiidi tagajärjel.
Kroonilise CMV-hepatiidiga patsientide kliinilised ja laboratoorsed parameetrid ei erine põhimõtteliselt teiste etioloogiatega kroonilise viirushepatiidi korral täheldatutest.
Omandatud kroonilise CMV-hepatiidiga patsientidel domineerib protsessi madal ja mõõdukas aktiivsus. Peaaegu 3/4 juhtudest diagnoositakse mõõdukas ja raske maksafibroos.
Remissiooniperioodil on omandatud kroonilise CMV-hepatiidiga patsientidel joobeseisundi sümptomid praktiliselt puuduvad. Enamikul patsientidest kaovad ekstrahepaatilised ilmingud. Maks ja põrn vähenevad, kuid nende täielikku normaliseerumist ei täheldata. Tavaliselt ulatub maksa serv roidekaare alt välja mitte rohkem kui 1-2 cm. Põrna palpeeritakse roidekaare servast vähem kui 1 cm allpool. Ensüümide aktiivsus vereseerumis ei ületa normaalseid väärtusi.
Omandatud tsütomegaloviiruse hepatiidi kliinilised ilmingud vastavad erineva raskusastmega ägeda ja kroonilise viirushepatiidi ilmingutele. 3/4 omandatud kroonilise tsütomegaloviiruse hepatiidi juhtudest diagnoositakse mõõdukas ja raske maksafibroos.
 [ 26 ], [ 27 ], [ 28 ], [ 29 ], [ 30 ]
[ 26 ], [ 27 ], [ 28 ], [ 29 ], [ 30 ]
Kaasasündinud tsütomegaloviiruse hepatiit
Kaasasündinud CMV-infektsioon võib esineda nii üldistatud kujul, millega kaasneb paljude organite ja süsteemide kahjustus, kui ka lokaliseeritud kujul, sealhulgas maksas. Maksakahjustus on kaasasündinud CMV-infektsioonile tüüpiline ja esineb 40–63,3%-l patsientidest. Maksa muutuste hulka kuuluvad krooniline hepatiit, tsirroos, kolangiit, intralobulaarne kolestaas. Registreeritakse ekstrahepaatiliste sapiteede kahjustusi põletikust kuni atresiani. Praeguseks on tsütomegaloviiruse roll ekstrahepaatiliste sapiteede kahjustuste (atresia, tsüstid) tekkes ebaselge.
Kaasasündinud tsütomegaloviirushepatiiti registreeritakse peamiselt esimestel elukuudel lastel, see kulgeb kas anikterilises vormis koos hepato-splenomegaalia ja biokeemilise aktiivsusega või ikterilises vormis koos ikteruse, tumeda uriini, hepatosplenomegaalia, hüpertransaminaseemia, alkaalse fosfataasi ja GGT taseme tõusuga ning pooltel patsientidest maksatsirroosi tekkega. Samal ajal võib kaasasündinud tsütomegaloviirushepatiit kulgeda ägeda ja pikaajalise vormina koos ühe- või kahelainelise ikterusega, kergete joobeseisundite ilmingutega, hepatotsellulaarsete ensüümide aktiivsuse suurenemisega 2-3 korda, kolestaatilise sündroomiga (1/3 patsientidest), harva kroonilise kulguga, mis nendel juhtudel areneb primaarse kroonilise protsessina, mis toimub ilma ikteruseta ja mõõduka või kõrge patoloogilise aktiivsusega.
 [ 31 ], [ 32 ], [ 33 ], [ 34 ], [ 35 ], [ 36 ], [ 37 ]
[ 31 ], [ 32 ], [ 33 ], [ 34 ], [ 35 ], [ 36 ], [ 37 ]
Kaasasündinud primaarne krooniline tsütomegaloviiruse hepatiit
Kaasasündinud kroonilise CMV-hepatiidiga laste seas diagnoositakse maksas patoloogilise protsessi minimaalne aktiivsus 1/4 juhtudest, madal aktiivsus 1/3 juhtudest ja mõõdukas aktiivsus 1/3 patsientidest.
Protsessil on väljendunud fibroosi tekitav suund. 1/3 patsientidest diagnoositakse väljendunud fibroos, 1/3-l - maksatsirroosi tunnused.
Kaasasündinud kroonilise CMV-hepatiidi kliinilistel ilmingutel ja laboratoorsetel parameetritel ei ole olulisi erinevusi teiste etioloogiate viirushepatiidist.
Remissiooniperioodil on kaasasündinud kroonilise CMV-hepatiidiga patsientidel joobesnähud praktiliselt puuduvad. Enamikul lastest kaovad ekstrahepaatilised ilmingud. Maks ja põrn vähenevad, kuid nende täielikku normaliseerumist ei täheldata. Tavaliselt ulatub maksa serv roidekaare alt mitte rohkem kui 1-2 cm. Enamikul splenomegaaliaga patsientidest on põrn palpeeritav vähem kui 1 cm roidekaare servast allpool. Ensüümide aktiivsus vereseerumis ei ületa normaalseid väärtusi.
Tsütomegaloviiruse hepatiit maksasiirdamise patsientidel
Tsütomegaloviirushepatiit on CMV-infektsiooni kõige sagedasem ilming immunosupressiivse ravi taustal. Sellistel juhtudel diagnoositakse tsütomegaloviiruse hepatiit maksa biopsia tulemuste põhjal ja kinnitatakse viiruskultuuri, ppb5 antigeeni, PCR-i ja immunohistokeemia meetodil. Enamikul CMV-hepatiidiga patsientidest tekib isoleeritud maksakahjustus ja ainult vähestel patsientidel tekib generaliseerunud CMV-infektsioon. Patsientidele määratakse intravenoosne gantsükloviir. AIDS-i korral täheldatakse tsütomegaloviiruse hepatiiti 3-5% patsientidest.
Ortotoopilise maksa siirdamise läbinud patsientidel ja AIDS-i korral on võimalik tsütomegaloviiruse etioloogiaga ekstrahepaatiliste sapijuhade striktuuride teke, mida kinnitab viiruse B tuvastamine sapijuhade epiteelis. Doonori ja retsipiendi maksa nakatumist tsütomegaloviirusega enne siirdamist peetakse transplantaadi äratõukereaktsiooni soodustavaks teguriks.
 [ 41 ], [ 42 ], [ 43 ], [ 44 ], [ 45 ], [ 46 ]
[ 41 ], [ 42 ], [ 43 ], [ 44 ], [ 45 ], [ 46 ]
Tsütomegaloviiruse hepatiidi kulg
Haiguse kulg võib olla äge (35%) ja lõppeda taastumisega, kusjuures maksa funktsionaalne seisund taastub täielikult 1–3 kuu jooksul. 65% patsientidest muutub haigus manifestse tsütomegaloviiruse hepatiidi tagajärjel krooniliseks.
Kus see haiget tekitab?
Diagnostika tsütomegaloviiruse hepatiit
Tsütomegaloviiruse hepatiiti diagnoositakse kliiniliste, biokeemiliste ja seroloogiliste andmete kombinatsiooni põhjal. Haigus algab tavaliselt asteno-düspeptiliste ilmingutega: halb enesetunne, nõrkus, isutus, millega kaasneb maksa suurenemine ja hüperfermenteemia. Patsiendi anamnees võib viidata parenteraalsetele manipulatsioonidele 2-3 kuud enne praegust haigust, vereseerumis ei ole hepatiitviiruste A, B, C, U, G jne markereid.
Oluline on arvestada, et tsütomegaloviiruse hepatiiti iseloomustab väljendunud tsütolüüsi sündroom. Selle näidustuseks kasutatakse laialdaselt aminotransferaaside aktiivsuse (ALAT, ASAT) ja LDH fraktsioonide (LDH-4, LDH-5) määramist. Maksarakkude ensüümide suurenenud aktiivsus on iseloomulik ägedale hepatiidile ja kroonilise tsütomegaloviiruse hepatiidi ägenemise staadiumile. Maksarakkude ensüümide aktiivsuse suurenemise aste tsütomegaloviiruse hepatiidi erinevates vormides vastab teiste etioloogiatega viirushepatiidi omale.
Kollatõve korral on oluline määrata kogu bilirubiini tase ja konjugeeritud ja konjugeerimata fraktsioonide suhe.
Põletikulise protsessi aktiivsust maksas peegeldab teatud määral vereseerumi valguspekter. Enamikul juhtudel säilib kroonilise CMV-hepatiidiga patsientidel vereseerumis normaalne üldvalgu tase - 65–80 g/l. Kõrge aktiivsusega kroonilise CMV-hepatiidiga patsientidel tekib düsproteineemia albumiinide taseme languse ja γ-globulite ja noovade osakaalu suurenemise tõttu. Düsproteineemia iseloom on mõõdukas ja saavutab olulise ekspressiooni ainult mõnedel patsientidel, kui albumiini tase langeb alla 45% ja γ-globuliini tase ületab 25%.
Kroonilise tsütomegaloviiruse hepatiidi ägenemise ajal on valgusünteesi funktsiooni langus seda olulisem, mida raskem on maksa põletikuline protsess. Kroonilise hepatiidiga patsientidel tekivad erineva raskusastmega vere hüübimissüsteemi häired (hüpokoagulatsioon) peamiselt maksa sünteesifunktsiooni vähenemise tõttu.
Ägeda ja kroonilise CMV-hepatiidi korral maksas esinev ultrahelipilt ei erine teiste etioloogiatega viirushepatiidi omast.
Doppleri ultraheli meetodit kasutatakse portaalveeni süsteemi verevoolu ja portokavaalsete anastomooside olemasolu määramiseks, mis võimaldab diagnoosida portaalhüpertensiooni, sealhulgas tsütomegaloviiruse etioloogiaga maksatsirroosiga patsientidel.
Morfoloogilised uuringud võimaldavad objektiivselt hinnata maksa patoloogilise protsessi olemust, selle suunda ja on ka üks ravi efektiivsuse kohustuslikest kriteeriumidest.
Punktsioonbiopsia tulemustel võib olla otsustav diferentsiaaldiagnostiline väärtus. Piisava suurusega maksapunktsiooni korral on saadud morfoloogilisel informatsioonil määrav tähtsus kroonilise hepatiidi aktiivsuse ja fibroosi astme hindamisel ning ravitaktika valikul.
Mida tuleb uurida?
Millised testid on vajalikud?
Kellega ühendust võtta?
Ravi tsütomegaloviiruse hepatiit
Gantsükloviiri ja rekombinantse interferoon A preparaate kasutatakse tsütomegaloviiruse hepatiidi raviks.
Allpool on esitatud ühe kliinilise uuringu tulemused, milles raviti 85 last, kes said Viferon-ravi kroonilise tsütomegaloviiruse hepatiidi raviks. Neist 31 lapsel oli omandatud ja 54-l kaasasündinud CMV-hepatiit. 49 lapsel esines kaasasündinud tsütomegaloviiruse hepatiiti koos sapiteede kahjustusega (44-l atreesia ja 5-l sapijuhade tsüstid) ning viiel lapsel kesknärvisüsteemi kahjustusega.
Vaadeldud patsientide seas oli 47 poissi ja 38 tüdrukut. 55 last olid alla 1-aastased, 23 olid 1–3-aastased ja 7 olid üle 3-aastased.
Kroonilise viirushepatiidi ravis said 45 last Viferoni monoteraapiat rektaalküünalde kujul, 31 Viferonit kombinatsioonis intravenoossete immunoglobuliinidega ja 9 last kombinatsioonravi, mis koosnes Viferonist ja gantsükloviirist. Interferooni annus on 5 miljonit/m2 3 korda nädalas.
Ravikuuri kestus oli 67 patsiendil 6 kuud, 11 patsiendil 9 kuud ja 7 lapsel 12 kuud. Interferoonravi efektiivsuse kriteeriumid määrati vastavalt EUROHEP-i konsensusele.
Kontrollgrupp koosnes 43 lapsest. See hõlmas 29 kaasasündinud ja 14 kroonilise tsütomegaloviiruse etioloogiaga hepatiidiga patsienti. Need lapsed said baasravi, mis hõlmas ainult kolereetikume, vitamiinipreparaate ja hepatoprotektoreid.
Lisaks kliinilisele ja biokeemilisele jälgimisele kontrolliti haiguse kulgu jälgides ka tsütomegaloviiruse replikatiivset aktiivsust.
Viferon-ravi taustal täieliku remissiooni saavutanud kroonilise CMV-hepatiidiga laste osakaal oli madal ega ulatunud 20%-ni. Siiski moodustas mõningase remissiooni saavutanud laste koondrühm 78,8% ravitud laste koguarvust. Samal ajal puudus remissioon peaaegu 1/4-l patsientidest. Samuti tuleb märkida, et kontrollrühmas ei tekkinud sama aja jooksul ühelgi lapsel spontaanset remissiooni.
Viferoonravi efektiivsuse võrdlev analüüs kaasasündinud ja omandatud CMV-hepatiidiga lastel näitas, et viferoonravi taustal ei leitud usaldusväärseid erinevusi remissiooni tekke protsendis. P-väärtused olid vahemikus p>0,05 kuni p>0,2.
Küsimusele tsütomegaloviiruse hepatiidi remissiooni saavutamise sageduse sõltuvuse kohta ravi ajal raviskeemist eristati 3 rühma. Esimesse kuulusid patsiendid, kes said Viferoni monoteraapiat, teise - lapsed, kes said Viferonit kombinatsioonis intravenoossete immunoglobuliinidega, ja kolmandasse - need, kes said kombineeritud ravi Viferoni ja gantsükloviiriga.
Erinevate rühmade patsientide ravitulemustes olulisi erinevusi ei täheldatud. Viferoni ja intravenoossete immunoglobuliinide kombinatsioonravi saavatel lastel täheldati vaid kalduvust tsütolüüsi raskusastme langusele. P-väärtused olid vahemikus p>0,05 kuni p>0,1.
Sarnast mustrit täheldati ka CMV replikatiivse aktiivsuse hindamisel kroonilise tsütomegaloviiruse hepatiidi korral lastel, kes said erinevaid raviskeeme. CMV DNA tuvastamise sagedus dünaamilise vaatluse ajal oli kõigi kolme rühma lastel praktiliselt identne. Viferoniga ravitud patsientidel koos intravenoossete immunoglobuliinidega täheldati CMV replikatiivset aktiivsust vaid veidi madalamal tasemel. P-väärtused olid vahemikus p>0,05 kuni p>0,2.
Rohkem informatsiooni ravi kohta
Ärahoidmine
CMV-nakkuse spetsiifilist ennetamist pole välja töötatud. Vaktsiini loomiseks on käimas eksperimentaalne töö.
Epideemiavastaseid meetmeid infektsioonikolletes ei rakendata. Arvestades parenteraalse infektsioonimehhanismi potentsiaalset rolli tsütomegaloviiruse hepatiidi tekkes, tunduvad eriti olulised meetmed parenteraalse, sealhulgas vereülekandega nakatumise kõigi võimaluste mahasurumiseks. Ühekordselt kasutatavate nõelte kasutamine ja kirurgiliste instrumentide steriliseerimise eeskirjade järgimine võivad parenteraalsete manipulatsioonide ajal nakkuse täielikult ära hoida.
Tsütomegaloviirusega nakatumise vältimiseks vere ja selle komponentide transfusiooni ajal on vaja otsustada doonori vere testimise üle CMV DNA suhtes.

