Waldenströmi B-rakuline lümfoplasmatsüütiline lümfoom
Viimati vaadatud: 12.03.2022

Kõik iLive'i sisu vaadatakse meditsiiniliselt läbi või seda kontrollitakse, et tagada võimalikult suur faktiline täpsus.
Meil on ranged allhanke juhised ja link ainult mainekate meediakanalite, akadeemiliste teadusasutuste ja võimaluse korral meditsiiniliselt vastastikuste eksperthinnangutega. Pange tähele, et sulgudes ([1], [2] jne) olevad numbrid on nende uuringute linkideks.
Kui tunnete, et mõni meie sisu on ebatäpne, aegunud või muul viisil küsitav, valige see ja vajutage Ctrl + Enter.
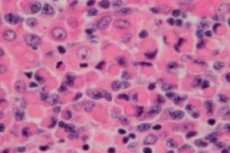
Seoses pahaloomuliste lümfoproliferatiivsete (immunoproliferatiivsete) haiguste kategooriaga on lümfoplasmatsüütiline lümfoom ehk Waldenströmi makroglobulineemia väikeste B-lümfotsüütide rakuline kasvaja - B-rakud, mis tagavad lümfisüsteemi kaitsefunktsioonid ja keha humoraalse immuunsuse. Diagnoosi tuleks teha alles pärast kõigi teiste väikeste B-rakuliste lümfoomide välistamist. Waldenströmi makroglobulineemiat kirjeldas 1944. Aastal Jan G. Waldenstrom, kes teatas kahel patsiendil ebatavalistest lümfadenopaatia verejooksu, aneemia, suurenenud settimise, hüperviskoossuse ja hüpergammaglobulineemia ilmingutest. [1], [2]
Epidemioloogia
Seda tüüpi lümfoom on haruldane, loid hematoloogiline pahaloomuline kasvaja ja kliinilise statistika hinnangul on selle esinemissagedus selles haiguste rühmas ligikaudu 2%. Pealegi on meespatsiente peaaegu kaks korda rohkem kui naispatsiente.
Mõnede aruannete kohaselt on lümfoplasmatsüütilise lümfoomi iga-aastaste juhtude sagedus Euroopas üks 102 tuhande inimese kohta ja Ameerika Ühendriikides üks 260 tuhande inimese kohta. [3]
Põhjused lümfoplasmatsüütiline lümfoom
Praeguseks on enamiku vähivormide etioloogia teadmata, kuid mõnede vähivormide geneetilise aluse uurimine jätkub. Uurides pahaloomuliste plasmarakkude haiguste , sealhulgas B-rakulise lümfoplasmatsüütilise lümfoomi ( Waldenströmi makroglobulineemia) põhjuseid, on teadlased leidnud seose B - lümfotsüütide patoloogilise proliferatsiooni (rakkude jagunemise) vahel nende diferentseerumise hilises staadiumis teatud molekulaarsete rakkude olemasoluga. Geenihäired, mis muudavad raku põhifunktsioone.
Waldenströmi makroglobulineemiaga patsientidel ilmnesid muutused mõnedes geenides - somaatilised mutatsioonid, see tähendab, et need mõjutavad ainult kudesid, millel on rakkude eraldi kloonse populatsiooni geenide kahjustus ja mis moodustavad nende genoomi variante, mis põhjustavad tsüklilisi ja struktuurseid häireid. Raku tase.
Esiteks on need geeni MYD88 (L265P) somaatilised mutatsioonid ja CXCR4, mis kodeerib tsütosoolset valku, mis on oluline kaasasündinud ja adaptiivse immuunvastuse jaoks: adapterina annab see signaali põletikueelse vahendaja IL-1 kohta. (interleukiin-1) ja Toll-sarnased rakud.retseptorid, mis aktiveerivad immuunvastust. Somaatilise mutatsiooni tulemusena tekivad antud valgumolekuli polüpeptiidahela, selle struktuurse baasi anomaaliad. [4]
Riskitegurid
Lisaks üldistele riskiteguritele (kõrgendatud kiirguse, kantserogeensete kemikaalide jne) ennustajad Waldenströmi makroglobulineemia kui madala raskusastmega lümfoproliferatiivse haiguse tekke tõenäosuse suurenemise kohta on järgmised:
- vanadus (üle 65 aasta);
- selle diagnoosiga sugulaste olemasolu, samuti B-rakulise mitte-Hodgkini lümfoomi või kroonilise lümfotsütaarse leukeemiaga;
- krooniline C- hepatiit ;
- anamneesis healoomuline monoklonaalne gammopaatia, idiopaatiline hematoloogiline haigus, mille põhiolemus on ebanormaalselt muutunud M-tüüpi gammaglobuliinide tootmine lümfotsüütide plasmotsüütide poolt;
- autoimmuunhaigused, eriti Sjögreni sündroom .
Pathogenesis
Antigeeniga kokkupuutel või T-lümfotsüütide stimulatsioonil muutub osa B-lümfotsüütidest plasmarakkudeks - lümfotsüütilisteks plasmotsüütideks, mis pärast teatud transformatsioone hakkavad tootma kaitsvaid globulaarseid valke, see tähendab gammaglobuliine (immunoglobuliine või antikehi).
Lümfoplasmatsüütilise lümfoomi/Waldenströmi makroglobulineemia patogenees seisneb B-rakkude hüperproliferatsioonis, lümfotsüütiliste plasmarakkude klooni normaalse taseme ületamises ja nende toodetud immunoglobuliini M (IgM), mida nimetatakse ka monoklonaalseks immunoglobuliiniks või M. - valk. See on suur suure molekulmassiga pentameerne antikeha, mis tekib spetsiifiliste bakteri- või viirusantigeenide esialgsel rünnakul. [5]
Peaaegu kõik selle haiguse sümptomid on seotud M-valgu aktiivsuse ilmingutega, mis võivad häirida vere reoloogilisi omadusi, suurendada selle viskoossust; immutavad luuüdi lümfoidseid ja müeloidseid kudesid, akumuleeruvad perifeersetes lümfoidkudedes (koos aeglaselt kasvavate neoplaasiate moodustumisega, mis võivad avaldada survet ümbritsevatele organitele, närvikiududele või veresoontele).
Kuigi krooniline lümfotsütaarne leukeemia, Waldenströmi makroglobulineemia või lümfoplasmatsüütiline lümfoom ja hulgimüeloom on eraldiseisvad haigused, on need kõik põhjustatud B-lümfotsüütide suurenenud proliferatsioonist.
Sümptomid lümfoplasmatsüütiline lümfoom
Esimesed haigusnähud on mittespetsiifilised ja võivad avalduda nõrkuses ja väsimuses (normokroomse aneemia tekke tõttu), kehakaalu langusena, õhupuuduses, öises liighigistamises ja korduvas madala palaviku palavikus.
Lisaks on haiguse algstaadiumis käte ja jalgade tundlikkuse rikkumine, perifeerne neuropaatia (jalgade ja jalgade tuimus või kipitus), naha kapillaaride väikesed fokaalsed hemorraagiad (purpur), samuti külm urtikaaria (ebanormaalsete krüoglobuliinivalkude moodustumise ja agregatsiooni tõttu seerumis).
Hüperviskoossussündroomiga seotud sümptomiteks on peavalud ja pearinglus, võrkkesta kahjustus ja nägemise hägustumine, tinnitus ja kuulmislangus, krambid, lihasvalu, kõrge vererõhk, spontaanne ninaverejooks ja igemete veritsemine. Naistel on võimalik emakaverejooks.
Täheldatud ka: lümfisõlmede suurenemist (lümfadenopaatia); põrna suurenemine (splenomegaalia); südamepuudulikkus koos kardialgia ja südame arütmiaga. Kuigi vistseraalne infiltratsioon on haruldane, võib see mõjutada magu ja soolestikku, mille tagajärjeks on kõhulahtisus (sageli rasvase väljaheitega). [6], [7]
Vormid
Maailma Terviseorganisatsiooni 2017. Aasta hematopoeetiliste ja lümfoidkoe kasvajate klassifikatsioon kehtestab Waldenströmi makroglobulineemia neli diagnostilist kriteeriumi, sealhulgas:
- Monoklonaalse IgM gammopaatia olemasolu
- Luuüdi infiltratsioon väikeste lümfotsüütidega, mis näitavad plasmatsütoidset või plasmarakkude diferentseerumist
- Intertrabekulaarse struktuuriga luuüdi infiltratsioon
- Waldenströmi makroglobulineemiat toetav immunofenotüüp, mis hõlmab pinna IgM+, CD19+, CD20+, CD22+, CD25+, CD27+, FMC7+, muutuvat CD5, CD10-, CD23-, CD103- ja CD108-
Tüsistused ja tagajärjed
Lümfoplasmatsüütilise lümfoomiga patsientidel tekivad tüsistused ja tagajärjed:
- immuunsuse vähenemine;
- luuüdi puudulikkus koos selle hematopoeetiliste funktsioonide rikkumise ja aneemia tekkega;
- selliste moodustunud vereelementide nagu erütrotsüüdid, leukotsüüdid, trombotsüütide puudumine;
- seedetrakti struktuuride kahjustus kroonilise kõhulahtisuse ja soolestiku imendumise häiretega (malabsorptsiooni sündroom);
- veresoonte seinte põletik (kompleksne immuunvaskuliit);
- suurenenud luude haprus (osteoporoos);
- nägemis- ja kuulmiskahjustused;
- siseorganite sekundaarne amüloidoos ;
- progresseerumine paraproteineemiliseks hemoblastoosiks hulgimüeloomi kujul;
- transformatsioon väga pahaloomuliseks lümfoomi tüübiks – difuusseks suureks B-rakuliseks lümfoomiks.
Diagnostika lümfoplasmatsüütiline lümfoom
Lümfoplasmatsüütilise lümfoomi/Waldenströmi makroglobulineemia diagnoosimine on tavaliselt raske spetsiifiliste morfoloogiliste, immunofenotüüpsete või kromosomaalsete muutuste puudumise tõttu. See puudulikkus eristab seda haigust teistest väikestest B-rakulistest lümfoomidest väljajätmise alusel. [8],
Lisaks olemasolevate sümptomite hindamisele on lümfoplasmatsüütilise lümfoomi diagnoosimiseks vajalikud üldised ja biokeemilised vereanalüüsid, koagulogramm, verevalkude immunoelektroforees koos immunoglobuliini M taseme määramisega veres ; üldine uriinianalüüs. [9]
Vajalik on luuüdi biopsia, mille jaoks tehakse selle punktsioon.
Instrumentaalne diagnostika viiakse läbi: lümfisõlmede ja põrna ultraheliuuring, luude röntgenuuring, rindkere ja kõhuõõne CT, oftalmoskoopia.
Diferentseeritud diagnoos
Lümfoplasmatsüütilist lümfoomi peetakse välistusdiagnoosiks, seetõttu tehakse diferentsiaaldiagnostika B-rakulise kroonilise lümfotsütaarse leukeemia, hulgimüeloomi, follikulaarse lümfoomi, mitte-Hodgkini lümfoomi erinevate alatüüpide, plasmatsütoomi, reaktiivse plasmatsütoosi, angiofollikulaarse lümfoidse hüperplaasia (Castlemani tõbi) korral., jne.
Kellega ühendust võtta?
Ravi lümfoplasmatsüütiline lümfoom
Tuleb meeles pidada, et Waldenströmi makroglobulineemia ehk lümfoplasmatsüütiline lümfoom võib olla aastaid asümptomaatiline ja diagnoositud M-valgu taseme tõusuga veres.
Sümptomite puudumisel viiakse läbi aktiivne jälgimine regulaarsete uuringute ja testidega.
Olemasolevate sümptomite ja laboratoorsete analüüside tulemuste põhjal tehakse otsus alustada ravi, mis sõltub paljudest teguritest (näiteks vanus, haiguse progresseerumine jne).
Protokolli kohaselt on seda tüüpi lümfoomiga patsientide esialgne ravi tavaliselt kiiritusravi ja keemiaravi kombinatsioon tsütostaatikumide, näiteks tsüklofosfamiidi , doksorubitsiini, vinkristiini, aga ka kortikosteroidide - metprednisoloon või deksametasoon (deksasoon) kasutuselevõtuga..
Monoklonaalsete antikehade rühma kuuluvate keemiaravi ravimite, eriti rituksimabi, efektiivsus on tõestatud . [10]
Üldise haiguse korral kasutatakse rituksimabi kombinatsioonis kasvajavastaste nukleosiidi analoogidega (pentostatiin, kladribiin). Aeglaselt progresseeruva haiguse korral, mille monoklonaalse immunoglobuliini M tase on madal, kasutatakse lisaks rituksimabile tsütostaatilist klorambutsiili (Leukeran). [11]
Vere viskoossuse vähendamiseks ja selle moodustunud elementide taseme stabiliseerimiseks kasutatakse terapeutilist hemafereesi .
Kriitiliselt madala antikehade tasemega veres - samaaegsete uuesti nakatumise vältimiseks - viiakse läbi immunoglobuliinide asendusravi.
Vaatamata asjaolule, et ravi võib viia haiguse remissioonini, kogeb onkohematoloogide sõnul enamik patsiente selle retsidiivi. Kui see ilmneb varem kui 24 kuud, võib kasutada vähivastast ravimit, nagu Ibrutiniib (tablettide kujul). Hilisemate ägenemiste korral toimub ravi vastavalt esialgsele skeemile. [12].. [13]_ [14]
Ärahoidmine
Spetsialistid määravad lümfoplasmatsüütilise lümfoomi tulemuste prognoosi vastavalt rahvusvahelisele prognostilisele süsteemile peamiste parameetrite hindamiseks: patsiendi vanus ja hemoglobiini, trombotsüütide, beeta-2-mikroglobuliini ja monoklonaalse immunoglobuliini tase seerumis. [15], [16]
Selle diagnoosi keskmine elulemus on umbes viis aastat, kuid peaaegu 40% patsientidest elab kümme aastat või kauem.

